Clear Sky Science · zh
微小RNA通过细胞外基质和发育通路塑造小鼠对太空飞行的无年龄差异组织适应
为什么太空旅行会改变我们的身体
随着前往月球和火星的旅程从科幻走向严肃规划,一个重要问题仍待回答:长期太空飞行如何在分子层面重塑身体?宇航员会丧失骨质和肌肉,心脏与免疫系统发生变化,其中一些问题类似于地球上的年龄相关疾病。本研究利用在国际空间站生活数周的小鼠,揭示了被称为微小RNA的微小基因调节因子如何帮助全身器官在轨道生活中适应——或可能出现功能失常。
对轨道小鼠的全身观察
为了超越单一器官的研究,研究者检查了来自13种器官的686个样本,这些雌性小鼠在空间站飞行三到六周。他们将这些动物与两组地面对照进行了比较:一组在正常实验室条件下饲养,另一组置于模拟空间站狭小环境、温度、湿度和升高二氧化碳的特殊笼中。这样的设计使团队能够区分哪些变化来自太空本身——失重和辐射——以及哪些来自小鼠经历的不寻常饲养和操作。他们聚焦于微小RNA,这是一类虽不编码蛋白质但能同时调节许多基因活性的短链RNA。
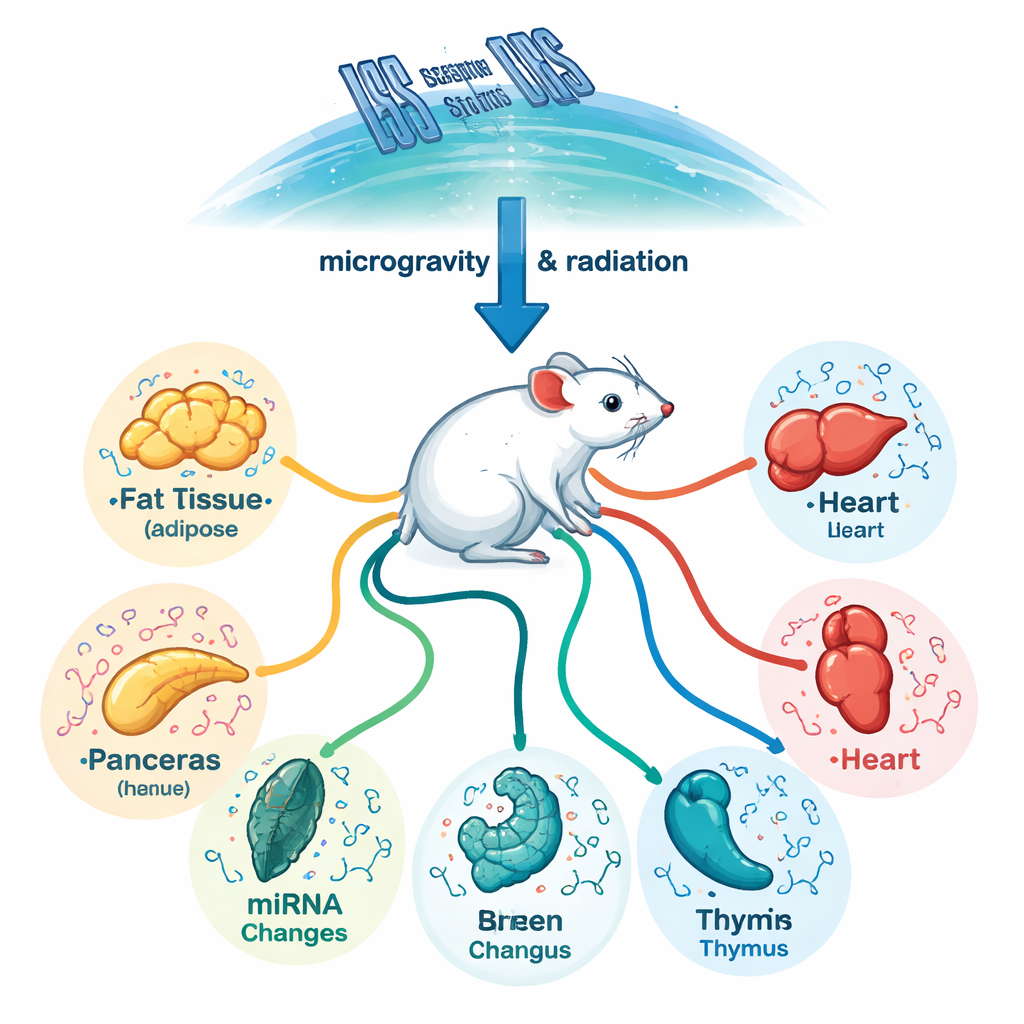
关键器官中的微小RNA主控开关
每个器官都有其独特的微小RNA“拨盘设定”,但太空飞行以特定模式改变了这些拨盘。皮下和器官周围的脂肪库,以及肝脏、胰腺、脾脏和胸腺表现出最强的太空驱动改变,而大脑、肾脏和某些脂肪库则更容易受地面饲养条件影响。团队发现了73种在太空暴露动物中稳定改变的微小RNA,且常表现出器官特异性。相关的微小RNA家族——尤其是MIR-17/92和MIR-1/133——脱颖而出成为主要参与者。这些家族在地球上与心脏功能、癌症和代谢有关,表明一小部分调控分子可能协调身体对离开地球生活的多种反应。
组织重塑与损伤修复
由于微小RNA通过调节信使RNA水平发挥作用——信使RNA是蛋白质的直接蓝图——研究者将微小RNA数据与来自同一批动物的单细胞基因活动图谱结合。这揭示了数千个与微小RNA变化相匹配的基因改变,尤其集中在脂肪组织、肝脏、肺、心脏和脾脏。受影响的基因聚集在重塑组织结构与处理应激的通路:构建与降解维持细胞连接的细胞外基质、引导细胞生长与迁移、调节神经与突触结构,以及应对来自辐射的DNA损伤。例如在脂肪组织中,微小RNA影响了参与血管生成和细胞物理支架的基因,指向代谢器官的大规模重塑。在胸腺和其他免疫器官中,微小RNA靶向控制DNA修复与免疫细胞成熟的转录因子,暗示对感染防御乃至潜在癌症风险的复杂影响。
太空应激与单纯衰老的区别
许多宇航员的症状与衰老脆弱性相似,因此团队探讨了太空飞行是否仅仅加速了正常的衰老钟。他们比较了成年早期小鼠(约三个月)与中年小鼠(约八个月),并将结果与地球上大规模小鼠年龄相关微小RNA变化图谱交叉比对。年龄确实有影响,但不及太空飞行本身:在大多数组织中,太空在两年龄组中引起了相似的变化。只有少数器官,特别是胰腺、膈肌(主要呼吸肌)和特定腹部脂肪库,表现出明显的年龄依赖性反应。在这些组织中,三大家族的微小RNA——MIR-8、MIR-15和MIR-154——尤其活跃,靶向控制细胞生长、肌肉维持和与癌症相关过程的基因。令人意外的是,总体模式并不简单地匹配正常衰老的加速:一些微小RNA遵循类似衰老的趋势,而另一些则走出独特的、太空特异的路径。
对未来探索者的意义
对非专业读者而言,核心信息是:数周的轨道生活将许多器官推向一个协调的重塑程序,由一小群微小RNA主导,它们同时调节数百个基因。这些改变有助于组织应对失重和辐射,但也可能将组织推向类似糖尿病、心脏问题和癌症的病态状态。重要的是,研究发现更支持一种独特的“太空状态”而非单纯的快速衰老,且年长小鼠仍能做出强烈反应。如果类似模式在人类中成立,这表明针对少数关键微小RNA家族的靶向药物或基因治疗,或许能在未来保护宇航员的器官——并且即使是中年探索者在学会如何向正确方向引导这些分子开关后,也可能安全参与长期任务。
引用: Grandke, F., Rishik, S., Wagner, V. et al. MiRNAs shape mouse age-independent tissue adaptation to spaceflight via ECM and developmental pathways. Nat Commun 17, 1387 (2026). https://doi.org/10.1038/s41467-026-68737-1
关键词: 太空生物学, 微小RNA, 组织重塑, 细胞外基质, 衰老与太空