Clear Sky Science · zh
镍催化的丙炔基碳酸酯发散性磺化反应
这门化学为何超越实验室重要
含硫分子是许多现代药物、农用保护剂和先进材料的核心。然而,以精确、高效且灵活的方式制备这些化合物往往很困难。本文描述了一种基于镍的催化方法,能够把简单的起始物转化为几类不同的富含硫的分子,而且对三维构型具有严格控制。这样的控制力可以加速药物发现,并帮助化学家以更清洁、更可持续的方式构建复杂分子。
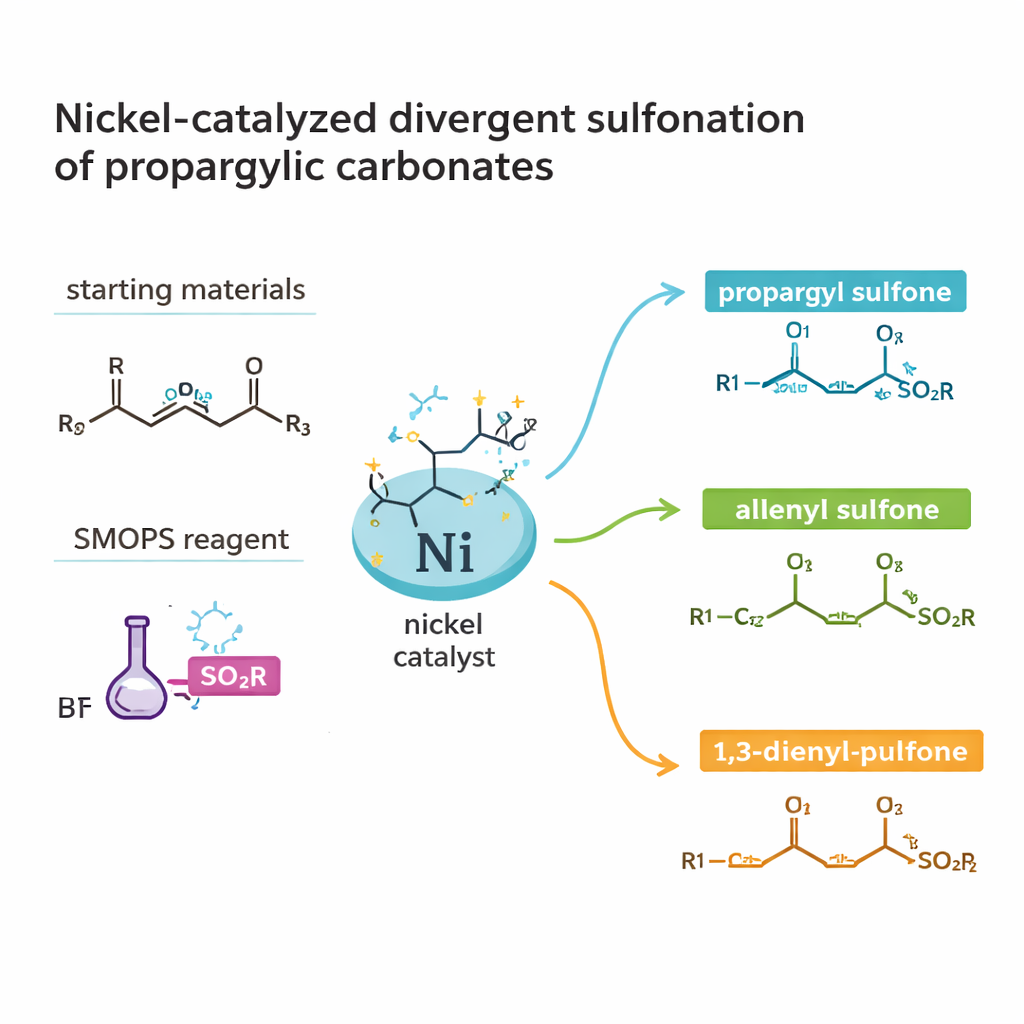
从简单片段构建有用分子
这项工作聚焦于一类称为磺(sulfones)和亚磺酸盐(sulfinates)的分子,它们含有与氧和碳相连的硫。这些结构在具有生物活性的天然产物和药物中广泛出现,但传统合成路线往往冗长且浪费。作者关注一种特别有价值的亚型:手性亚磺酸盐,其对映体在体内可能表现出截然不同的行为。他们并不从已复杂化的构建块出发,而是使用两种现成的反应伙伴:丙炔基碳酸酯(一类带有离去基的小碳骨架)和一种商用硫源 SMOPS。通过在镍催化下将二者组合,他们目标是在一到两步内生成极具价值的含硫产物。
一套催化体系,三类产物
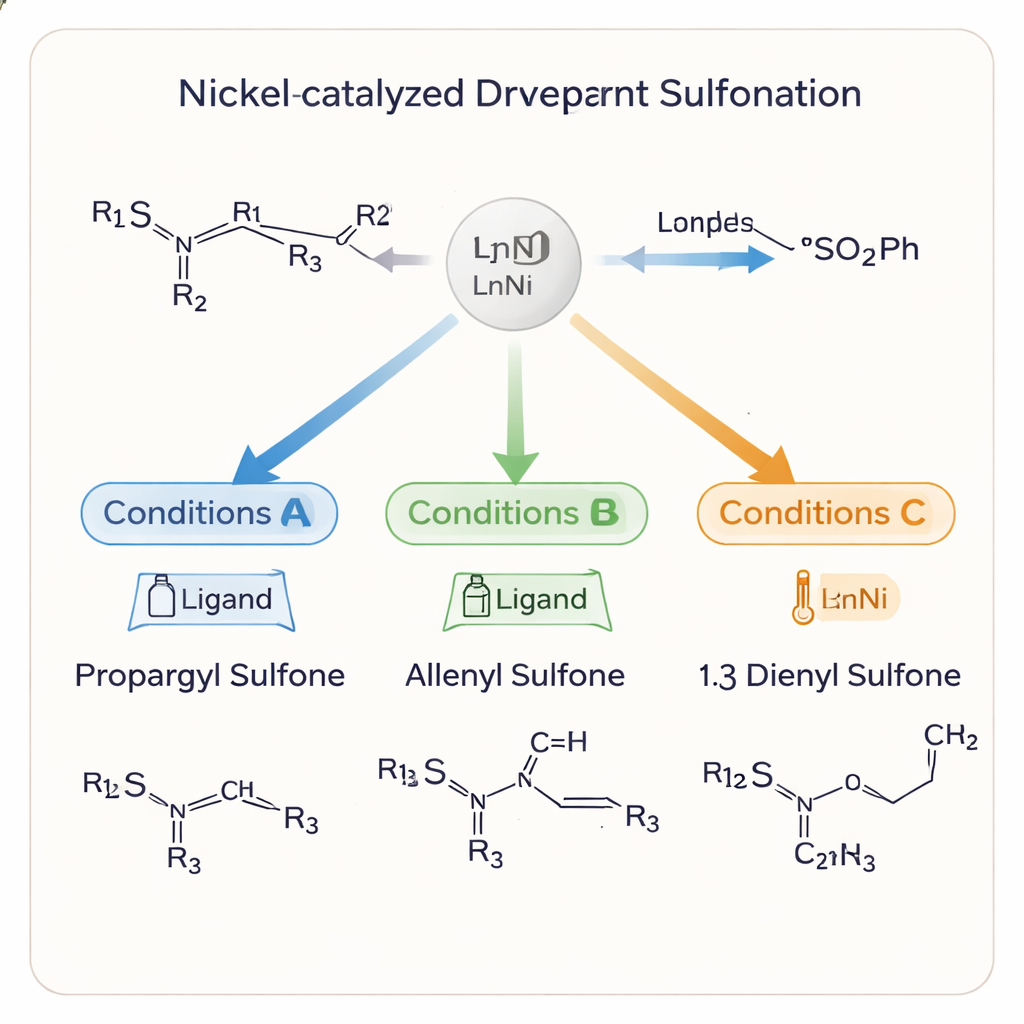
该研究的显著特点是,相同的基本试剂在不同条件下可以导向三种截然不同的产物类型:丙炔基磺、亚炔烯(allenyl)磺和1,3‑二烯基磺。每一种碳骨架会引出不同的后续化学反应和生物活性。通过精心选择与镍配位的配体、溶剂、温度和添加剂,研究团队能够“操控”反应走向某一结果。在乙腈、温和条件下并使用手性膦配体时,他们能高产率并以优异的立体选择性获得丙炔基磺。将这些产物用氧化铝温和处理可以将碳–碳三键重塑为全烯,同时保留手性信息。换用不同的配体和溶剂,则可将过程引导为生成1,3‑二烯基磺,从而延展碳骨架。
检验适用范围与柔性
为评估该方法的通用性,研究者改变了两种反应物。他们展示了许多不同的钠亚磺酸盐,包括简单的烷基、芳基以及更复杂的环系,都能干净地参与反应并得到高对映纯度的手性产物。同样,带有不同芳环或碳链取代基的广泛丙炔基碳酸酯也能良好反应,尽管一些非常体积庞大的底物或端炔类目前不适用。团队还证明了该反应可放大到更大规模而不牺牲效率或选择性,这是走向实用化的重要一步。宽泛的适用范围意味着化学家可以插入多种片段,迅速获得一系列相关的含硫分子库。
将构建块转化为复杂靶分子
除了直接合成这些磺类,作者还展示了它们如何方便地转化为其他有用结构。加氢可将三键还原为烷或烯,同时保留硫邻位的手性中心。简单的后续反应能将磺基单元转化为亚磺酸盐、磺酰胺和磺酰氟——这些基序在药物化学和“类点击”键合反应中常见。作为亮点,他们将该方法作为关键步骤,简洁合成了一种手性β‑亚磺酰羟肟酸,这类分子已知可抑制细菌酶。这一路线避免了若干较旧且繁琐的步骤,强调了按需获得手性亚磺酸盐的合成优势。
反应如何选择路径
团队还探究了反应为何以及如何在不同产物间切换。时间进程实验显示,丙炔基磺通常首先形成,然后在特定条件下可以重排为全烯,最终转化为1,3‑二烯。镍催化剂与所选配体和添加剂共同控制了哪些中间体被偏好以及硫基如何沿碳链迁移。例如,氧化铝允许在非常低温下进行炔到全烯的重塑,同时保持原有的三维构型。简化的机理表明,反应条件的细微变化会将共同的镍中间体引导到不同的路径上,从而解释了为何一个体系能生成多种精确定义的产物。
这对未来药物和材料的意义
对非专业读者来说,关键结论是:这种镍催化方法提供了一个多功能的化学“开关板”:用相同的简单起始片段,化学家可以选择所需的富硫骨架,并在一步高选择性反应中得到它们。由于这些产物是药物及其他功能分子的优秀构建基块,该方法可缩短从概念到候选化合物的路径。它也展示了通过精心设计催化剂和反应条件,曾经具有挑战性的转化可以成为日常工具,从而为更快、更清洁地构建复杂手性含硫分子打开大门。
引用: Gu, W., He, Z., Wang, H. et al. Nickel-catalyzed divergent sulfonations of propargylic carbonate. Nat Commun 17, 1882 (2026). https://doi.org/10.1038/s41467-026-68720-w
关键词: 镍催化, 手性磺, 不对称合成, 有机反应设计, 类药物构建基块