Clear Sky Science · zh
肿瘤内在特征通过从前驱期到有症状的多发性骨髓瘤塑造T细胞分化
这项研究为何重要
多发性骨髓瘤是一种在骨髓中形成的血液癌症,几乎总是由更为“静默”的早期状态先行,这些早期状态可能会也可能不会演变为明显的疾病。许多人在这些前驱阶段中多年生存,却不确定是否或何时会进展。本研究提出了一个及时的问题:我们能否通过解读免疫系统——尤其是T细胞的“状态”和历史,来理解骨髓瘤如何发展、如何响应治疗以及谁最有可能进展?
身体的抗癌侦察兵
T细胞是多功能的免疫细胞,能识别并消灭异常细胞,包括癌细胞。在肺癌或皮肤癌等实体瘤中,长期刺激会把T细胞推向一种“耗竭”状态,使其失去效能,而现代免疫疗法正试图逆转这种变化。作者构建了一个庞大的单细胞图谱,包含来自多发性骨髓瘤患者、其前驱期(MGUS和无火花型骨髓瘤)以及非癌症对照的骨髓和血液中超过一百万个细胞。通过同时读取基因活动和定义每个T细胞克隆的独特受体序列,他们重建了T细胞的组织结构、它们看起来有多“老”或有多少“经验”,以及它们与潜在肿瘤之间的联系程度。
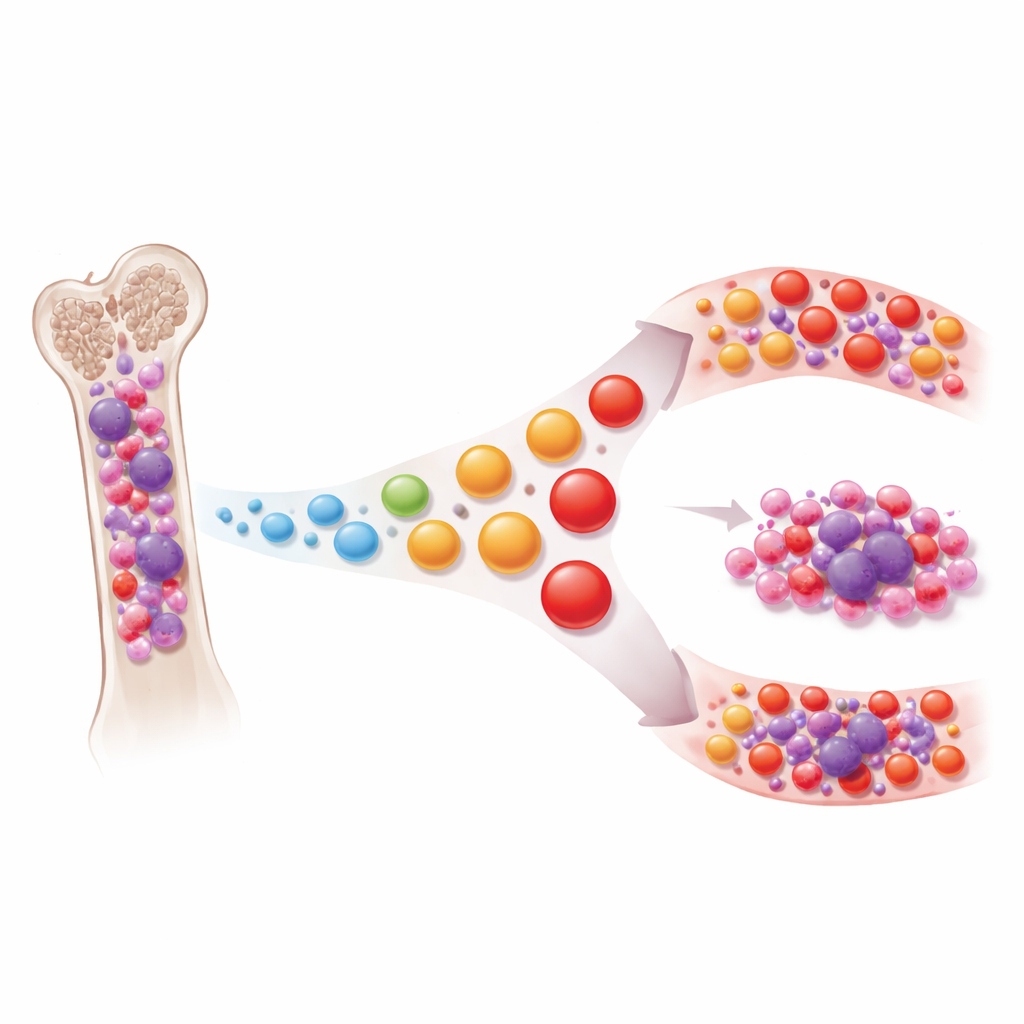
不是疲惫,而是过早老化
与许多实体瘤中看到的情形相反,研究团队发现骨髓瘤中的T细胞很少真正处于经典的耗竭状态。带有传统耗竭标志的细胞主要集中在一位不同寻常的患者中。相反,在无火花型和有症状的骨髓瘤中,骨髓T细胞从幼稚、早期状态转向高度“有经验”的终末记忆类型,这些类型类似于老年个体中的T细胞。这种被称为T细胞偏倚的模式与免疫系统的自然衰老相并行,但在患者中表现得更为夸张,仿佛他们的T细胞比其身体其他部分更快老化。疾病越晚期、肿瘤负荷越高,这种向晚期记忆细胞的偏倚越明显,类似的变化也可见于外周血中。
来自T细胞指纹的线索
每个T细胞携带独特的受体,具有相同受体序列的细胞属于因某种触发而扩增的克隆。通过追踪这些受体,研究者表明骨髓瘤患者的骨髓含有许多扩增的T细胞克隆,具有强效杀伤细胞的特征。这些克隆并非主要识别常见病毒。相反,它们表现出一种独特的“非病毒性”基因签名,关联于强大的细胞毒性机制,并在骨髓瘤患者中比在前驱期更为富集。那些在细胞表面更善于展示蛋白片段——即抗原呈递基因活性较高的肿瘤——往往与这些非病毒性、高度分化的T细胞相关联。肿瘤呈现出更强免疫参与的患者总体生存更好,这提示这些T细胞在一定程度上确实具有抗肿瘤作用。
治疗、复发与早期预警信号
该研究还追踪了接受自体干细胞移植的患者,这是一种常见的强化治疗。移植后,T细胞受体谱系更多被少数大克隆所主导。许多扩张的克隆可以追溯到治疗前已存在的终末分化CD8 T细胞,这些细胞带有相同的非病毒性、与骨髓瘤相关的基因特征。移植后仍有残余癌症的患者通常具有特别克隆化、偏倚的T细胞谱系,这表明一种强烈但类似于老化的T细胞反应可能无法彻底清除疾病。在疾病早期,作者发现那些后来进展为活动性骨髓瘤的无火花型患者往往在调节性CD4 T细胞(通常帮助维持免疫反应与骨髓环境平衡)中出现下降。低水平的这些细胞能独立于既有临床风险评分预测更快的进展。
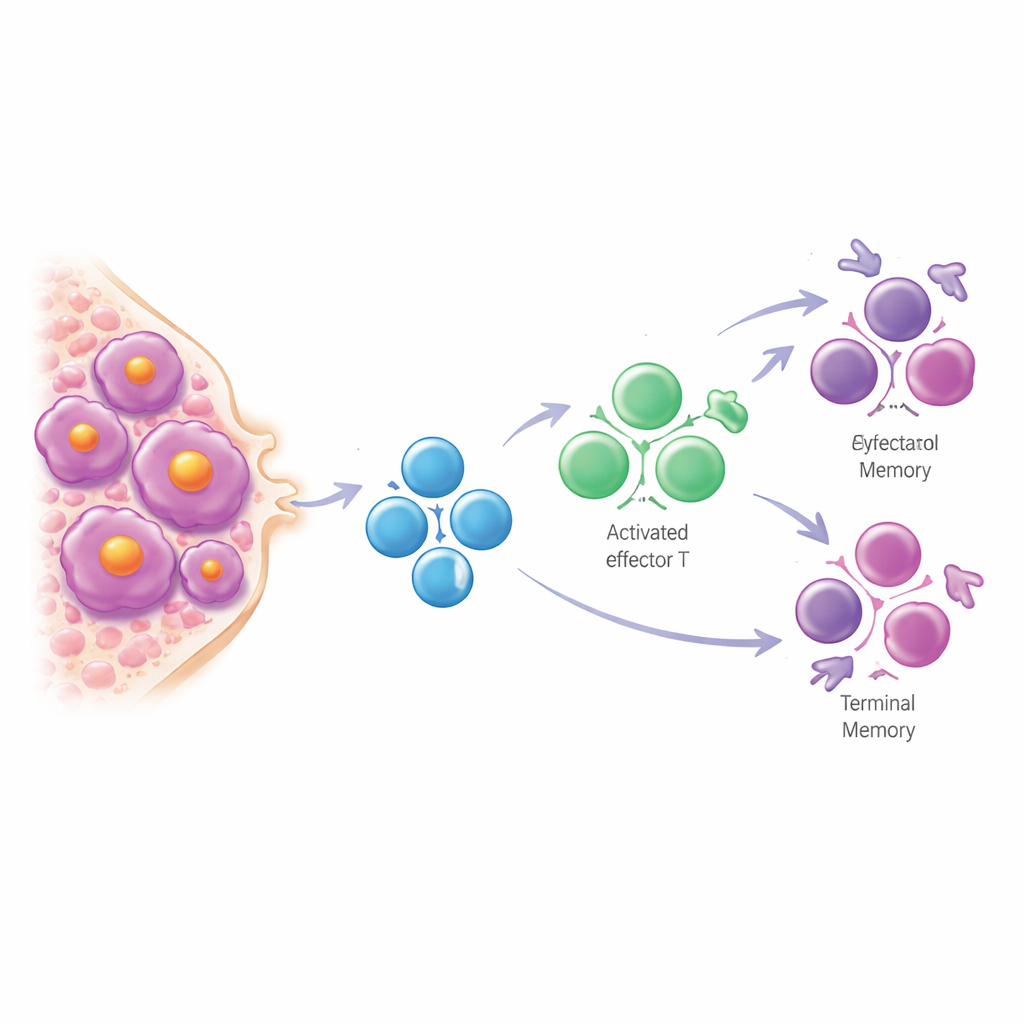
对患者意味着什么
对于与骨髓瘤及其前驱期共存的人群,本研究重新框定了免疫系统如何应对肿瘤。T细胞不像简单地变得耗竭,而是因与肿瘤细胞的持续对抗被长期驱动进入一种晚期、衰老样状态。这种偏倚且克隆化的T细胞景观反映了肿瘤负荷,影响对移植和T细胞相关药物等治疗的反应,并且在调节性T细胞丢失的情况下,能够提示从无火花期进展到有症状疾病的高风险个体。长期来看,这些见解可为开发刷新或重新定向T细胞的免疫疗法提供方向,并帮助临床医生将免疫学特征与传统指标结合,更精确地安排监测与早期干预的时机。
引用: Foster, K.A., Rees, E., Ainley, L. et al. Tumour-intrinsic features shape T cell differentiation through precursor to symptomatic multiple myeloma. Nat Commun 17, 2400 (2026). https://doi.org/10.1038/s41467-026-68718-4
关键词: 多发性骨髓瘤, T细胞, 免疫衰老, 单细胞测序, 癌症免疫学