Clear Sky Science · zh
携带 STK11/LKB1 突变的非小细胞肺癌中的癌症恶病质依赖于肿瘤分泌的 GDF15
为何部分肺癌会导致危险性体重下降
癌症并不总是在单一部位悄无声息地生长。许多患者会出现一种称为恶病质或消瘦的情况,肿瘤逐步掠夺机体的脂肪、肌肉、力量和精力。本研究针对一种常见肺癌形式提出了一个紧迫的问题:为何有些肿瘤会触发这种严重的体重下降,而另一些则不会?研究人员将问题追溯到某些肿瘤产生的一种应激信号,并在动物模型中证明阻断该信号可以在很大程度上阻止甚至逆转消瘦。
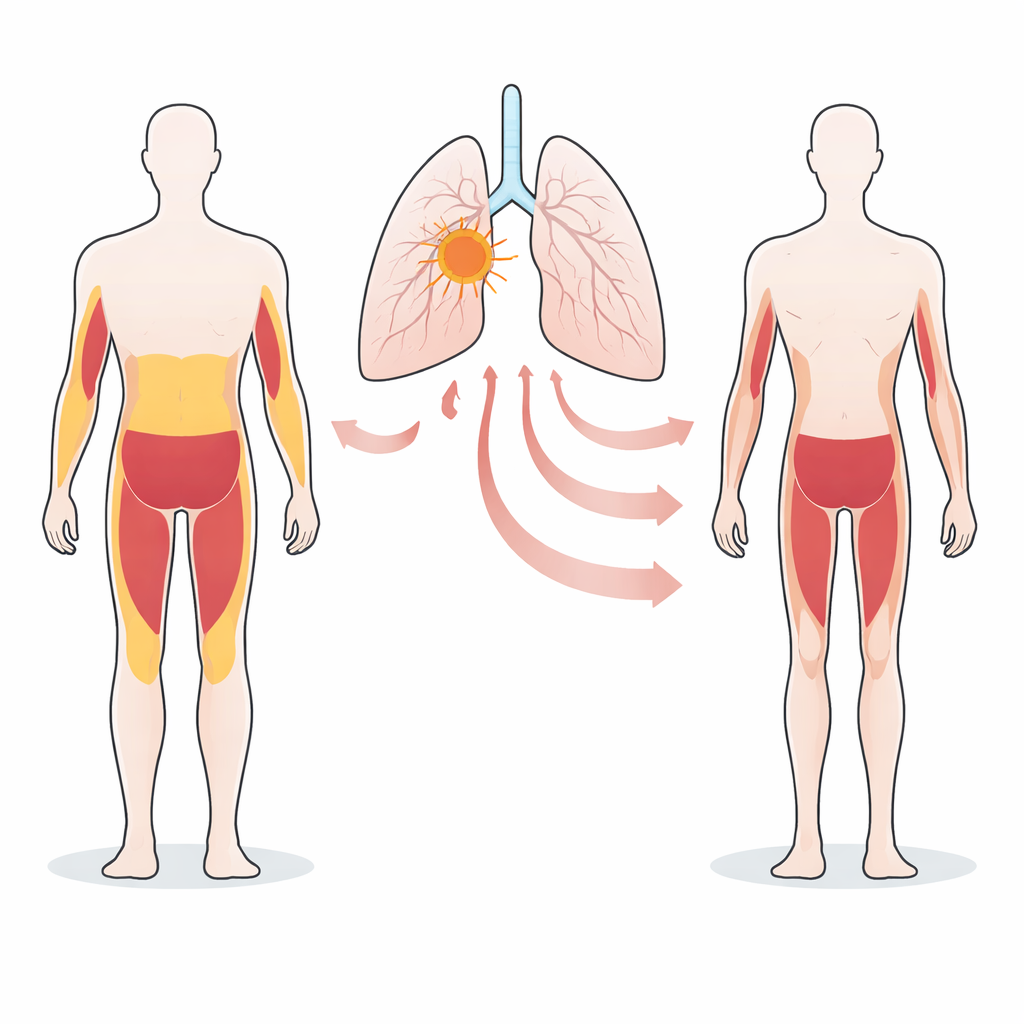
肿瘤基因与全身消耗之间的隐性关联
研究小组聚焦于携带 STK11/LKB1 基因缺陷的非小细胞肺癌。早期工作已显示,拥有该缺陷的肿瘤在小鼠和患者中常伴随显著的体重、脂肪和肌肉流失。在本研究中,科学家比较了多种在小鼠体内生长时会或不会引起消瘦的人类肺肿瘤系。他们发现,带有 STK11/LKB1 缺陷并引发消瘦的肿瘤产生大量一种类似应激激素的蛋白 GDF15,并将其释放到血液中。相比之下,宿主动物自身细胞对血液中 GDF15 的贡献很小,表明肿瘤本身是主要来源。
证实肿瘤信号驱动体重、脂肪和肌肉丧失
为检验肿瘤产生的 GDF15 是否确实导致消瘦,研究者使用基因工具仅在癌细胞中关闭 GDF15,而不影响其他基因。在若干不同的 STK11/LKB1 突变肺癌系中,关闭 GDF15 并未减缓肿瘤生长,但显著保护小鼠免于体重、脂肪量、肌肉量和握力下降。这种保护在雄性和雌性中均可观察到,并且在皮下或直接注入肺内的肿瘤模型中都成立,提示其作用来自释放到血液中的因子,而非肿瘤所在的部位。即便肿瘤产生的 GDF15 量适中,阻断该信号仍然能减弱消瘦,表明相对较低的水平也具有生物学意义。
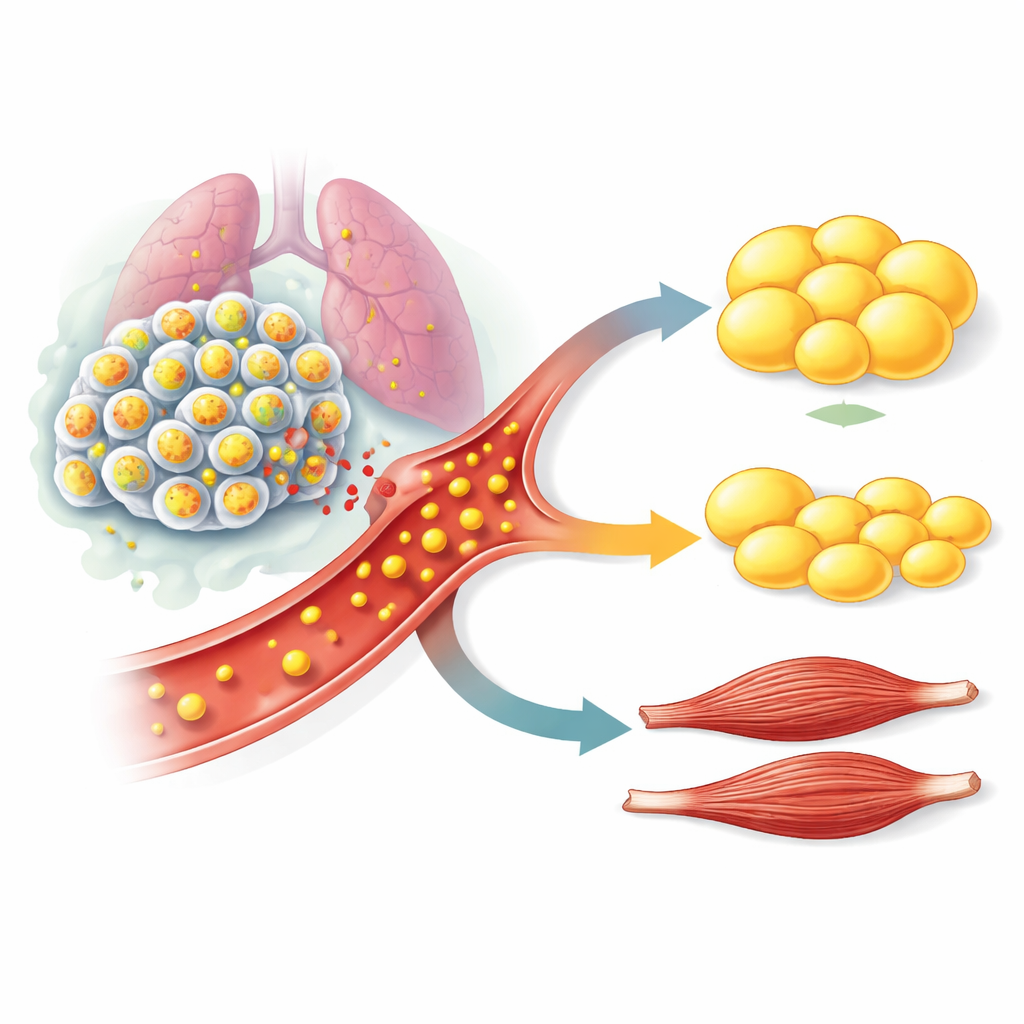
阻断该信号的抗体显示出治疗潜力
由于制药公司已在开发中和临床试验中的中和 GDF15 的抗体,团队评估了这种方法在其模型中的效果。他们用一种类似于正在临床试验中的 GDF15 阻断抗体处理携带 STK11/LKB1 突变肿瘤的小鼠。早期给药时,该抗体能防止通常出现的脂肪、肌肉和力量丧失,而不影响肿瘤的生长速度。即使在晚期给药——动物已丧失大量脂肪之后——相同的抗体仍能阻止进一步恶化并部分恢复体内储备和肌肉重量。在具有完整免疫系统的小鼠肺癌模型中也观察到类似结果,表明这些发现并不局限于免疫缺陷动物。
受压的肿瘤如何打开消耗开关
研究还探讨了为何携带 STK11/LKB1 突变的肿瘤会产生大量 GDF15。细胞利用一种称为应激反应的内在警报系统来应对营养缺乏等威胁。在缺失 STK11/LKB1 的肿瘤中,该警报长期处于活跃状态,促进 GDF15 的产生及其加工为成熟的分泌型形式。当研究者将功能性 STK11/LKB1 基因重新引入到一株人肺癌细胞系中时,应激反应减弱,肿瘤内及血液中的 GDF15 水平显著下降,食欲改善,动物也不再发展为恶病质,尽管肿瘤仍然存在。
这对肺癌患者意味着什么
对于携带 STK11/LKB1 突变的非小细胞肺癌患者,这项工作表明肿瘤本身可以像内分泌器官一样,将 GDF15 释放到血液中,驱动全身性消耗。在小鼠中,通过从肿瘤中移除 GDF15 或在循环中使用抗体阻断 GDF15 都能大幅减少脂肪和肌肉损失,而并非直接缩小肿瘤。这提示在大约 15% 带有 STK11/LKB1 缺陷的肺癌患者中,抗 GDF15 疗法可能有助于在各种血中 GDF15 水平下维持体力和体重。换言之,下调这一由肿瘤产生的单一信号,未来或许能为缓解癌症最使人虚弱的并发症之一提供切实可行的方法。
引用: Yu, J., Guo, T., Gupta, A. et al. Cancer cachexia in STK11/LKB1-mutated non-small cell lung cancer is dependent on tumor-secreted GDF15. Nat Commun 17, 2182 (2026). https://doi.org/10.1038/s41467-026-68702-y
关键词: 癌症恶病质, 非小细胞肺癌, GDF15, STK11 LKB1 突变, 肌肉和脂肪流失