Clear Sky Science · zh
一种由患者来源的 R252C 突变引发的替代 EGFR 激活促进癌症进展
当细胞“天线”失控时
为什么有些癌症在经历化疗和最先进的免疫疗法后仍继续生长?这项研究跟踪了一位同时患有肺部和脑部肿瘤的患者,并将其疾病追溯到细胞表面一个关键“天线”蛋白 EGFR 上的微小变化。通过阐明这一单一突变如何重连生长信号,研究人员不仅解释了该患者侵袭性的癌症,还展示了已有药物阿法替尼如何将其抑制。
罕见突变,深远影响
EGFR 是横跨细胞膜的受体,帮助细胞响应生长信号。许多肺癌和脑癌携带 EGFR 突变,但多数已知的改变位于细胞内、充当酶开关的那一段。在这里,团队发现了一个不寻常的外部位点变化,发生在通常用于结合生长因子的区域。在一位同时患有肺癌和胶质瘤的患者体内,他们发现位于第 252 位的氨基酸由精氨酸被置换为半胱氨酸——命名为 EGFR R252C。对癌症数据库的挖掘显示,这一突变在少数胶质瘤患者中出现,而在肺癌中几乎未见,提示其罕见但确实存在。研究者用基因编辑工具在若干人类脑癌和肺癌细胞系中复现了这一精确突变,以检测其功能。
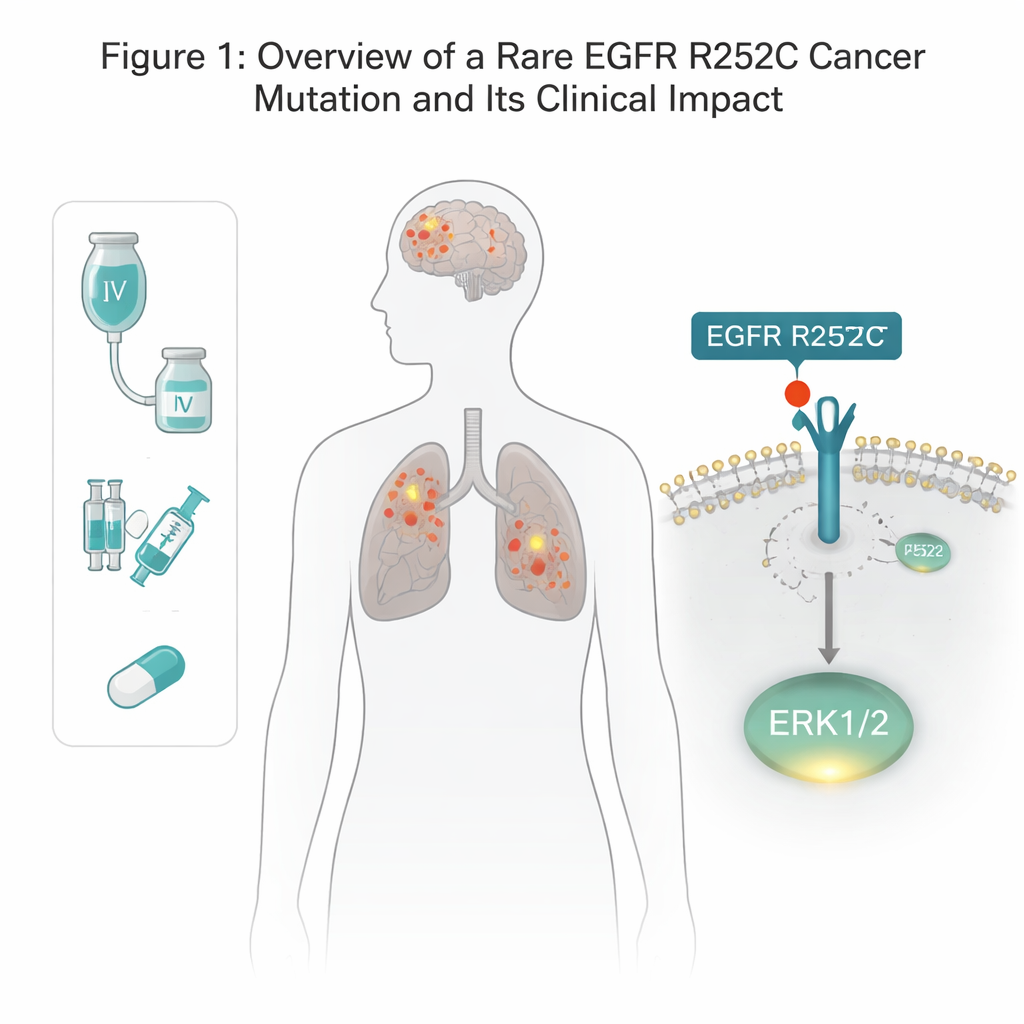
通往生长信号的新捷径
通常,EGFR 需要与另一个副本配对,然后在其内侧尾部自磷酸化,才能开启下游生长通路。令人惊讶的是,R252C 型并未显示这种典型的自磷酸化。相反,携带 EGFR R252C 的细胞显著激活了一个特定的生长调控器 ERK1/2,而其他经典的 EGFR 通路——如 AKT 和 STAT3——基本保持不变。用针对 ERK1/2 的抑制剂阻断其活性后,R252C 细胞额外的生长优势被抹去,证明 ERK1/2 是该突变驱动肿瘤的主要动力。
将受体锁定在持续开启的构象
为理解外部改变如何引起如此选择性的过度激活,研究人员将生化检测与计算模拟结合。R252C 置换在 EGFR 的外部引入了一个新的半胱氨酸。两个这样的突变体可以在它们的 C252 残基之间形成二硫键——一种分子“订书钉”——把它们锁定成稳定的偶联体。结构建模显示,这一二硫键迫使受体的外部呈现“V”形、错落的排列,这种构象很像配体结合时的活性形态,即便没有生长因子存在也能模拟活性。该排列向穿膜段及近膜内段传递,扭转内侧的酶结构域成一种异常构型:活性位点朝向细胞但彼此保持过远,无法高效相互磷酸化。相反,这种构象形成了一个强有力的 ERK1/2 停靠表面,使得 EGFR R252C 能直接磷酸化 ERK1/2,绕过常规的 RAS–RAF–MEK 中继。
从小鼠模型到单例患者
作者证明,携带 EGFR R252C 的脑和肺癌细胞在培养皿中生长更快,移植到小鼠体内后形成的肿瘤也更大、更具侵袭性,相较于携带正常 EGFR 的细胞。他们随后测试了几代 EGFR 抑制剂。只有第二代抑制剂阿法替尼能持续抑制 ERK1/2 激活并显著降低肿瘤细胞生长。在以 R252C 驱动的脑和肺肿瘤小鼠模型中,阿法替尼减缓了肿瘤扩张并延长了生存期。关键是,当原始患者在化疗、抗血管生成药物和免疫疗法后病情恶化并改用阿法替尼时,肺和脑的影像显示肿瘤负荷明显缩小,患者享有数年无进展生存期。
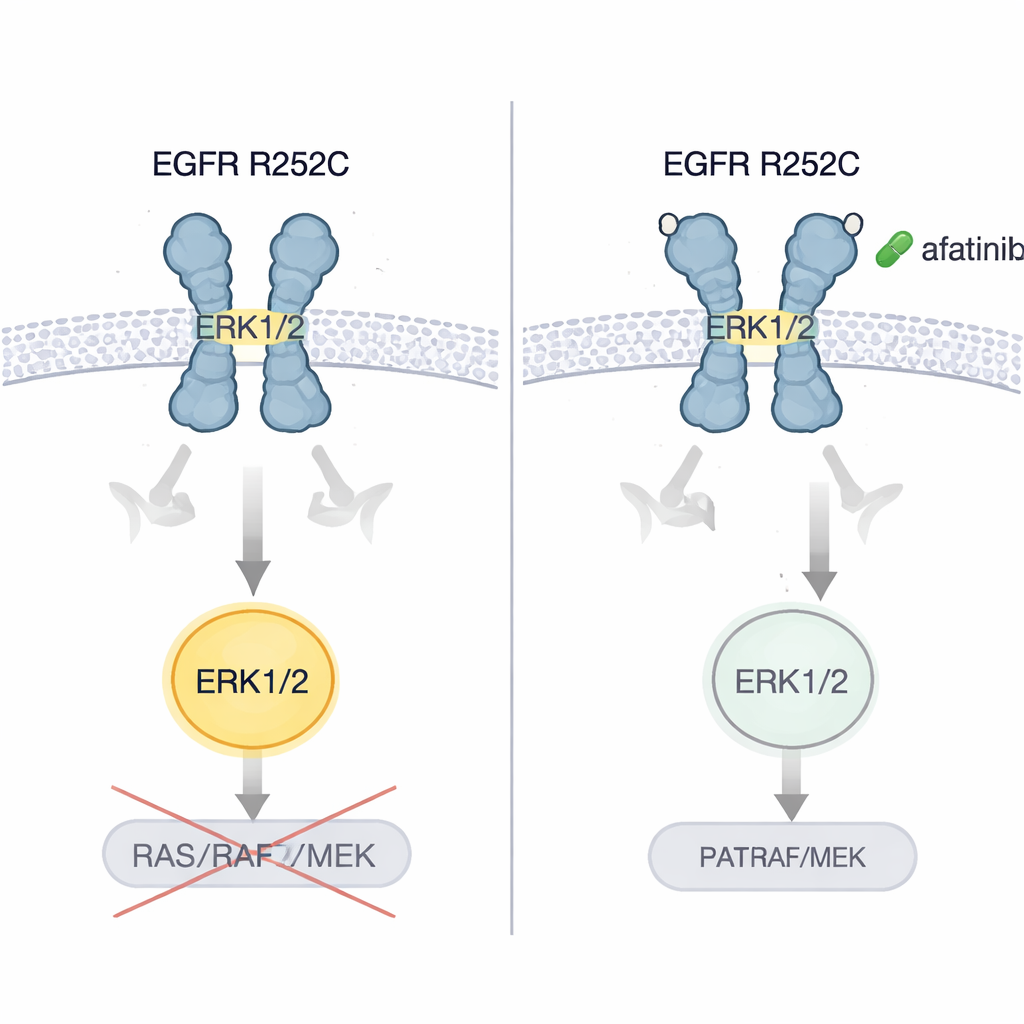
这对患者意味着什么
这项工作揭示了一种此前未被识别的致癌 EGFR 突变作用机制:通过在细胞外把两个受体“订”在一起,将它们扭成一种能直接开启 ERK1/2 的活跃构象,而不是沿教科书式的信号链传递。对非专业读者而言,关键要点是:同一基因中的不同突变行为可能截然不同,一些罕见改变可能最适合用特定的现有药物治疗。EGFR R252C 似乎导致的肿瘤对阿法替尼特别敏感。虽然这一结论目前基于一例详尽的患者病例加大量实验室工作,但它指向了对应 EGFR 外域突变进行更个体化检测的方向,并暗示精心选择的靶向治疗可能为某些难治的脑与肺肿瘤患者带来新的希望。
引用: Zhang, Y., Fei, Q., Li, Y. et al. An alternative EGFR activation by patient-derived R252C mutation promotes cancer progression. Nat Commun 17, 1902 (2026). https://doi.org/10.1038/s41467-026-68699-4
关键词: EGFR 突变, 神经胶质瘤, 肺癌, ERK 信号通路, 阿法替尼