Clear Sky Science · zh
关于β- Arrestin 1与Gαs或Gαi1相互作用的功能与结构见解
这为何与健康和医学有关
如今的许多药物——从抗过敏药到心血管药物和精神科治疗——都以一大家族的细胞表面蛋白为靶点,这类蛋白称为G蛋白偶联受体(GPCR)。这些受体通过两类主要辅助者将信息传入细胞:G蛋白和称为β-逮捕素的蛋白。本研究考察了一种β-逮捕素(β-逮捕素1)如何直接与细胞内的两种G蛋白类型对话。理解这一隐蔽的“对话”可能帮助科学家设计更精确的药物,通过微调细胞内信号流向来减少副作用。
细胞内的两类主要信使
当激素或药物与细胞表面的GPCR结合时,会触发两条大致独立的传导路线。一条由G蛋白介导,G蛋白像分子计时器一样通过用另一种小分子(GTP)替换GDP来开关。另一条由β-逮捕素承担,β-逮捕素既能终止G蛋白信号,也能启动自身的信号通路。长期以来,科学家主要分别研究受体如何与G蛋白或与β-逮捕素相互作用。近期工作提示G蛋白与β-逮捕素可能也会彼此结合,甚至与受体形成大的“巨型复合体”。但这些蛋白如何连接以及这对信号传导意味着什么,仍不清楚。
测量谁与谁结合
在这项研究中,研究者将焦点放在β-逮捕素1和两种G蛋白α亚基:通常激活细胞活动的Gαs以及通常抑制细胞活动的Gαi1。他们使用一种高灵敏度的结合检测技术,测试在不同条件下纯化的β-逮捕素1与每种G蛋白的结合强度。结果表明,关键因素并非G蛋白处于“开”还是“关”,而是β-逮捕素1是否处于更为活跃、柔性的构象。缺失尾端的β-逮捕素1版本——表现为松散、活性样的构象集合——与Gαs和Gαi1都强烈结合。相比之下,静息形式的β-逮捕素1或被受体尾类似肽锁定的形式,结合弱或根本不结合。这提示G蛋白更倾向识别那些采样活性样构象的β-逮捕素1,这种构象可能在受体激活后出现。 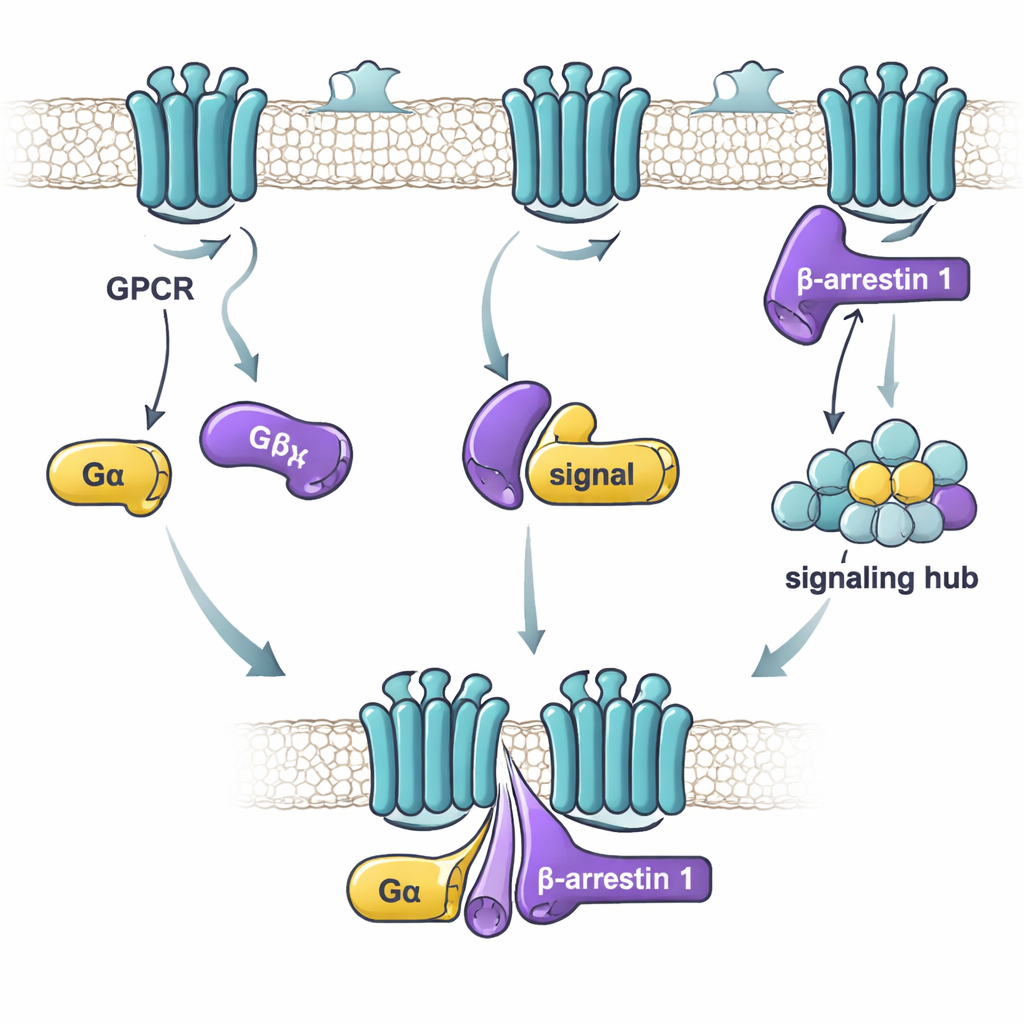
观察微妙的构象变化
为了看清结合如何影响蛋白构象,研究团队使用了一种方法,追踪蛋白主链上的氢原子与溶剂中重氢(氘)的交换速率。交换变慢通常意味着某一区域变得更受保护或更刚性;交换加快则表示该区域更柔性或暴露。当活性样的β-逮捕素1片段与Gαs或Gαi1结合时,两种G蛋白在多个区域都显示出明显的模式变化,表明它们围绕复合体发生了重塑。相比之下,β-逮捕素1本身仅发生了轻微改变,主要集中在柔性环区。通过使用G蛋白的分离结构域,研究者还表明主催化的“Ras样”部分与周围的α螺旋部分都参与结合。对于Gαs,螺旋域发挥了尤为重要的作用;而对Gαi1,两者大致同等重要。
不改变主开关却有功能作用
下一个问题是这种直接接触是否会改变G蛋白的开启行为。团队使用了一种荧光GTP模拟探针,当G蛋白从GDP切换到GTP时会发光,这是衡量活化的标准读数。出人意料的是,加入β-逮捕素1并未改变Gαs或Gαi1的核苷酸交换速度或程度。换言之,β-逮捕素1并不充当传统的使G蛋白“开启”的酶。相反,其影响体现在自身构象上。利用一种经过巧妙设计、其尾部运动可通过荧光追踪的β-逮捕素1,他们发现有受体来源肽存在时,活性Gαs(但非Gαi1)能够促进β-逮捕素C端尾的释放。在活细胞中,额外的成像和能量传递传感器证实,激素刺激时Gαs与β-逮捕素1会靠近,并且Gαs有助于将β-逮捕素1推动到更活性的构象。
细胞信号传导中新的一层调控
综合这些结果,研究提出Gαs和Gαi1都能直接与β-逮捕素1结合,但结合方式略有不同,后果也不同。两种G蛋白的主要“开/关”行为并未被此接触改变。相反,尤其是对Gαs而言,这种相互作用更像是在β-逮捕素1上微调的旋钮,推动或稳定其更活性、尾部释放的形式。这为GPCR信号传导增添了此前被低估的一层:受体不仅能协调G蛋白与β-逮捕素,G蛋白与β-逮捕素也能相互直接调节。长期来看,绘制这些微妙相互作用的图谱,有助于药物设计者引导信号朝有益路径发展——增强有利通路,同时避开引起副作用的通路。
引用: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
关键词: G蛋白偶联受体, β-逮捕素, G蛋白信号传导, 细胞信号机制, 结构生物学