Clear Sky Science · zh
全基因组表观组分析发现儿童期癌症治疗相关心脏代谢风险的DNA甲基化介导因子
为何癌症的后效在体内挥之不去
得益于治疗进步,大多数儿童癌症患者如今能够长大成人。但这些幸存者中有许多人在数十年后面对新的健康问题,包括肥胖、高血压和类糖尿病状况。本研究提出了一个紧迫的问题:童年时期接受的治疗如何在心脏和代谢系统上留下如此持久的影响?通过检测血细胞DNA上的化学标记,研究者发现线索表明既往的化疗和放疗可能以某种方式“重新编程”机体,增加长期的心脏代谢风险。
在成年后的儿童癌症幸存者中追踪隐匿风险
研究团队分析了近3,000名成年儿童癌症幸存者,这些受试者被纳入长期随访的圣裘德终生队列。作为儿童时他们接受过多种化疗以及针对脑部或躯干(胸部、腹部、盆腔)的放疗,若干年后回到队列接受详细的健康检查和血液检测。科学家将注意力集中在五类关键的心脏代谢问题上,这些问题已知会增加心脏病和过早死亡的风险:肥胖、血糖异常、高甘油三酯、高胆固醇和高血压。通过比较有无这些状况的幸存者,研究人员在基因组的数百万个位点中搜索DNA甲基化差异——这些微小的化学开关有助于控制基因的开关状态。
作为治疗记忆的DNA化学标记
在全基因组范围内,研究者发现近1,900个DNA位点的甲基化水平与至少一种心脏代谢状况相关。大多数位点仅与单一问题相关,但有一小部分似乎是连接多个问题的“枢纽”。其中五个关键位点位于两个基因附近,称为CPT1A和LMNA,与全部五类心脏代谢风险均有关联。这些基因已知影响机体如何处理脂肪以及细胞如何维持结构,提示治疗可能扰动共同的代谢和心血管通路。许多甲基化变化与普通人群中之前观察到的信号重叠,特别是与炎症相关的信号,但也有一些似乎是幸存者特有的——表明治疗留下了独特的生物学印记。
连接治疗、DNA变化与疾病
下一步是检验这些甲基化变化是否实质性地解释了治疗如何导致后期疾病,而不仅仅是伴随出现。研究者关注的是在采血后才出现或加重的心脏代谢问题,从而保留了从治疗到DNA变化再到疾病的时间顺序。通过统计学的中介分析,他们识别出24个甲基化位点,这些位点合在一起可以解释特定治疗与后期心脏代谢问题之间高达约四分之一的关联。脑部和躯干放射治疗表现出尤其显著的模式:一组甲基化位点共同解释了这些放疗对血糖异常影响的大约10–20%。其中一个突出位点位于名为ANTXR2的基因附近,似乎介导了躯干放疗对随后血糖问题约20%的影响。
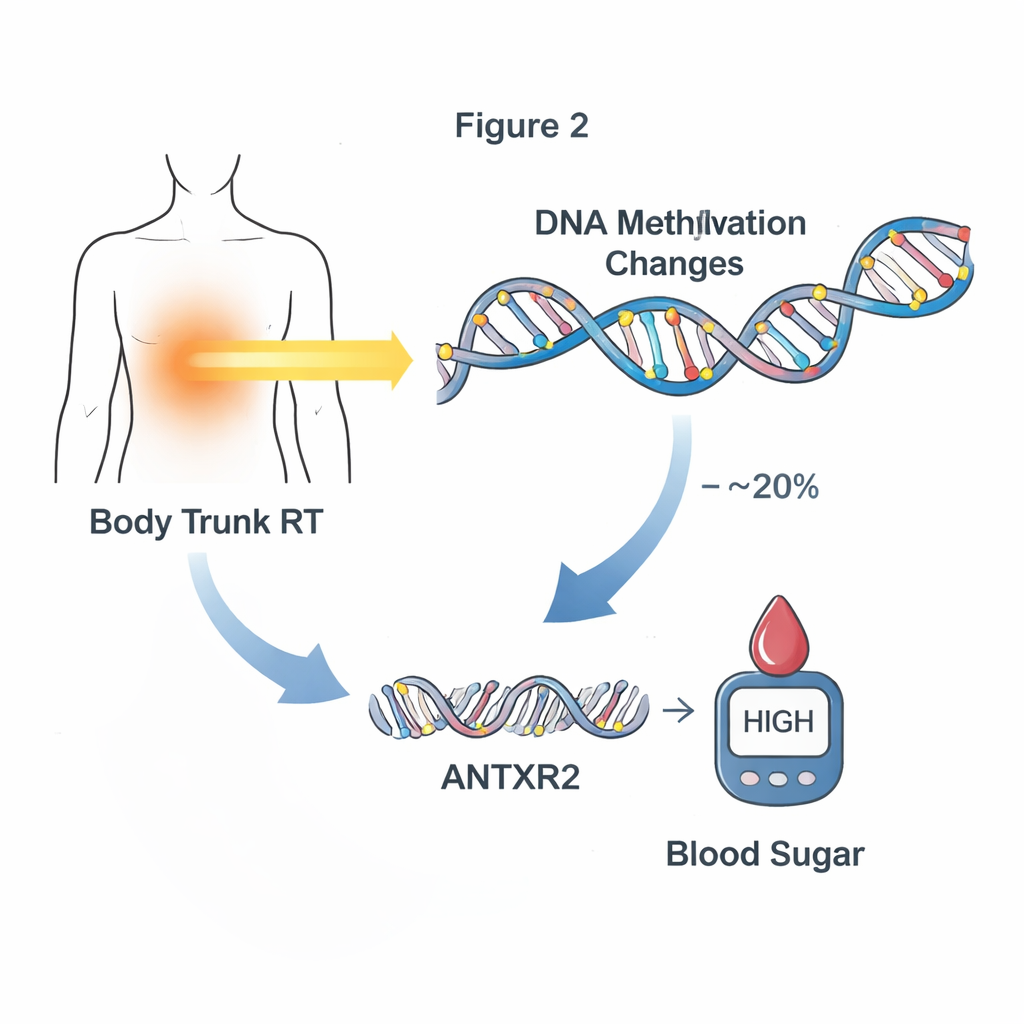
从DNA标记到基因活性
为理解这些甲基化标记如何改变生物学功能,团队在一部分同时拥有DNA和RNA血液数据的幸存者中考察了基因表达。他们发现数十个甲基化位点的甲基化水平升高或降低与近邻基因表达变化有关。其中就包括靠近ANTXR2的关键中介位点,该位点的甲基化水平与该基因的表达量强相关,尤其在接受过躯干放疗的幸存者中更为明显。ANTXR2参与调控血管及其周围组织框架——这些系统影响葡萄糖和胰岛素在体内的流动。该模式提示了一个事件链:放疗改变甲基化,进而改变基因活性,最终可能推动机体走向血糖异常。
这对幸存者与未来护理意味着什么
对非专业读者来说,关键信息是:儿童期癌症治疗不仅在当时损伤组织;它们还可能在DNA上留下长期的“笔记”,影响数十年的健康。在本研究中,部分这些“笔记”——DNA甲基化变化——有助于解释为何某些幸存者更容易出现肥胖、血脂异常或与糖尿病和心脏病相关的血糖问题。尽管这些化学标记只是完整故事的一部分,但它们最终可能作为血液生物标志物,用于识别风险最高的幸存者,并用于检验生活方式干预或新疗法是否能安全地改写部分表观遗传历史。这项工作使幸存者护理向精准医学更进一步:利用既往治疗的分子足迹来指导更早、更个性化的心血管和代谢疾病预防。
引用: Eulalio, T., Kim, Y., Meng, X. et al. Epigenome-wide analysis identifies DNA methylation mediators of treatment-related cardiometabolic risk in survivors of childhood cancer. Nat Commun 17, 1979 (2026). https://doi.org/10.1038/s41467-026-68689-6
关键词: 儿童癌症幸存者, DNA甲基化, 心脏代谢风险, 放射治疗, 表观遗传学