Clear Sky Science · zh
通过多阶段与多任务学习迭代发现高效聚合物抗生素以应对抗菌耐药性
为什么新抗生素与每个人息息相关
耐药性感染在全球范围内上升,使得熟悉的疾病变得更难,有时甚至无法治疗。该研究描述了一种快速发现不同类型抗生素的新方法:微小的合成聚合物,它们既能杀死顽固细菌,又能使像青霉素这样的旧药物重新发挥作用。该工作将先进的人工智能与化学和动物试验相结合,以探索一个通过试错法几乎不可能穷尽的巨大化学空间。
在拥挤的化学宇宙中寻找新防御者
传统抗生素通常靶向特定的细菌蛋白,而细菌可以逐步规避这些靶点。相比之下,本研究中的聚合物模仿了我们体内的防御肽,通过物理方式破坏细菌膜,更不容易产生耐药性。挑战在于可能的聚合物结构多达数万种,其行为依赖于正电荷、亲水与疏水组分之间的微妙平衡。手工测试足够多的候选物以找到既安全又有效的聚合物将耗时数年。作者构建了一个大约10万种相关聚合物的组合库,称为聚(β-氨基酯),每种设计为自组装成纳米级颗粒,能够与细菌细胞表面强烈相互作用。
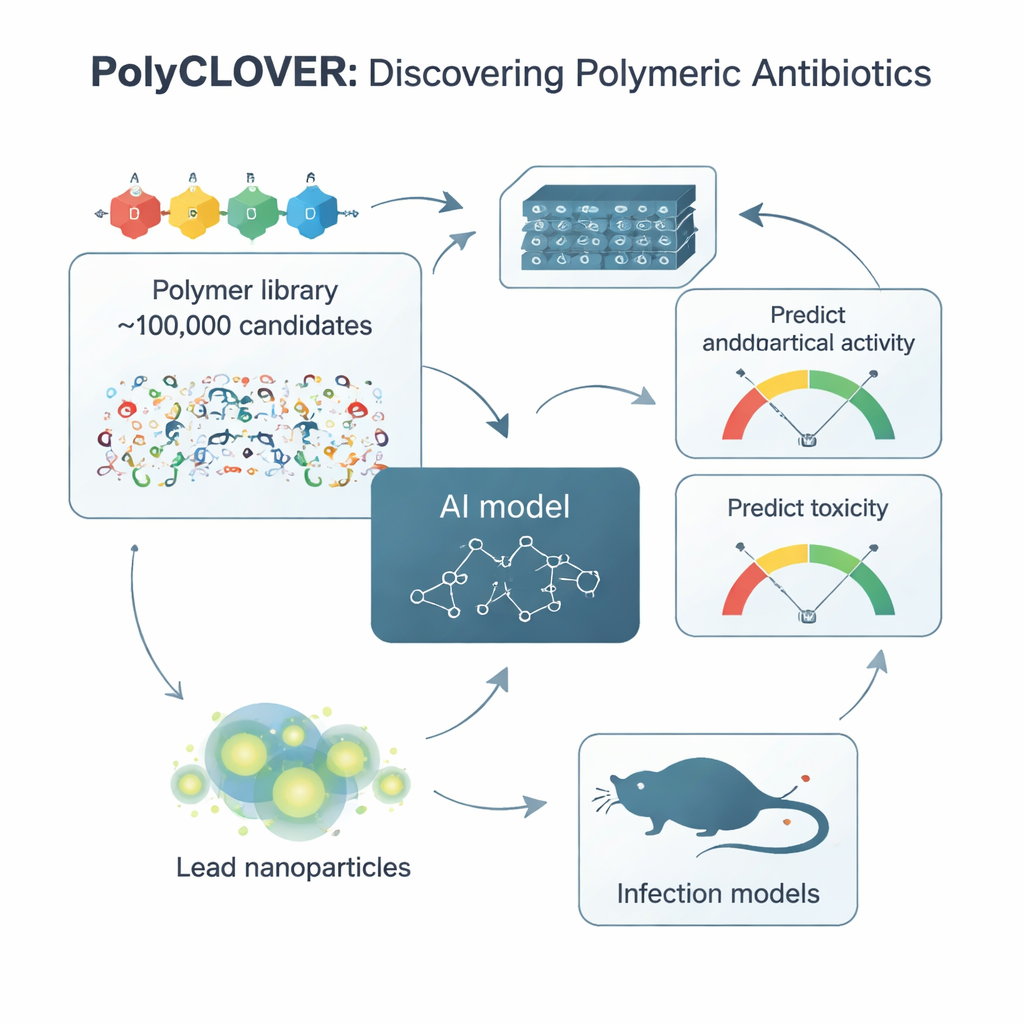
教AI读懂聚合物的“肢体语言”
为了在该库中导航,团队创建了一个名为PolyCLOVER的框架。其核心是基于图的神经网络,将每个聚合物视为相连原子的网络,使模型能够感知结构中的细微差别。由于关于哪些聚合物是优或劣抗生素的标注样本极少,研究者采用了多阶段的自监督学习策略。首先,模型在大约一百万个无标注聚合物结构上训练以捕捉通用化学模式;接着在无标注的10万成员库上进一步训练;最后在一小批已合成并测试过的220种聚合物上微调,这些聚合物同时测定了抗菌强度和对红细胞的损伤。分阶段学习显著提升了模型预测哪些新聚合物既强效又安全的能力。
让实验与算法相互学习
PolyCLOVER并不止于一轮预测。它以循环方式运行:AI建议最有前景且信息量最大的候选物,化学家以高通量方式合成并测试它们,新的结果被反馈用于改进模型。选择步骤采用“上置信界”方法,在利用(优先考虑被预测为有效的聚合物)与探索(探查模型不确定、能最大化学习的区域)之间取得平衡。经过大约四轮迭代,所建议的聚合物持续改进:它们对耐甲氧西林金黄色葡萄球菌(MRSA)的效力增强,同时对红细胞的毒性保持在可接受范围内。在仅约20天的实验内,该系统收敛到一小组表现突出的聚合物。
自组装微粒对细菌造成穿孔打击
最终的三种候选聚合物命名为H1、H2和H3,它们自发形成带正电的纳米颗粒,直径约100纳米。在体外测试中,它们杀死MRSA的效果与常规抗生素链霉素相当,但速度更快——在几分钟到几小时内将细菌数量降低数个数量级,即便在富含蛋白质的血清中也有效。电子显微镜和荧光探针显示,这些颗粒迅速附着于细菌表面并破坏膜的完整性与电位,导致细胞内容物泄漏。重要的是,当MRSA暴露于这些聚合物近一个月时,细菌几乎没有产生耐药性,这与链霉素在相同时期所需剂量显著上升形成鲜明对比。
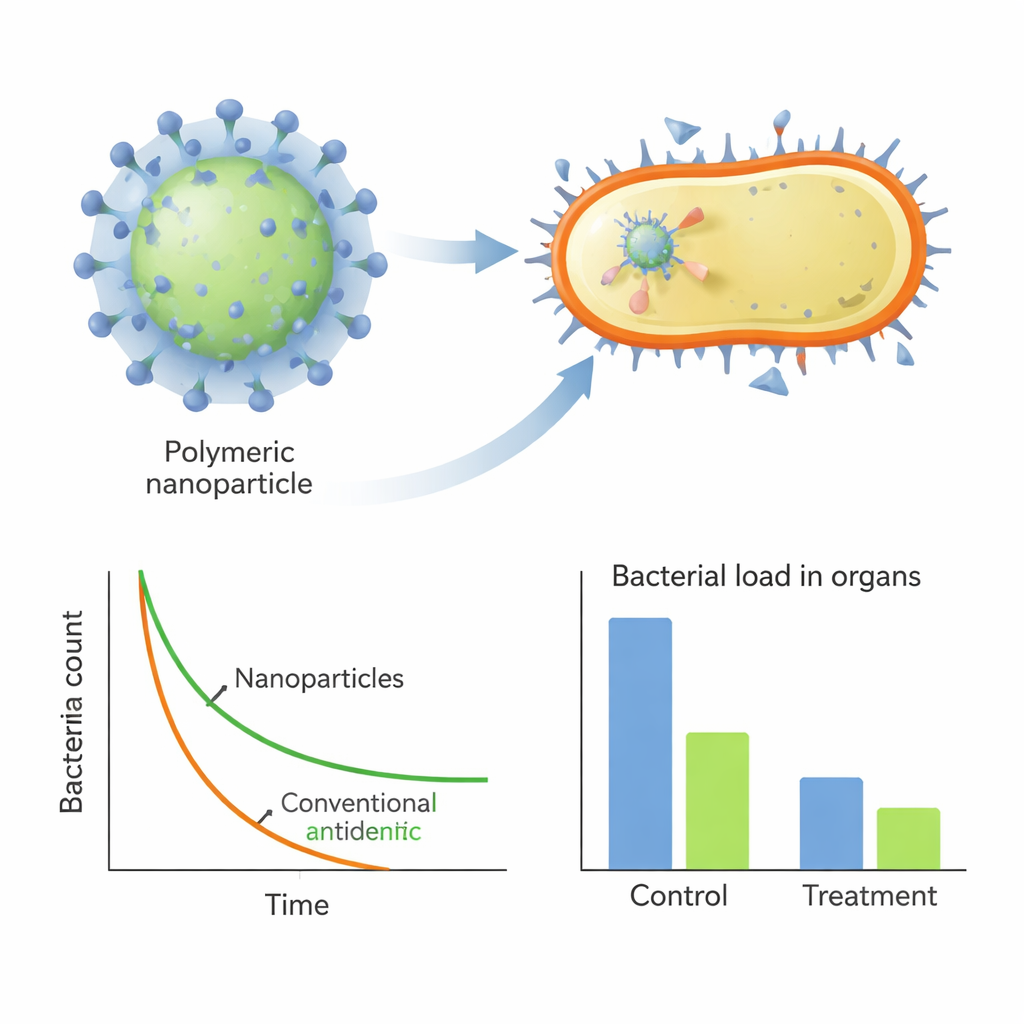
在动物感染中使旧抗生素重新发挥作用
除了单独有效外,这些纳米颗粒还能作为传统药物的强力助推器。当与对MRSA通常高度耐药的苄青霉素(penicillin G)结合时,最佳聚合物(H2)形成了将抗生素包裹在颗粒内部的纳米复合物。这些复合物在体外测试中表现出强烈的协同作用,大幅降低了抑制MRSA所需的苄青霉素剂量。在小鼠的肺部感染和严重腹腔感染模型中,使用这些领先聚合物进行治疗——无论单独使用还是与苄青霉素联合——都显著降低了器官内的细菌负荷、降低了血液中的炎性信号并减少了组织损伤,且未见明显毒性。
更智能地发现抗生素的新剧本
对非专业读者来说,关键要点是PolyCLOVER展示了AI与自动化实验如何协作,以比以往更快地发现全新类型的抗生素。该方法不再仅依赖偶然和缓慢的筛选,而是从每一批结果中学习,聚焦那些既能攻击耐药细菌又能更有效携带传统抗生素的聚合物。尽管在这些材料进入临床之前仍需进一步工作,这项研究为补充我们日益枯竭的抗耐药感染武器库提供了有希望的途径,并提出了一种可推广的策略用于设计其他多种智能生物材料。
引用: Wu, Y., Wang, C., Shen, X. et al. Iterative discovery of potent polymeric antibiotics via multi-stage and multi-task learning against antimicrobial resistance. Nat Commun 17, 1878 (2026). https://doi.org/10.1038/s41467-026-68682-z
关键词: 抗菌耐药性, 聚合物抗生素, 纳米颗粒, 机器学习, 耐药细菌