Clear Sky Science · zh
脂肪肽类抗生素科利斯汀与turnercyclamycin对膜脂的差异性破坏
这对未来抗生素为何重要
预计到本世纪中叶,耐药性感染每年将导致数千万人的死亡,其中一些最致命的病原体是已经能抵御多种抗生素的革兰氏阴性菌。科利斯汀是为数不多仍能治疗这些感染的药物之一,但对患者副作用大,且细菌对其的抗性日益增加。本研究解析了科利斯汀与一种新发现的天然抗生素家族turnercyclamycins的作用机制,揭示了微小的化学差异如何产生截然不同的致菌方式——并可能带来更安全的药物。
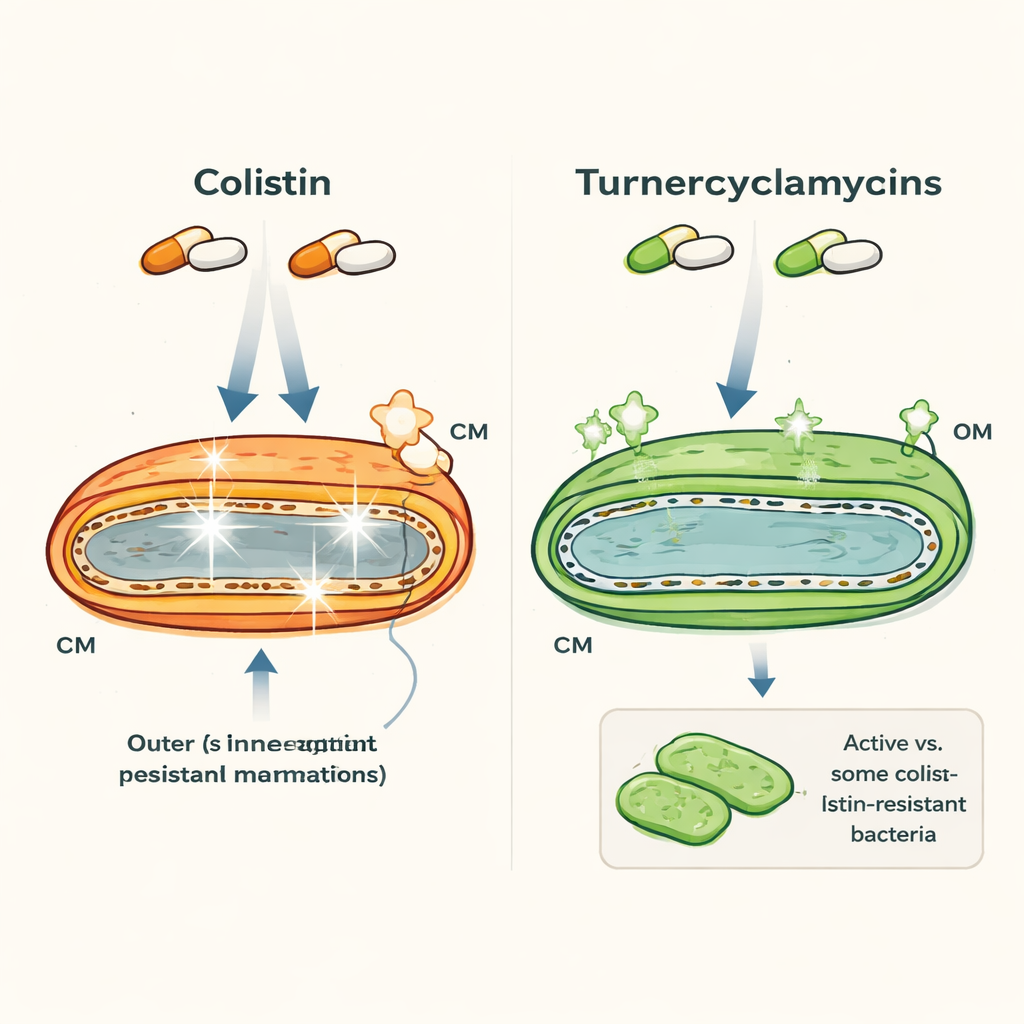
外观相似却行为迥异的两种药物
科利斯汀和turnercyclamycins都属于脂肽类分子——将脂肪尾与肽环结合的化合物——两者均针对革兰氏阴性菌,如大肠埃希氏菌(Escherichia coli)和不动杆菌属(Acinetobacter)。乍看之下它们相似,但性质却大相径庭。科利斯汀作为最后手段药物起效迅速,但会损伤人类肾脏和神经,且细菌日益携带如mcr-1之类的抗性基因。turnercyclamycins来自与船蛀虫共生的细菌,能杀死许多相同的病原体,包括某些对科利斯汀耐药的菌株,但在实验室测试中毒性远低。奇特的是,仅因脂肪尾部的一点延伸而有两种版本,已显示出不同的抗性谱,暗示极其细微的结构特征就能产生重要影响。
科利斯汀如何打穿孔洞而turnercyclamycins则从容以待
作者使用荧光染料、时间-杀菌实验和电子显微镜,随着时间推移观察这些药物对细菌膜的影响。科利斯汀迅速使外膜和细胞质膜都变得渗漏,导致数小时内迅速死亡。相比之下,turnercyclamycins杀灭更慢——需要6到10小时才能完全清除培养物——且主要扰动外膜。针对内膜破损会发光的染料对科利斯汀显示强烈信号,而对turnercyclamycins仅显示温和且延迟的信号,高分辨率图像也证实即便细胞濒死,内膜仍缺乏明显可见损伤。这表明turnercyclamycins并非通过许多膜靶向抗生素常见的“孔形成”途径致死。
作为隐藏控制钮的脂质构件
两类药物的活性最终都依赖于一种称为脂多糖(LPS)的细菌组分,LPS在内膜中合成并通常被输送到外表面。当研究者破坏LPS生物合成的早期步骤时,科利斯汀和turnercyclamycins的活性都消失;但当他们阻断将LPS向外运输的机械时,药物仍然有效。这意味着LPS的合成前体是必需的,但其最终定位并不关键。在直接测量结合时出现关键差异:科利斯汀能以微摩尔亲和力黏附纯化的LPS,而turnercyclamycins未显示可测的结合。相反,turnercyclamycins受其他膜脂质影响显著。某些磷脂,尤其是磷脂酰甘油,可削弱或调节其活性,且这些药物容易被外膜囊泡(细菌释放的微小脂质泡)捕获。
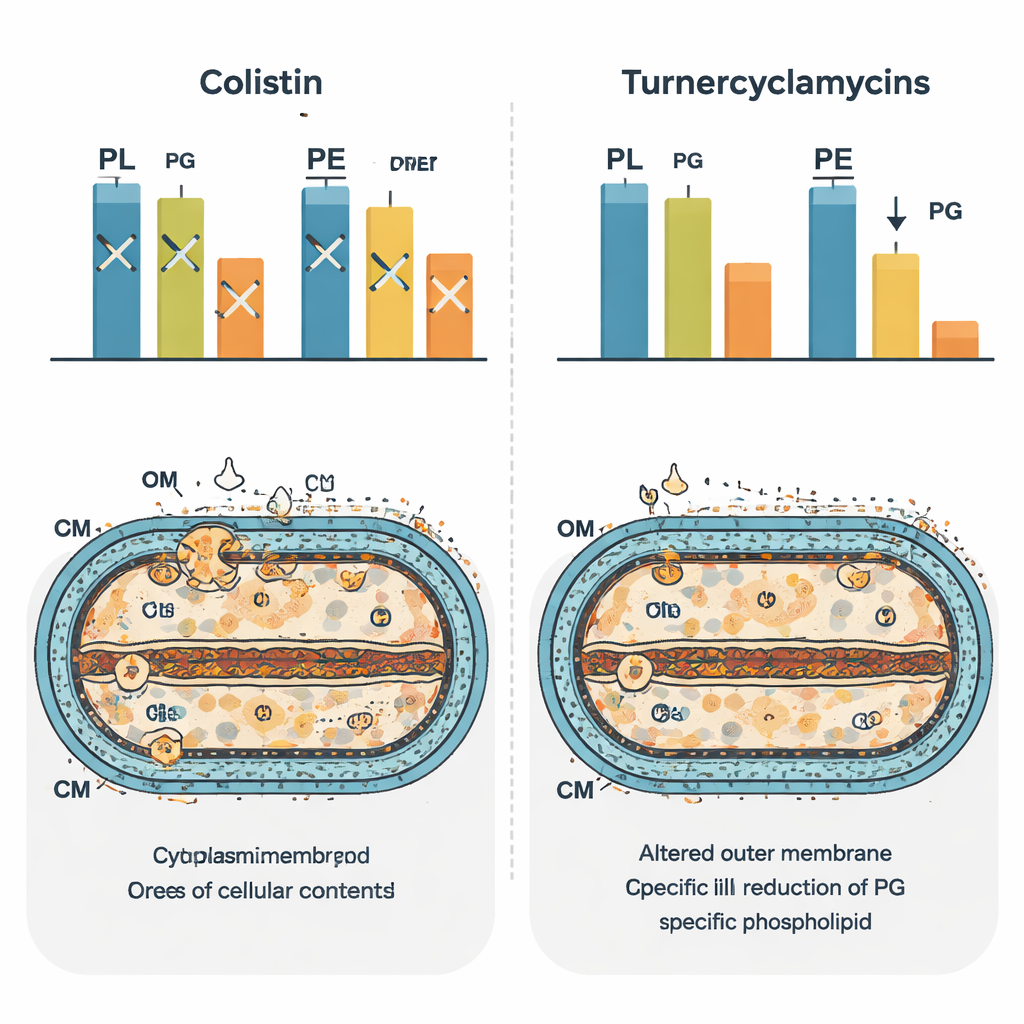
改写细菌的脂质景观
为观察对细胞更广泛的影响,团队使用基于质谱的“磷脂质组学”对处理后数百种脂质进行目录化。科利斯汀产生了一种独特的变化模式,反映其对膜稳态的广泛破坏。turnercyclamycins则生成了不同的指纹,极像缺失一种名为MlaA的脂质转运蛋白的细菌。在这些细胞中,某些二酰基脂质被耗竭,而单酰基形式增加,表明磷脂在膜间的正常循环和重塑被打乱。值得注意的是,turnercyclamycin处理细胞中磷脂酰甘油的水平下降,进一步支持该脂质与其效力直接相关的观点。作者提出,turnercyclamycins可能作为分子模仿物,卡住连接脂肪酸、LPS和磷脂酰甘油合成或转运的路径。
对设计更佳药物的启示
简而言之,研究表明科利斯汀通过紧密结合LPS、迅速撕裂革兰氏阴性细菌的两层保护膜来致死,而turnercyclamycins更像是破坏细胞脂质供应链的破坏者。它们进入外膜,逐步扰乱特定脂质的合成与回收,最终导致细胞包膜失效——而不严重攻击内膜。由于这种较温和、更有针对性的机制与较低的毒性和不同的抗性谱相关,理解它为设计下一代脂肽类抗生素提供了路线图。通过微调诸如脂肪尾的长度与饱和度等特征,化学家可能能合成出对人体组织更为友好、对科利斯汀耐药株仍具活性并能在与耐药细菌的军备竞赛中保持领先的药物。
引用: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
关键词: 抗生素耐药性, 革兰氏阴性菌, 科利斯汀, 脂肽类抗生素, 膜脂质