Clear Sky Science · zh
结核菌素皮肤试验的演变揭示了可泛化的Mtb反应性T细胞元克隆
这对结核病为何重要
大多数被结核分枝杆菌(TB)感染的人并不会发病,但结核仍是主要的传染性致死原因之一。临床上知道某些免疫细胞——称为T细胞——有助于控制结核分枝杆菌(Mtb),但究竟哪些T细胞最关键一直难以确定。该研究将熟悉的结核菌素皮肤试验(TST,即皮肤上出现的小丘疹)作为观察人体T细胞实时应答Mtb的窗口,并引入了一种新方法,用以在不同个体间发现共享的、针对Mtb的T细胞模式。
从简单皮试到强大的免疫模型
结核菌素皮肤试验长期在门诊作为是否既往暴露于结核的二元判读:将纯化的结核蛋白注入皮下,然后在两到三天后测量隆起丘疹的大小。作者把这一常规检测转为研究工具:在注射部位于第2天和第7天取微小活检,并与生理盐水对照注射进行比较。他们测量了哪些基因被激活,并且关键地对T细胞受体(TCR)——赋予每个T细胞识别特定靶标的分子“身份证”——进行测序。这样他们得以追踪局部免疫反应如何随时间成熟,而不仅仅记录丘疹的大小。
早期人群,后期专家 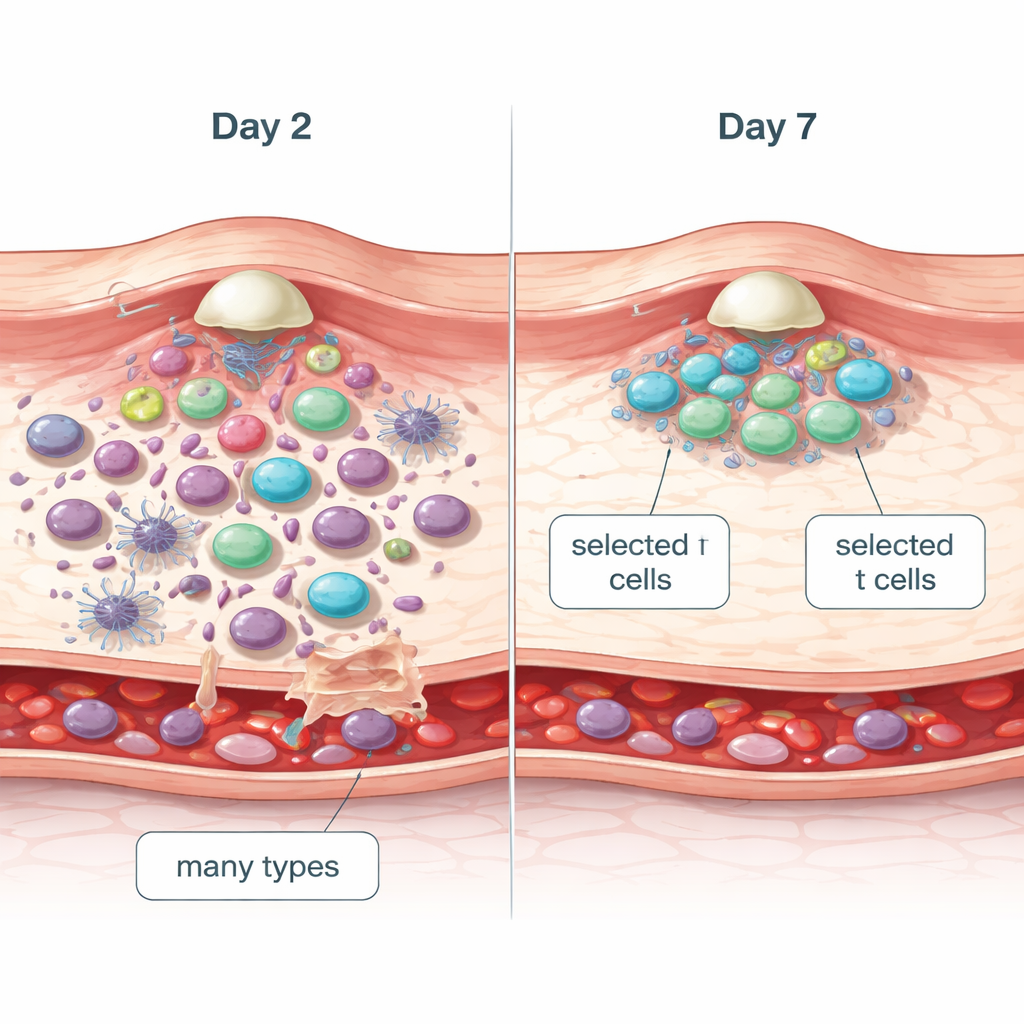
Figure 1.

基因表达数据显示,第2天时皮肤已经呈炎性并充斥多种免疫细胞,但几乎没有细胞分裂的迹象。到第7天,整体炎性信号开始平息,而与细胞周期和增殖相关的基因显著上调,特别是在CD4 T细胞中。TCR测序证实了这一转变:第2天时检测到的T细胞群体多样性高,对任何特定克隆的偏倚很小,表明来自血液的招募较为非选择性。到第7天,一小部分T细胞克隆显著扩增——呈现“寡克隆”模式——表明识别结核抗原的T细胞在注射部位发生了选择性增殖。
证明这些T细胞确实识别结核
为验证这些扩增的克隆确实对结核有反应,研究团队将皮肤的TCR序列与大型公开数据库中具有已知特异性的TCR进行比对,并与通过在体外用结核蛋白刺激志愿者血细胞而培养得到的T细胞进行比较。第7天的皮肤样本中显著富集对结核有反应的TCR,同时在已知针对如巨细胞病毒(CMV)和爱泼斯坦-巴尔病毒(EBV)等无关病毒的TCR中呈耗竭。重要的是,每位受试者皮试中发现的许多结核反应性TCR都是“私有”序列——个体专有、不与他人共享——这也解释了为何仅在血液中简单计数结核反应性T细胞难以预测谁受保护或有风险。
用Metaclonotypist寻找共享的免疫模式 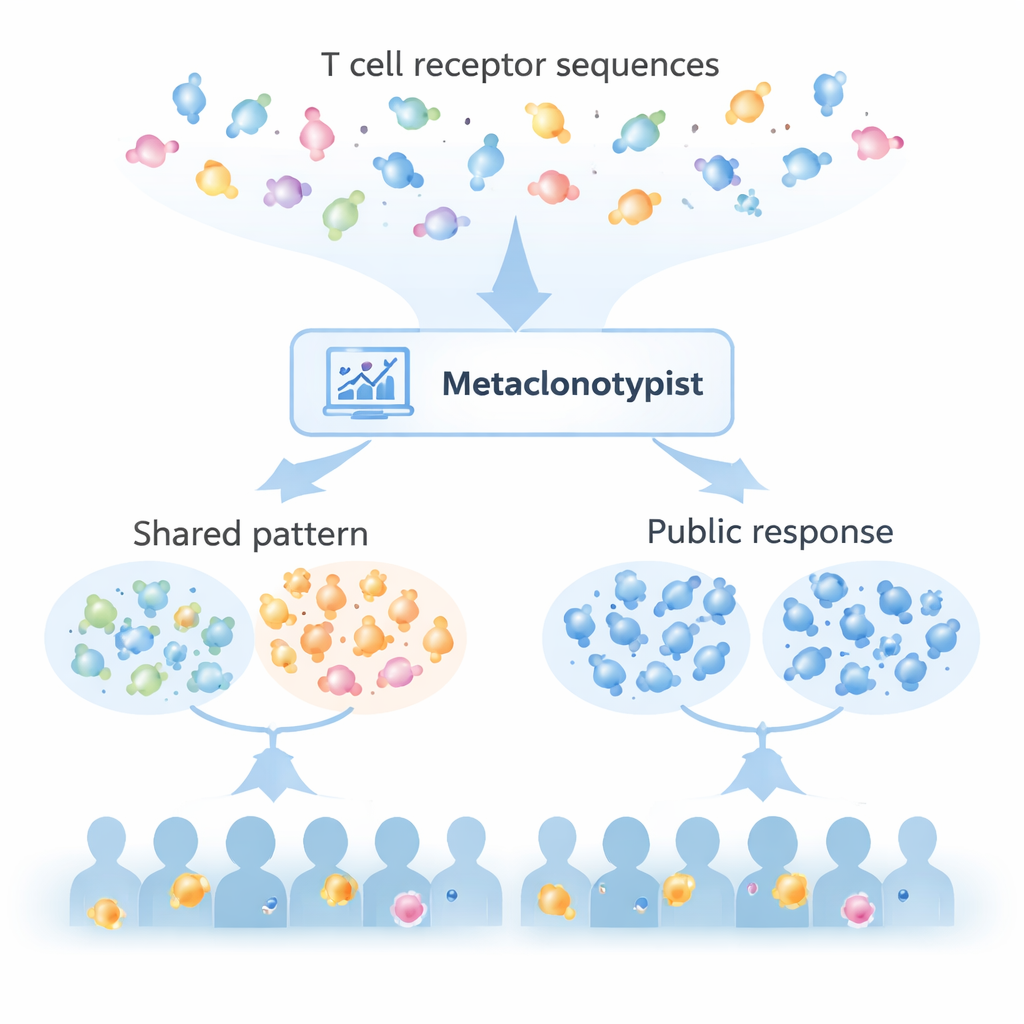
Figure 2.

尽管存在个体差异,研究者推测不同个体的TCR可能仍会趋同于相同的结核肽靶点,即便确切的受体序列略有不同。他们构建了一个计算流水线Metaclonotypist,将相似的TCR分组为“元克隆”(metaclones)——预测识别由特定HLA分子呈递的同一段结核蛋白的簇。通过分析来自150多名参与者的第7天皮肤TCR,他们发现了180个此类元克隆,其中绝大多数与向CD4 T细胞呈递抗原的II类HLA分子相关。大约只有3%的独特TCR序列落入这些公共元克隆中,但超过95%的参与者至少贡献了其中一个,而仅约10个高度“公共”的元克隆已足以在整个队列中检测到结核反应性T细胞。
跨组织与疾病的共享特征
为检验这些元克隆是否确实标志结核特异性反应,而非仅标识任何炎症,作者在独立数据集中进行了查证。相同的元克隆在从血液培养得到的结核反应性T细胞中富集,在结核患者的血液和肺组织中相比癌症或COVID-19患者富集,并在肺病灶部位相比患者自身血液中富集。相比之下,第7天皮试中全部扩增的TCR集合富集信号较弱,强调了元克隆捕捉了最结核特异且广泛共享的反应部分。这表明皮肤试验可作为研究人类临床相关结核免疫的实用、标准化“挑战”模型。
这对患者和疫苗的意义
对非专业读者而言,关键结论是熟悉的结核皮试在皮下藏着一个丰富且演化中的故事。早期的丘疹反映的是免疫细胞的广泛涌入,但到第7天,注射部位被一小群聚焦的CD4 T细胞主导,这些细胞正在主动识别结核蛋白。多数应答细胞在个体间是独特的,然而Metaclonotypist方法揭示出少量反复出现的共享T细胞模式——元克隆——在许多人和病变肺中反复出现。这些公共特征可能成为未来血液检测用于分层结核风险、追踪治疗或评估疫苗的基础,并可能指向能诱发最具保护性的T细胞反应的特定结核肽片段。
引用: Turner, C.T., Tiffeau-Mayer, A., Rosenheim, J. et al. Evolution of the tuberculin skin test reveals generalisable Mtb-reactive T cell metaclones. Nat Commun 17, 1900 (2026). https://doi.org/10.1038/s41467-026-68678-9
关键词: 结核病, T细胞, 结核菌素皮肤试验, T细胞受体测序, 免疫生物标志物