Clear Sky Science · zh
促蜕膜化赋能的细胞外基质水凝胶整合持续释放Tβ4驱动宫腔粘连子宫内膜再生
为何无疤痕修复子宫至关重要
对许多女性而言,子宫内膜的损伤可能在不知不觉中剥夺生育能力。宫腔粘连——在子宫腔内形成的瘢痕组织带——可导致痛经、反复流产和受孕困难。现有的常规治疗多为手术切除瘢痕,但组织常会再次形成瘢痕。本研究提出了一种生物工程“智能”凝胶,其目标不仅是去除损伤,更要教会子宫像早期妊娠那样自我修复——再生健康的内膜,而不是继续沉积瘢痕组织。
修复何以出错
宫腔粘连产生于子宫内膜在受伤后不是重建柔软且富血管的表面,而是形成致密纤维性瘢痕。损伤后,剧烈的炎症反应通常有助于清除碎屑;在这种疾病中,这一反应却陷入过度运作:免疫细胞释放强烈的炎性信号,特定的细胞死亡通路被触发,且一个关键的瘢痕化通路TGF‑β/Smad3持续被激活。胶原及其它基质蛋白堆积,使组织僵硬,阻断新血管的形成,并抑制驻留的干细胞和祖细胞的活性。结果形成一种不利环境,胚胎无法正常着床或发育。
借用早期妊娠的修复程序 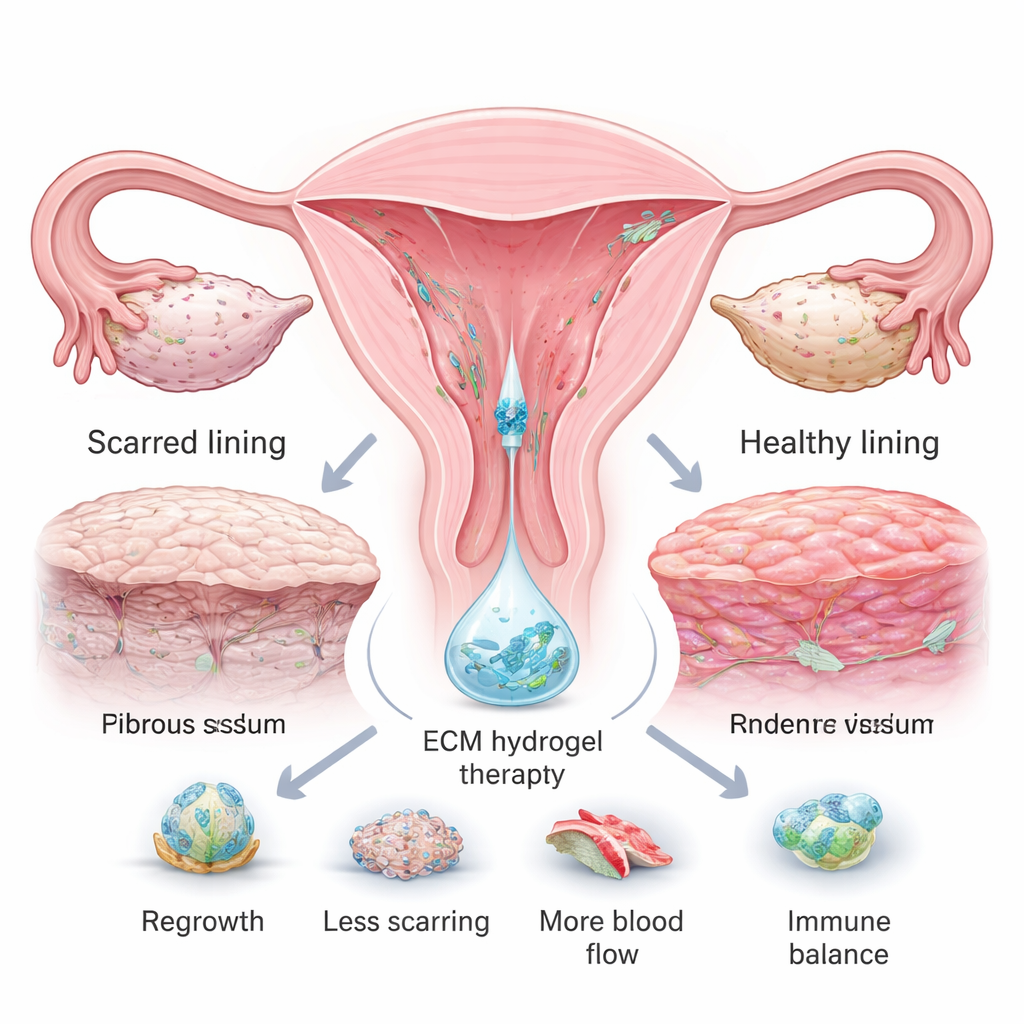
Figure 1.

作者们探问是否可以复制并作为治疗重复利用子宫在早期妊娠中展现出的“最佳”修复模式。在这一自然过程——称为蜕膜化——中,内膜增厚、血管丰富,并且免疫环境由攻击性转向有利于平静修复。研究团队在小鼠体内诱导出类似蜕膜化的状态,然后去除细胞,仅保留称为细胞外基质的蛋白支架。这种蜕膜化基质(DEndo‑UdECM)保留了原始组织的三维结构,并富含与伤口愈合、血管生成、干细胞支持及自然抑制瘢痕信号相关的蛋白质。与简单凝胶不同,该基质更像是子宫促再生的保留蓝图。
双重水凝胶:加速器与刹车
即便是智能支架,在严重病变中也必须应对强烈的瘢痕化驱动力。为此,研究者加入了第二成分:由可生物降解聚合物(PLGA)制成、负载胸腺素β4的小微球。胸腺素β4是一种已知能促进血管生长并抑制纤维化的小肽。将这些微球混入液化的蜕膜化基质中,形成一种复合水凝胶,可通过细针注射并在体温下迅速凝固。体外实验显示,蜕膜基质显著促进子宫内膜细胞的增殖和迁移,并促进毛细血管样网络的形成,而胸腺素β4则特异性抑制与纤维化相关的蛋白。两者协同,支架充当再生的加速器,缓释药物作为长期抑制瘢痕的刹车。
从瘢痕子宫到健康妊娠 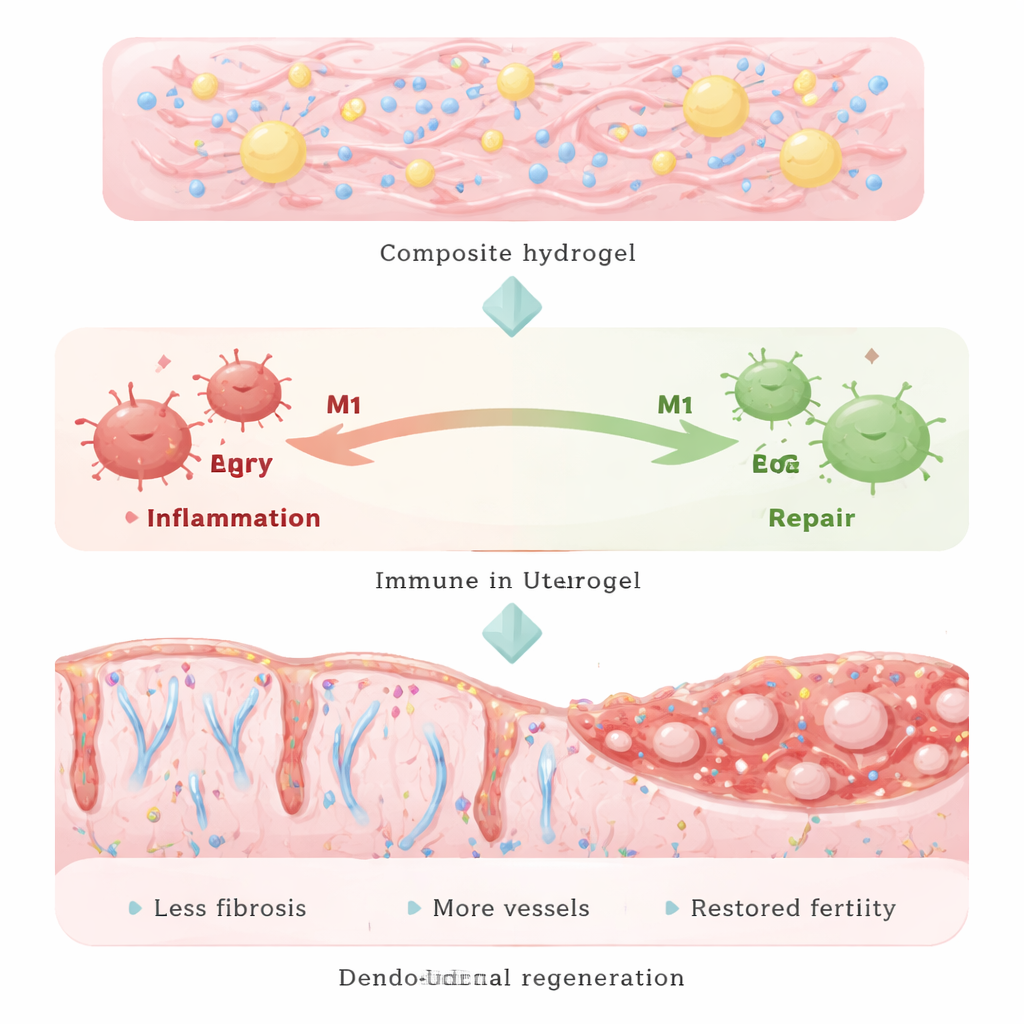
Figure 2.

随后团队在一个严格的小鼠模型中测试,该模型通过乙醇严重破坏子宫内膜,模拟重度宫腔粘连。向受伤子宫单次注射该复合水凝胶,两周内产生了显著变化。与未处理或部分处理的动物相比,接受完整凝胶的小鼠表现出更厚、更有序的子宫内膜,许多腺体得到恢复,含胶原的瘢痕组织明显减少。有害炎症及TGF‑β/Smad3瘢痕通路的标志物显著降低。同时,巨噬细胞从破坏性的“M1”状态转向有助修复的“M2”状态,干细胞活性、新血管生成及有序细胞分裂的信号均恢复。关键是,这些小鼠配种后,着床率和窝产量几乎恢复正常,后代的生长发育与来自健康母鼠的后代相当。
更智能组织修复的蓝图
对非专业读者而言,核心信息是研究者构建了一种帮助子宫“记起”正常修复方式的凝胶。通过复制早期妊娠的基质并结合缓释的抗瘢痕因子,他们创造了一个能平息失控炎症、阻断纤维化通路并鼓励真实组织再生而非零散修补的微环境。在重度子宫瘢痕的小鼠中,该方法不仅改善了组织外观——更恢复了承载健康胎儿的能力。尽管在用于人类前仍需更多工作,这项研究展示了一个更广泛的理念:仔细模拟人体自身最佳的修复程序,或能逆转顽固瘢痕性疾病并恢复器官功能。
引用: Liang, Y., Yu, Z., Du, S. et al. Decidualization-empowered ECM hydrogel integrating sustained Tβ4 release drives endometrial regeneration in intrauterine adhesions. Nat Commun 17, 1910 (2026). https://doi.org/10.1038/s41467-026-68677-w
关键词: 宫腔粘连, 子宫内膜再生, 水凝胶疗法, 细胞外基质, 女性不孕