Clear Sky Science · zh
sortilin对甲状腺球蛋白的分子识别
甲状腺细胞如何决定何时释放激素
甲状腺激素帮助设定我们的代谢“恒温器”,影响从心率到体温的诸多生理指标。这些激素在一个巨大的蛋白质——甲状腺球蛋白(thyroglobulin)内合成并储存。本文研究揭示了另一种蛋白质sortilin如何帮助甲状腺细胞选择应从细胞表面回收哪种形式的甲状腺球蛋白,以便将激素释放到血液中——这一决策最终影响我们体内可用甲状腺激素的量。
等待加工的储存蛋白
甲状腺球蛋白是一种巨大、Y形的蛋白,由甲状腺细胞合成并分泌到被称为胶质的凝胶样池中。在那里,它既充当原料又充当激素的仓库:甲状腺球蛋白内部的特定氨基酸残基会被碘化成为甲状腺激素,这些激素仍嵌在较大的蛋白中。要真正释放这些激素,甲状腺球蛋白必须被细胞回收,进入被称为溶酶体的降解与回收室内切割,其激素片段随后被转运到血液中。
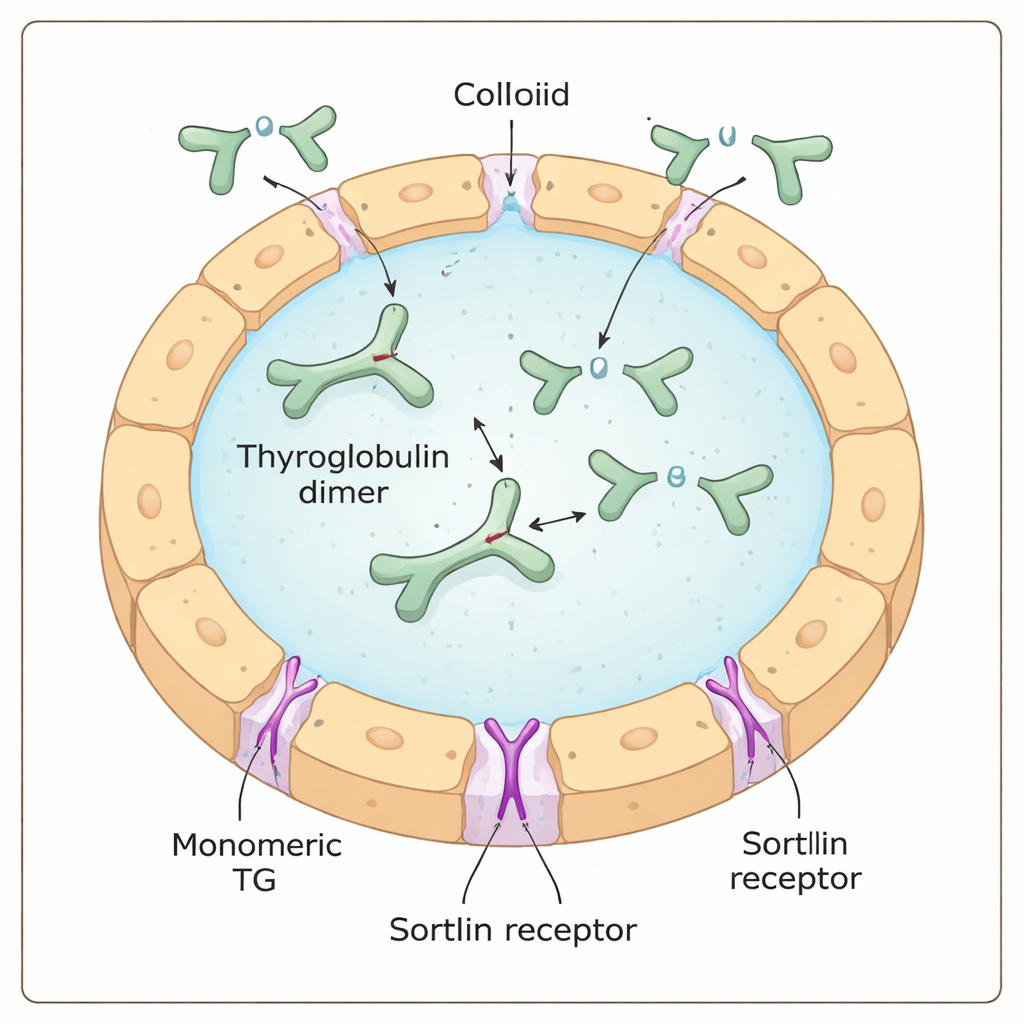
具有隐性偏好的细胞门卫
受体蛋白sortilin被提出为在细胞表面结合甲状腺球蛋白并引导其内吞的“门卫”之一。早期工作暗示sortilin偏好高度碘化的甲状腺球蛋白,提示该受体可能直接感知碘含量。作者通过生化测试、单分子质量测量和基于细胞的摄取实验相结合,发现相反的结论:sortilin明显偏好单一单元(单体)形式的甲状腺球蛋白,而非其更常见的配对二聚体形式。样品中单体比例越高,与sortilin形成复合物并被甲状腺细胞内化的效率越高,且这一现象与所携带的碘含量无关。
放大接触点看细节
为了在原子水平上理解这种偏好,研究团队使用了高分辨率低温电子显微镜(cryo-EM)和交联质谱技术。这些方法显示,sortilin识别单体甲状腺球蛋白在C端(一个末端)的一段短而松散的尾部。该尾部伸入sortilin中心的一个十叶片螺旋状腔体,并在内部两个小的“热点”位置停靠。显著的是,在二聚体形式中,尾部周围的部分区域被埋藏,sortilin无法接触,从而解释了二聚体为何不易成为结合伙伴。数据表明,细胞外的修剪或对甲状腺球蛋白的天然降解可帮助将二聚体转化为sortilin能够识别的单体。
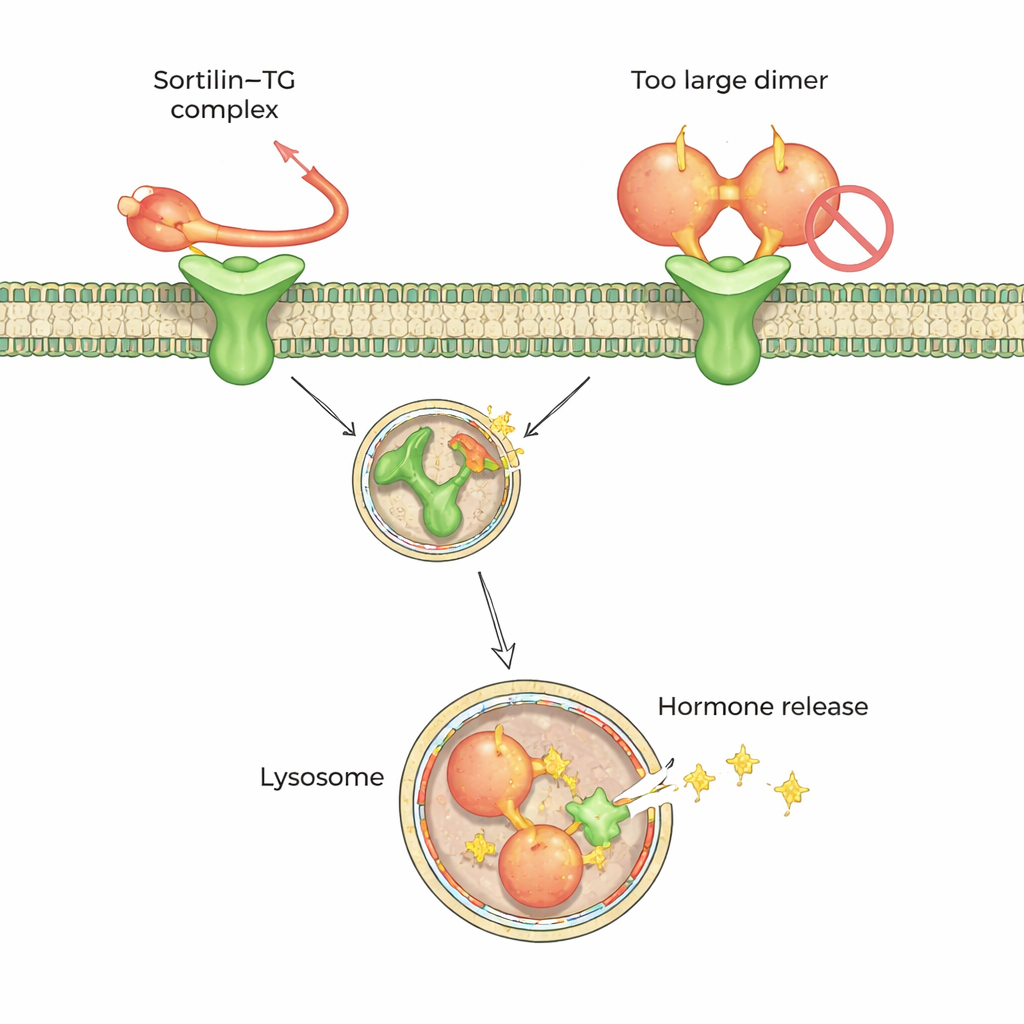
许多货物蛋白共享的停靠编码
sortilin并非仅限于甲状腺功能;它参与体内许多分子的运输,包括与心脏病和脑部疾病相关的因子。研究者将他们的结构学工作与AlphaFold和AlphaPulldown等先进结构预测工具结合,比较了数十种已知sortilin配体如何可能与其螺旋腔结合。他们发现了一个反复出现的模式:许多货物蛋白呈现大约二十个氨基酸的无序肽段,能够适配与甲状腺球蛋白尾部相同的口袋,这些肽段有时与已知脑肽神经肽素(neurotensin)方向一致,有时则相反。尽管方向相反,这些肽段具有相似特征——一端带有酸性或负电荷基团,另一端有体积较大的芳香族残基,中间则是柔性、常富含脯氨酸运动的区段。
为何碘比形状不那么重要
由于sortilin与甲状腺球蛋白的关键接触是通过这一柔性尾部,作者测试了在尾部将一个形成激素的酪氨酸再碘化是否会改变结合。结果并未改变:携带已形成甲状腺激素的合成肽与未修饰版本的行为几乎相同。建模显示,碘化的芳香环伸向溶剂而未形成新的紧密接触。结合摄取实验,这些结果支持一种修正的观点:sortilin并不会“计数”甲状腺球蛋白上的碘原子;相反,它感知的是蛋白是否被松动或部分降解,从而以适当方式暴露出单体形式和尾部。
这对甲状腺健康意味着什么
对非专业读者而言,核心信息是甲状腺激素释放更多受蛋白形状与柔性的机械性检查所控制,而非内置的碘传感器。sortilin像细胞表面的扫描器,寻找被松动或修剪成单体的甲状腺球蛋白分子,然后将它们拉入细胞以完成最终的激素释放与碘回收。这项工作澄清了甲状腺激素生物学中的关键步骤,并提示正在为其他疾病探索的sortilin抑制药物,可能通过干扰这一识别步骤而无意中改变甲状腺激素的处理。
引用: Boniardi, I., Tanzi, G., Di Ianni, A. et al. Molecular recognition of thyroglobulin by sortilin. Nat Commun 17, 2004 (2026). https://doi.org/10.1038/s41467-026-68658-z
关键词: 甲状腺激素, 甲状腺球蛋白, sortilin, 蛋白质运输, 内吞作用