Clear Sky Science · zh
Cas12a 的桥螺旋是 R-环形成和 RuvC 激活的变构调节器
这对基因编辑为何重要
许多强大的基因编辑工具——包括用于新兴疗法和快速诊断测试的那些工具——都依赖于能够在选定位点切割 DNA 的 CRISPR 蛋白。但如果这些分子剪刀切错了位置,就可能造成有害的副作用。这项研究剖析了 Cas12a 编辑器内部的一个微小可动部件,称为桥螺旋,展示了其构象变化如何像内部安全开关一样,将正确的靶标识别与 DNA 切割联结起来。理解这一开关为工程化更精确、更安全的 CRISPR 工具提供了路线图,适用于医学和生物技术领域。
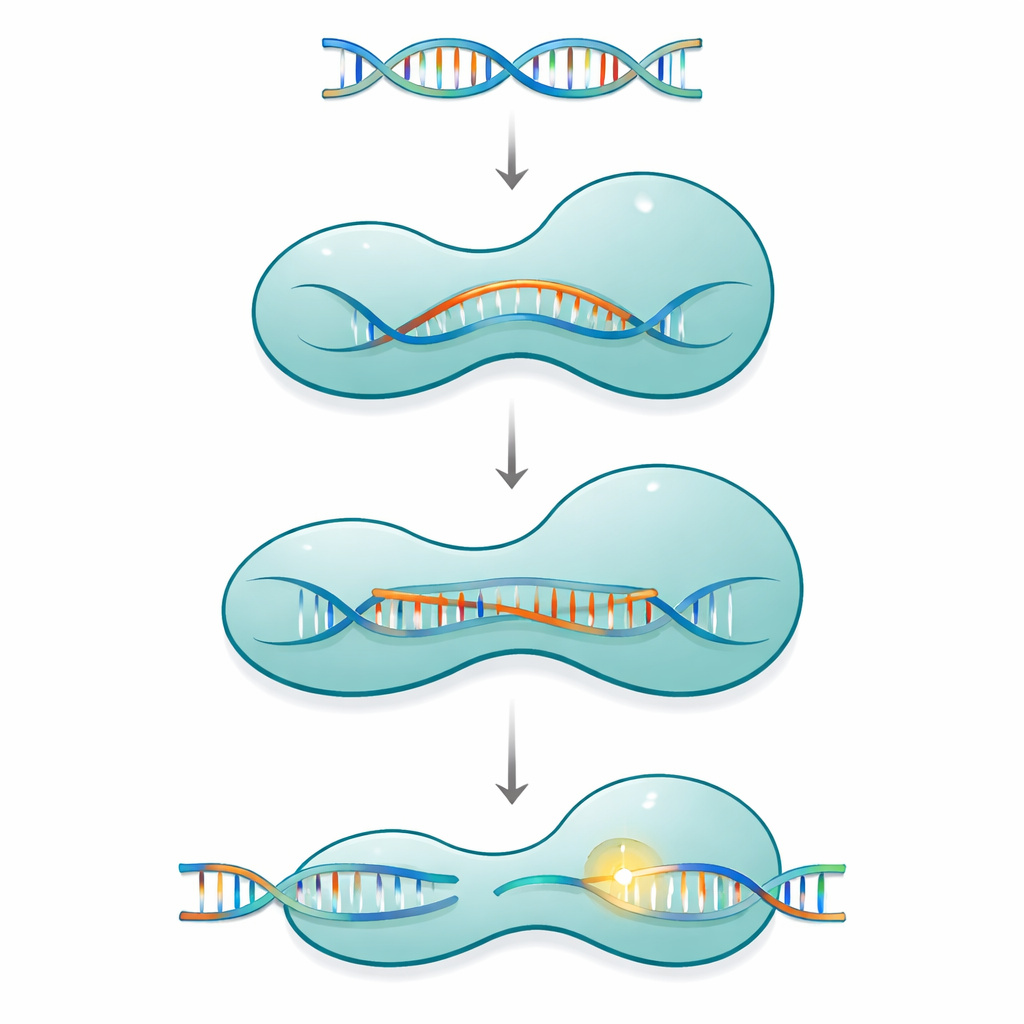
带有可动部件的分子夹钳
Cas12a 属于一类单蛋白 CRISPR 系统,这些系统使用短的导引 RNA 来识别并切割病毒或细胞基因组中匹配的 DNA。该蛋白呈两臂夹钳状:一侧负责序列识别,另一侧包含化学切割机构。这两半由一段细长的带正电的结构连接,称为桥螺旋。当 Cas12a 与导引 RNA 结合并随后结合其 DNA 靶标时,这个蛋白并不是一把僵硬的工具。相反,它经历一系列大到小的构象变化,逐步围拢在一个不断增长的 RNA–DNA 杂合体(称为 R-环)周围,只有在形成足够长的正确碱基配对后,切割位点才会完全激活。
探测内置的安全开关
研究者聚焦于来自细菌 Francisella novicida 的 Cas12a,以及一个先前设计的变体,其中桥螺旋上的两个氨基酸被替换为脯氨酸——这类替换已知会使螺旋段变僵或中断。该变体称为 FnoCas12aKD2P,相比天然蛋白它对 DNA 的切割更具选择性但更慢。通过冷冻电子显微镜,他们捕获了该变体与其导引 RNA 及一段靶 DNA 结合时的五个不同结构快照。这些快照显示了蛋白在激活途径上的不同阶段,从早期的初始 DNA 识别,到后期形成部分 RNA–DNA 杂合但尚未达到完全切割准备的状态。
构象变化如何驱动准确切割
将该变体与先前测定的正常 Cas12a 结构比较,揭示了清晰的模式。在天然蛋白中,桥螺旋的一段由松散的环状转变为更长的直螺旋,并向增长中的 RNA–DNA 杂合体弯曲,与之紧密接触。与此同时,切割结构域中相邻的一段螺旋松弛,而一个通常阻挡活性位点的小区域称为“盖板”的部分,从环状转为螺旋并翻转打开。协同的这些动作打开了一个口袋,使单股 DNA 可以进入并被切割。在含脯氨酸的变体中,桥螺旋无法完全完成这种环到螺旋的转变或正确弯曲。因此,RNA–DNA 杂合体保持扭曲并且距离较远,盖板仍处于闭合的环状状态,复合体很少达到完全预催化的构象。这一机械瓶颈减慢了对靶标的切割,并且更难让不匹配的 DNA 通过内部检查点。
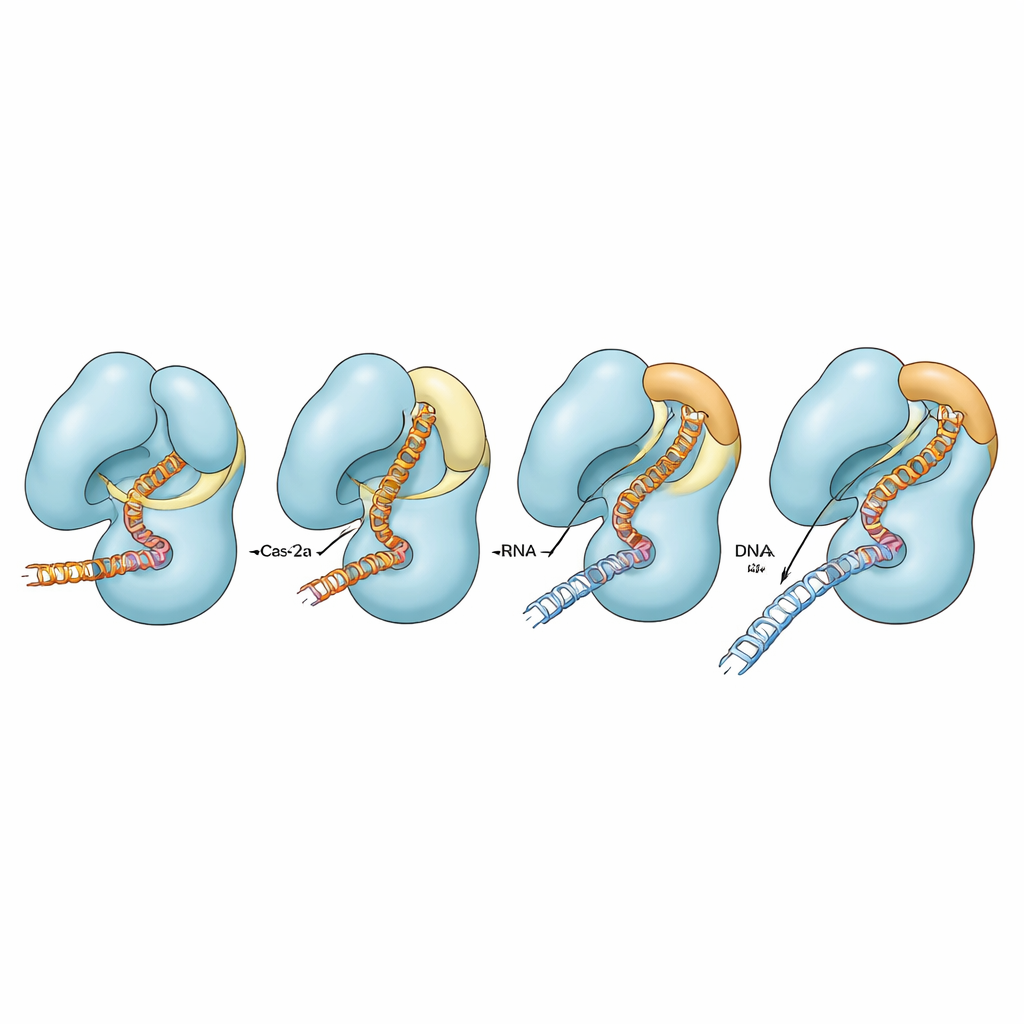
通过调整接触来微调保真性
为测试盖板和桥螺旋周围不同接触对活性的贡献,作者改变了连接这些区域的特定带电残基。在正常 Cas12a 中,破坏这些接触对完美匹配 DNA 的切割只有温和影响,尽管在存在不匹配时某些条件影响了第二股 DNA 的切割效率。然而在受损的桥螺旋背景下,相同的替换严重降低或几乎消除了两股 DNA 的切割,尤其在导引 RNA 与 DNA 并不完全匹配时。计算机模拟支持这些发现,显示只有当桥螺旋能够完全采用其螺旋构象时,桥螺旋、相邻螺旋、盖板与核酸才能强烈协同运动。若该螺旋受损,这些运动部分或完全解耦,酶就难以完成其催化循环。
下一代 CRISPR 工具的设计指南
总体而言,这项工作将桥螺旋揭示为一个内部控制杠杆,将 RNA–DNA 杂合体的长度与质量与 Cas12a 切割口袋的打开联结起来。通过强制蛋白在切割 DNA 之前完成一系列特定的构象变化,这一机制天然地强化了对不匹配的识别。研究结果有助于解释为何对这一小区域的定向改变可以得到具有降低脱靶切割和减少“连带”DNA 活性的 Cas12a 变体,这些特性对于更安全的基因组编辑和诊断是可取的。更广泛地说,该研究强调了短螺旋的微妙位移如何协调大型分子机器中的长程通信,为工程高保真核酸处理酶提供了通用原理。
引用: Ganguly, C., Aribam, S.D., dos Santos, A.M. et al. Bridge helix of Cas12a is an allosteric regulator of R-loop formation and RuvC activation. Nat Commun 17, 2126 (2026). https://doi.org/10.1038/s41467-026-68657-0
关键词: CRISPR-Cas12a, 基因编辑保真性, 桥螺旋, R-环形成, 变构调节