Clear Sky Science · zh
RoboA通过FoxA和Anosmin1a增强涡虫干细胞命运的确定
蠕虫如何重建器官
一些扁形虫能重生几乎任何缺失的身体部位,从它们的摄食管到大脑。这种惊人的能力依赖于成体干细胞,它们可以按需分化为多种细胞类型。但在高度自由的情况下,这些细胞如何避免在错误的位置构建错误的组织——例如在头部生成胃细胞而不是神经元?这项研究利用涡虫模型揭示了一小组信号如何在再生过程中将高度可塑的干细胞维持在正确的轨道上。
再生中的涡虫及其潜在能量
涡虫Schmidtea mediterranea是研究再生学的常用模型,因为大量干细胞分布在其全身。一个关键器官是咽(pharynx),即位于虫体中部的肌性摄食管,在动物进食时与外界相连。早期工作表明,一个名为foxA的基因对损伤后重建咽至关重要,而且通常只有靠近咽的特定干细胞会开启foxA。新研究提出一个看似简单的问题:是什么阻止其他区域——尤其是头部和大脑的干细胞——也选择咽的身份?
当引导信号缺失
研究人员把注意力集中在一种名为RoboA的受体蛋白上,这种蛋白在包括干细胞在内的多种细胞类型中以低水平表达。当他们通过RNA干扰降低RoboA活性时,动物在被切割后经常长出额外的、位置错误的咽。更仔细的观察揭示了更微妙的现象:即使在未受伤的涡虫中,下调RoboA也会导致咽样的神经元和肌肉出现在大脑区域内。这些“异位咽神经元”在基因表达上表现得像正常的咽细胞,但位置错误。重要的是,整体体型和大脑结构在很大程度上保持完整,表明RoboA并没有重塑整个动物,而是在微调周围干细胞的命运选择。
细胞命运的三方开关
为了解RoboA的作用,团队寻找细胞外的协同因子。尽管Robo蛋白最著名的是结合一种叫Slit的配体,但敲低Slit并未重现异位咽细胞的表型。一项针对分泌蛋白和膜蛋白的大规模RNAi筛选反而锁定了Anosmin1a(Anos1a),这是一种与人类卡尔曼综合征相关因子有关的分泌蛋白。减少Anos1a会导致类似的额外咽神经元,而同时敲低RoboA和Anos1a的效果显示出它们似乎在同一路径中发挥作用。与此同时,分子分析表明转录因子FoxA处在决策的核心:当RoboA存在时,它在头部干细胞中抑制FoxA;当RoboA信号被去除时,FoxA被激活,这些相同的干细胞即使位于大脑内也可以选择成为咽神经元命运。
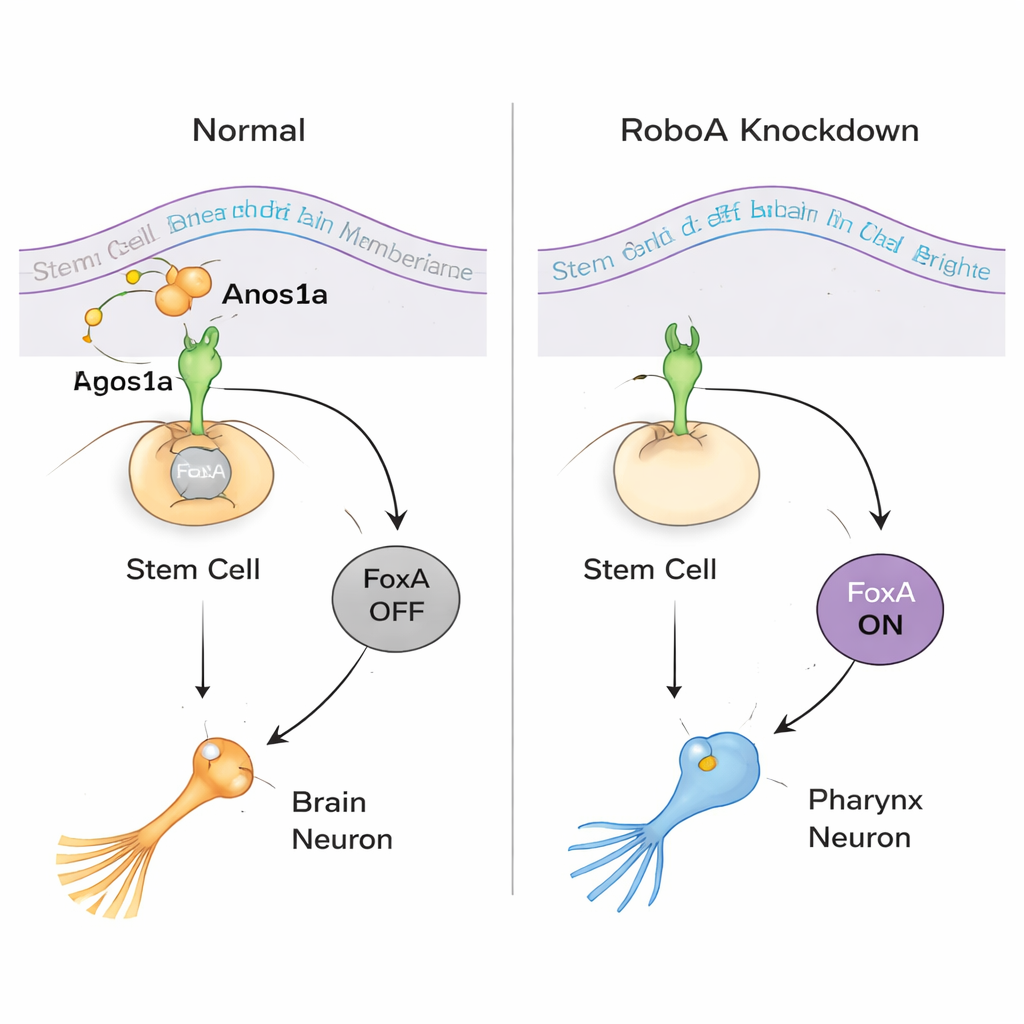
揭示干细胞的双向选择
团队随后探问这种可塑性是否是双向的。在正常动物中,围绕咽的干细胞依赖FoxA分化为咽神经元和上皮细胞,而咽肌则走不同的分化路线。当长时间敲低FoxA时,涡虫完全失去咽并在体中部产生异常的外生长。单细胞RNA测序和标记分析显示,这些外生长包含许多通常局限于头部的细胞类型,包括眼细胞和特异性的大脑神经元。换言之,当咽应形成处缺失FoxA时,当地干细胞会默认走向类脑命运。该发现表明,同一群干细胞可根据所接收的信号被推向“咽”或“脑”两种身份之一。
微调再生,而非重绘地图
综合所有证据,作者提出涡虫再生由两层机制引导。广泛的“位置控制”信号,如Wnt和其他图式分子,建立了头、躯干与尾的粗略地图。在此之上,局部的“命运强化”基因如RoboA和Anos1a充当安全阀,阻止不适当的选项。在头部,RoboA–Anos1a信号抑制FoxA,使干细胞生成大脑神经元而非咽细胞;在咽附近,允许FoxA开启并驱动咽特异性命运。这种分层控制使涡虫干细胞在保持极高可塑性的同时,仍能在正确的位置重建器官,为理解鲁棒的再生如何与严格的解剖秩序共存提供了蓝图。
引用: Wang, KT., Tsai, FY., Chen, YC. et al. RoboA reinforces planarian stem cell fate through FoxA and Anosmin1a. Nat Commun 17, 1971 (2026). https://doi.org/10.1038/s41467-026-68656-1
关键词: 涡虫再生, 干细胞可塑性, 器官图式形成, RoboA信号, FoxA转录因子