Clear Sky Science · zh
非典型每毛细血管 Ly6G⁺Nur77⁺ 巨噬细胞在小鼠肺中启动对过敏原的2型免疫反应
尘螨为何与肺有关
对数百万名哮喘或枯草热患者而言,日常灰尘即可诱发咳嗽、喘息和眼痒——但身体如何首先感知这些看似无害的颗粒长期成谜。本研究在小鼠中揭示了一类先前未知的肺“哨兵”细胞,它们能检测尘螨过敏原并触发驱动过敏的那种免疫反应。了解这一早期警报系统,或可指向在炎症失控成为明显疾病之前预防或抑制过敏反应的新方法。 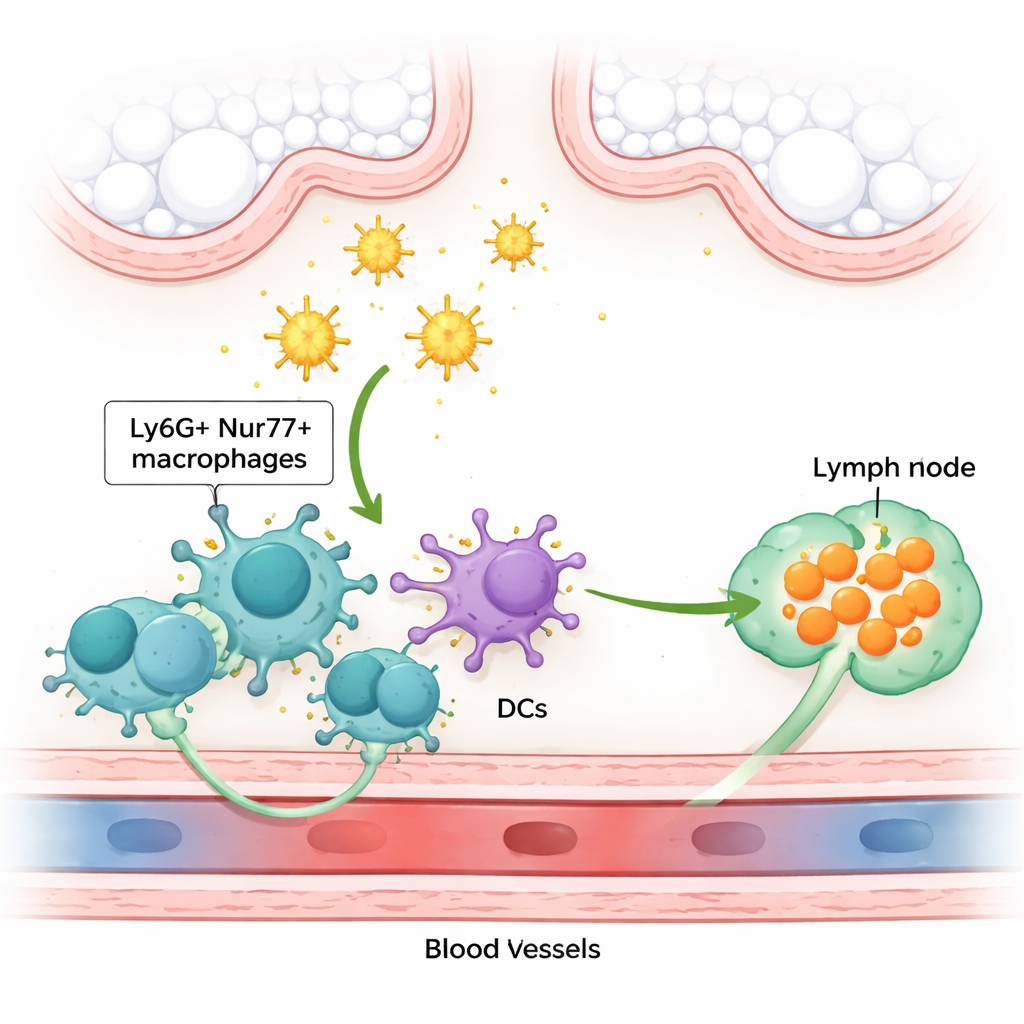
肺血管中的隐秘警报系统
研究者将注意力集中在室内最常见的过敏原之一——尘螨提取物上。研究团队没有把过敏原仅当作简单的外来入侵者,而是问了一个不同的问题:免疫系统是否对过敏原对组织所做的“行为”作出反应?许多尘螨蛋白具有像剪刀一样的作用,会切割其他蛋白。科学家们表明,来自尘螨及相关模型过敏原的特定切割活性——称为半胱氨酸蛋白酶活性——对引发经典的2型反应(与哮喘和其他过敏性疾病相关)是绝对必要的。当这种切割活性被阻断时,小鼠即便仍接触到过敏原,也无法在肺内产生驱动过敏的辅助性T细胞2型(Th2细胞)和嗜酸性粒细胞。
认识包绕毛细血管的“哨兵”巨噬细胞
进一步研究发现一组不寻常的免疫细胞,就位于微小肺血管旁。这些细胞形态类似巨噬细胞——吞噬颗粒的专职细胞——但其表面带有一个意想不到的标志物Ly6G(通常见于中性粒细胞),以及一种名为Nur77(亦称Nr4a1)的核蛋白,参与基因活动调控。由于它们缠绕在毛细血管周围,作者将其称为每毛细血管 Ly6G⁺Nur77⁺ 巨噬细胞。这些哨兵尤其擅长捕获吸入的过敏原:尽管它们仅约占肺细胞的1%,却承担了大量实际吞噬尘螨或胰蛋白酶类过敏原的细胞。它们还形成一个稳定、自我更新的群体,早期定植,与更常见的肺泡巨噬细胞和间质巨噬细胞明显不同。
如何将对过敏原的感知转化为过敏反应
每毛细血管 Ly6G⁺Nur77⁺ 巨噬细胞通过一种称为PAR2的表面受体感知过敏原活性,该受体在被蛋白酶切割后被激活。一旦被富含蛋白酶的过敏原激活,这些巨噬细胞就在肺内增殖并发出化学信号,改变免疫反应的后续进程。它们本身并不迁移到淋巴结;相反,它们控制常规树突状细胞的迁移——后者携带过敏原片段到附近的纵隔淋巴结对T细胞进行致敏。巨噬细胞通过产生半胱氨酸运动白三烯(cysteinyl leukotrienes,尤以LTC₄为主)来实现这一点——这些脂质介质在哮喘治疗领域已为人所知。该类分子通过树突状细胞上的CCR7受体增强其响应引导信号CCL21的迁移能力,从而更有效地到达淋巴结。 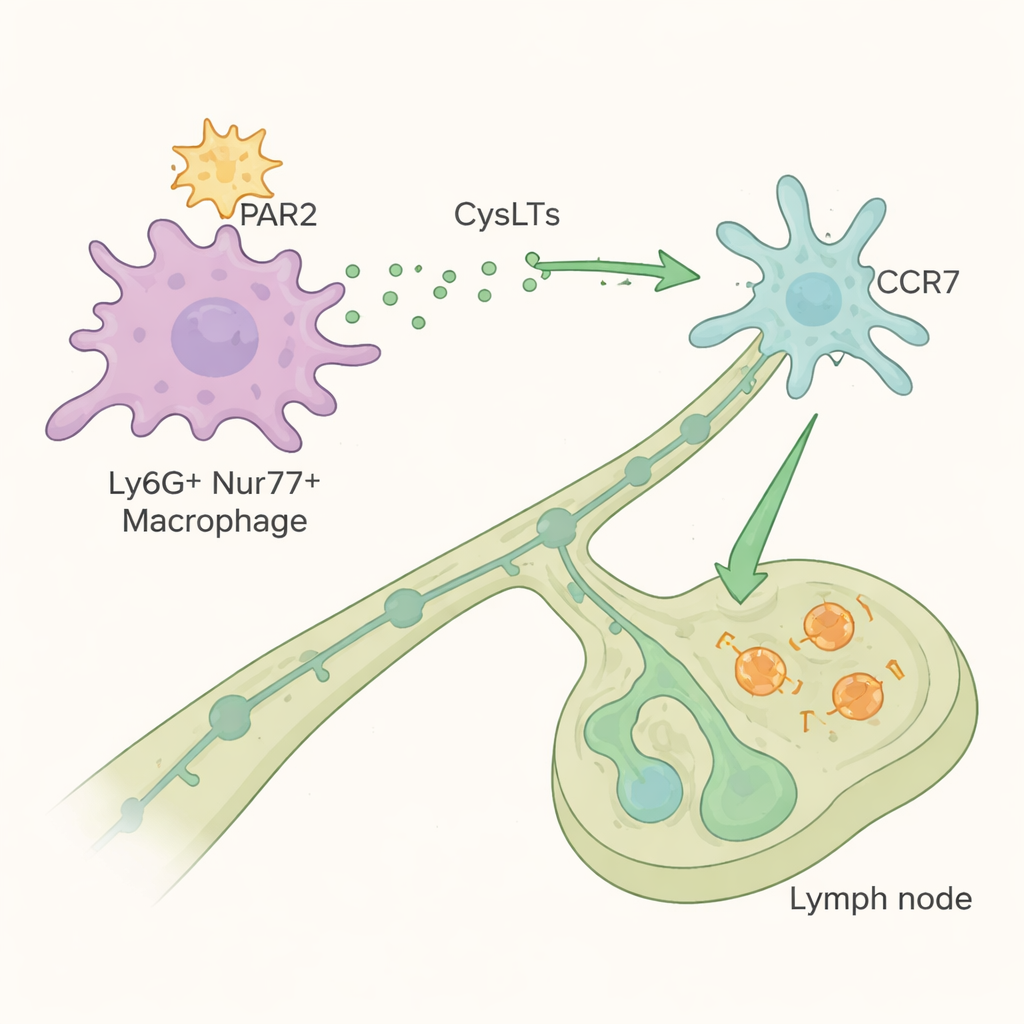
在不关闭全部免疫的情况下关闭信号
利用遗传模型和骨髓嵌合体,作者证明PAR2和Nur77在这些非典型巨噬细胞内在地必须用于它们的扩增、白三烯生成以及驱动树突状细胞迁移。缺乏功能性 Ly6G⁺Nur77⁺ 巨噬细胞或其白三烯合成酶的小鼠表现出淋巴结中树突状细胞到达减少、特异性过敏原T细胞扩增弱以及肺内Th2炎症受抑制。关键在于,该通路似乎对富含蛋白酶的过敏原具有选择性:对病毒感染或细菌信号(LPS)的反应得以保留,提示阻断该通路不会削弱整体免疫。当研究团队药理学抑制生成半胱氨酸运动白三烯的酶LTC₄合酶时,即便药物仅在致敏期间或仅在随后过敏原挑战期间给予,也能显著减少树突状细胞迁移、T细胞致敏和过敏性肺炎症。
对过敏患者意味着什么
简而言之,这项工作识别出一类位于毛细血管旁的专门肺巨噬细胞,它们通过PAR2感知尘螨过敏原的“剪刀”活性,随后利用白三烯召集其他免疫细胞以发起2型过敏反应。通过在源头上靶向白三烯产生,而不仅仅像现有哮喘药那样阻断某一种白三烯受体,或可更精确地降低特异性过敏性炎症,同时保留健康的免疫防御。这个每血管周巨噬细胞—白三烯轴为为何某些环境蛋白成为过敏原提供了新的概念性解释,并突出了预防或减轻过敏性气道疾病的潜在治疗途径。
引用: Meloun, A., Bachus, H., Lewis, C. et al. Atypical pericapillary Ly6G⁺Nur77⁺ macrophages initiate type-2 immune responses to allergens in the mouse lung. Nat Commun 17, 1946 (2026). https://doi.org/10.1038/s41467-026-68652-5
关键词: 过敏性哮喘, 尘螨, 肺巨噬细胞, 白三烯, 2型免疫