Clear Sky Science · zh
NeoPrecis:通过整合经鉴定的免疫原性与克隆性意识的新抗原图谱,提升免疫治疗反应预测
为何有些癌症对免疫治疗有效而有些无效
免疫治疗已改变癌症治疗格局,但仍有许多患者得不到收益,且部分人会出现严重副作用。一个关键问题是为何有的肿瘤会被免疫系统识别并清除,而有的则能逃逸检测。本研究提出了NeoPrecis,一种计算方法,能更精细地评估肿瘤向免疫系统显示的“标志”——称为新抗原——并利用这些信息更好地预测哪些患者更可能对现代免疫治疗产生反应。
癌细胞上的新标志
癌细胞会积累改变其蛋白质序列的DNA突变。这些被改变的蛋白片段,称为新抗原,可以呈现在细胞表面并被T细胞识别——T细胞是免疫系统的“刺客”。多年来,临床医生和研究者常用粗略指标如肿瘤突变负荷(突变总数)来估算癌症对免疫检查点抑制剂的反应可能性。但这是一个粗糙的工具:并非所有突变都会产生可见或吸引T细胞的靶点,而且肿瘤通常由多种不同细胞亚型拼凑而成。NeoPrecis旨在超越简单计数突变,而是评估整个肿瘤中有多少突变真正构成有希望的靶点。
同时考察三种关键要素
NeoPrecis沿三条维度评估每个突变:它在肿瘤中的丰度、是否可能被呈递到细胞表面,以及被T细胞识别的可能性。丰度由DNA和RNA测序估算,揭示突变的普遍程度及其表达强度。呈递通过与MHC I类和II类分子的结合建模,MHC如同广告牌将蛋白片段展示给T细胞。最具创新性的是T细胞识别成分,称为NeoPrecis-Immuno。该模型从大型已知T细胞—肽相互作用数据库中学习,以评估突变片段与其正常对应片段在T细胞识别上有多大差异,同时考虑每个人携带的特定MHC变体。
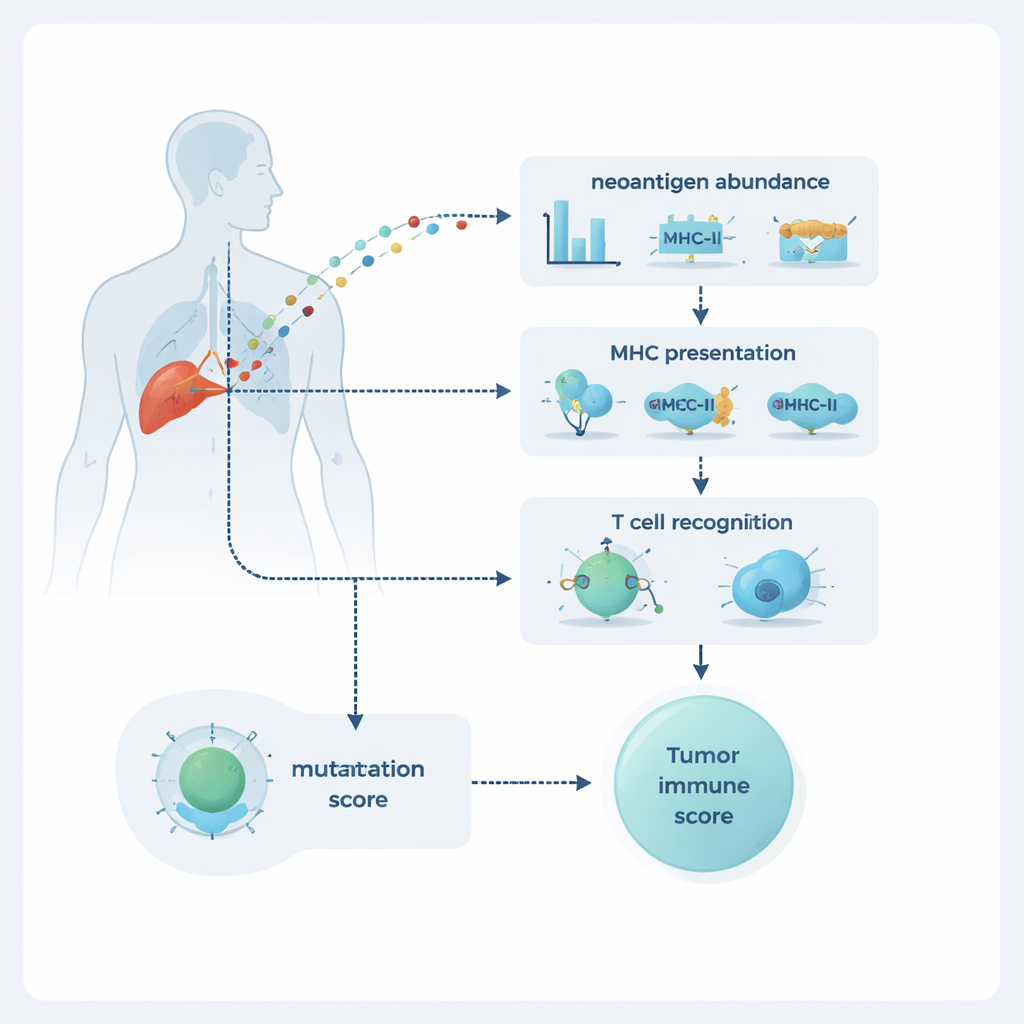
教计算机识别T细胞“看见”的东西
为训练NeoPrecis-Immuno,研究者首先汇集了数千个例子,其中同一T细胞识别多个相似肽的情况以及不识别的情况。他们利用这些例子教会模型:与自身肽非常相似的突变片段较不可能触发免疫攻击,因为这类“自我相似”靶点通常在T细胞发育阶段被清除。模型将每个肽表示为一个数学空间中的点,该空间由氨基酸序列和个体MHC分子的结合偏好共同塑造。然后测量突变肽与原始肽之间的距离;较大且包含基序信息的距离意味着更高的免疫原性。在独立的癌症数据集上与现有工具比较时,NeoPrecis-Immuno表现相当或更优,尤其是在处理向辅助性T细胞呈递的MHC II类时,其优势更为明显。
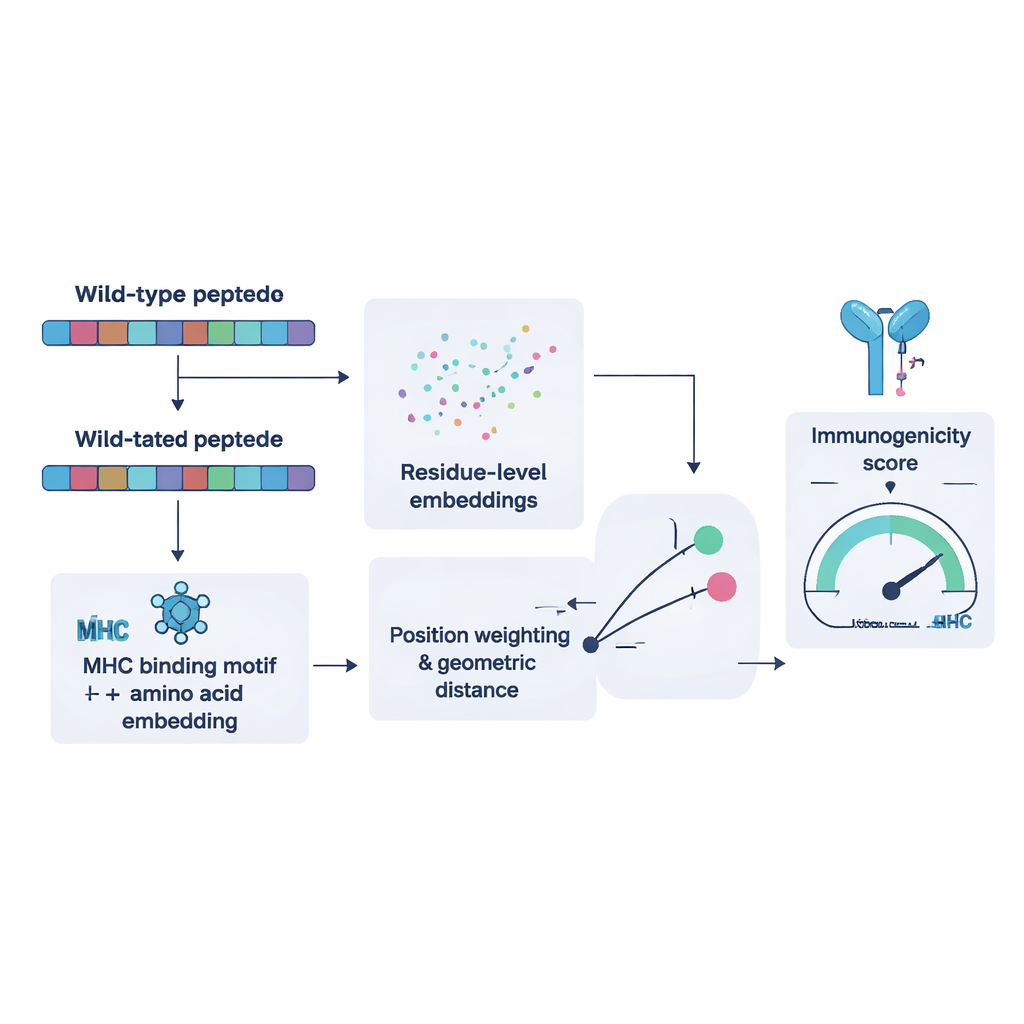
从单个突变到整体肿瘤
单个突变只是部分故事;它们在肿瘤内的分布同样重要。有些突变是“克隆性”的,存在于几乎所有癌细胞中,而有些是“亚克隆性”的,仅出现在特定区域。NeoPrecis通过将每个突变的免疫原性评分相加,并叠加这些突变所属亚克隆及其频率信息,构建了“新抗原图谱”。由此产生的肿瘤级评分能够突出那些富含强效且广泛共享新抗原的癌症——尤其是那些可同时通过MHC I类和II类呈递、可能触发协同的辅助与杀伤性T细胞反应的靶点。在接受检查点抑制剂治疗的黑色素瘤和非小细胞肺癌患者群体中,基于NeoPrecis的评分比标准突变计数更准确地将应答者与非应答者区分开来,且在复杂、异质性高的肺肿瘤中尤为有用。
这对患者意味着什么
对患者而言,NeoPrecis的前景是更精确地将免疫治疗匹配给最有可能受益的人,并更清晰地理解为何有些肿瘤会抵抗治疗。通过关注新抗原的质量与分布——而不单是数量——该框架有助于解释为何具有相似突变负荷的肿瘤可能表现截然不同。未来,这类关于肿瘤对免疫可见性的详尽地图不仅可指导检查点抑制剂的使用,还可用于设计个体化的癌症疫苗,优先针对每位患者肿瘤中最具效力且广泛共享的靶点。
引用: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
关键词: 癌症免疫治疗, 新抗原, 肿瘤异质性, 检查点抑制剂, 计算肿瘤学