Clear Sky Science · zh
斯氏假单胞菌通过在肿瘤细胞中降解STING并减弱免疫反应促进胃肠肿瘤进展
肿瘤内部的隐匿细菌
大多数人知道肠道微生物会影响消化甚至情绪,但很少有人意识到活细菌甚至能寄居在癌细胞内部。这项研究揭示了一种常见环境细菌——斯氏假单胞菌如何潜伏在胃肠道肿瘤内,悄然助长肿瘤生长,同时削弱机体的免疫防御并降低现代癌症免疫疗法的疗效。
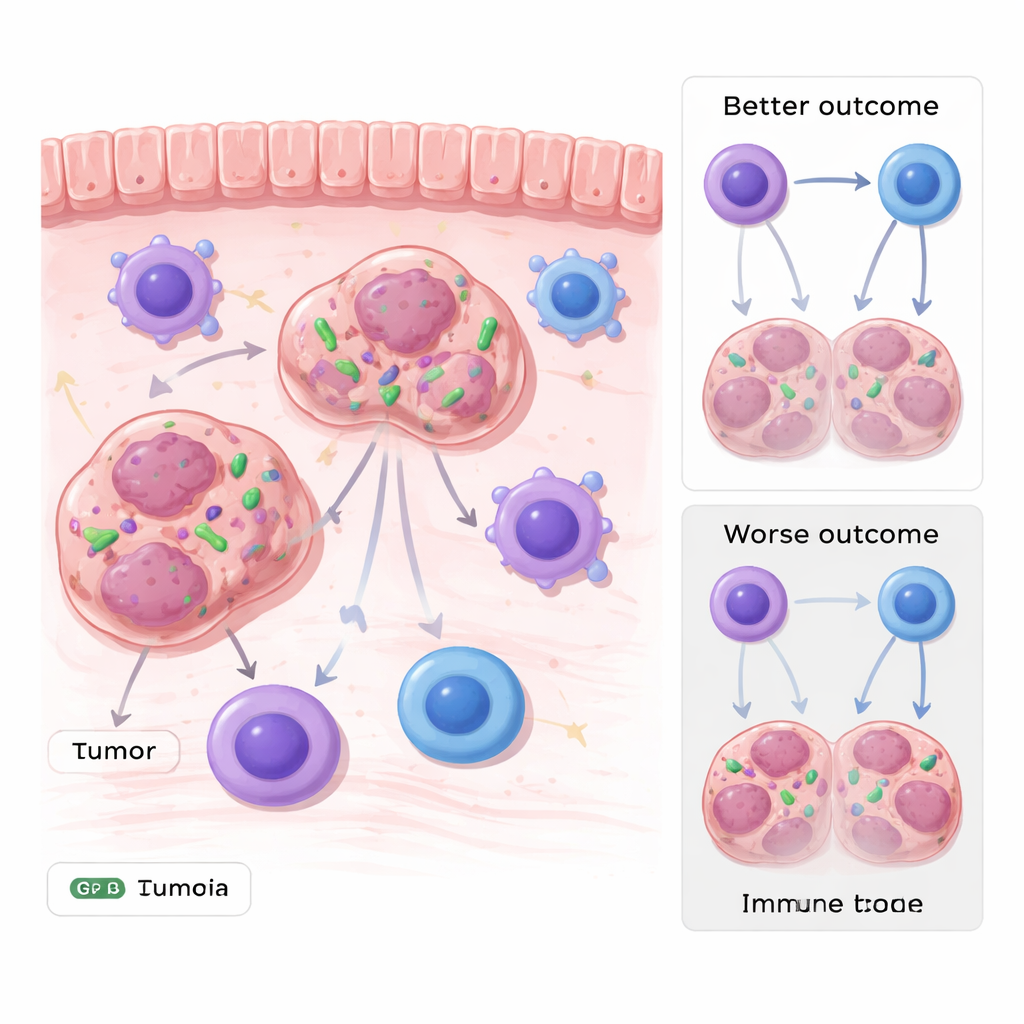
生活在癌细胞内的细菌
胃肠道肿瘤,如胃癌和结直肠癌,一直与消化道丰富的细菌群落紧密接触。研究人员通过挖掘多组病人基因组数据并在肿瘤样本中验证发现,斯氏假单胞菌的DNA在若干类型的胃肠道肿瘤中异常丰富。重要的是,这种存在并非仅为表面污染:包括荧光探针和电子显微镜在内的成像方法显示完整的细菌位于肿瘤细胞的细胞质内。肿瘤中含有较高该细菌水平的患者随访预后更差,将该微生物与更差的预后联系起来。
微生物如何倾斜免疫天平
团队接着探究这些隐匿细菌是仅与侵袭性肿瘤相关还是在实质上推动疾病发展。在小鼠模型中,他们在移植入动物之前用荧光标记的斯氏假单胞菌感染肿瘤细胞。携带该细菌的肿瘤在多种肿瘤细胞类型中均生长更快、更大。检查肿瘤周围的免疫景观时,研究者发现免疫细胞总数,包括T细胞和巨噬细胞相近。关键差异在于一类专业化的、表达MHC-II分子的巨噬细胞,这类细胞帮助向细胞毒性T细胞呈递肿瘤抗原。在含有斯氏假单胞菌的肿瘤中,MHC-II阳性巨噬细胞明显减少,T细胞的抗肿瘤杀伤活性也减弱。
短路细胞的警报系统
为了解机制,研究者关注细胞内的关键警报通路STING,该通路通常感知外源DNA并触发抗病毒的“危险”信号——I型干扰素的释放。在体外实验中,被斯氏假单胞菌感染的肿瘤细胞产生的干扰素β明显减少,该通路通常激活的基因表达也被抑制。研究显示,细菌诱发了内质网这一蛋白折叠工厂的应激反应,继而劫持了一条称为ER相关降解(ERAD)的质控通路。通过名为SEL1L的辅助蛋白,该通路将STING蛋白标记并送往细胞的蛋白酶体“粉碎机”降解。STING水平被耗竭后,肿瘤细胞发出的警报变弱,导致干扰素减少,并在下游抑制MHC-II阳性巨噬细胞的活化。
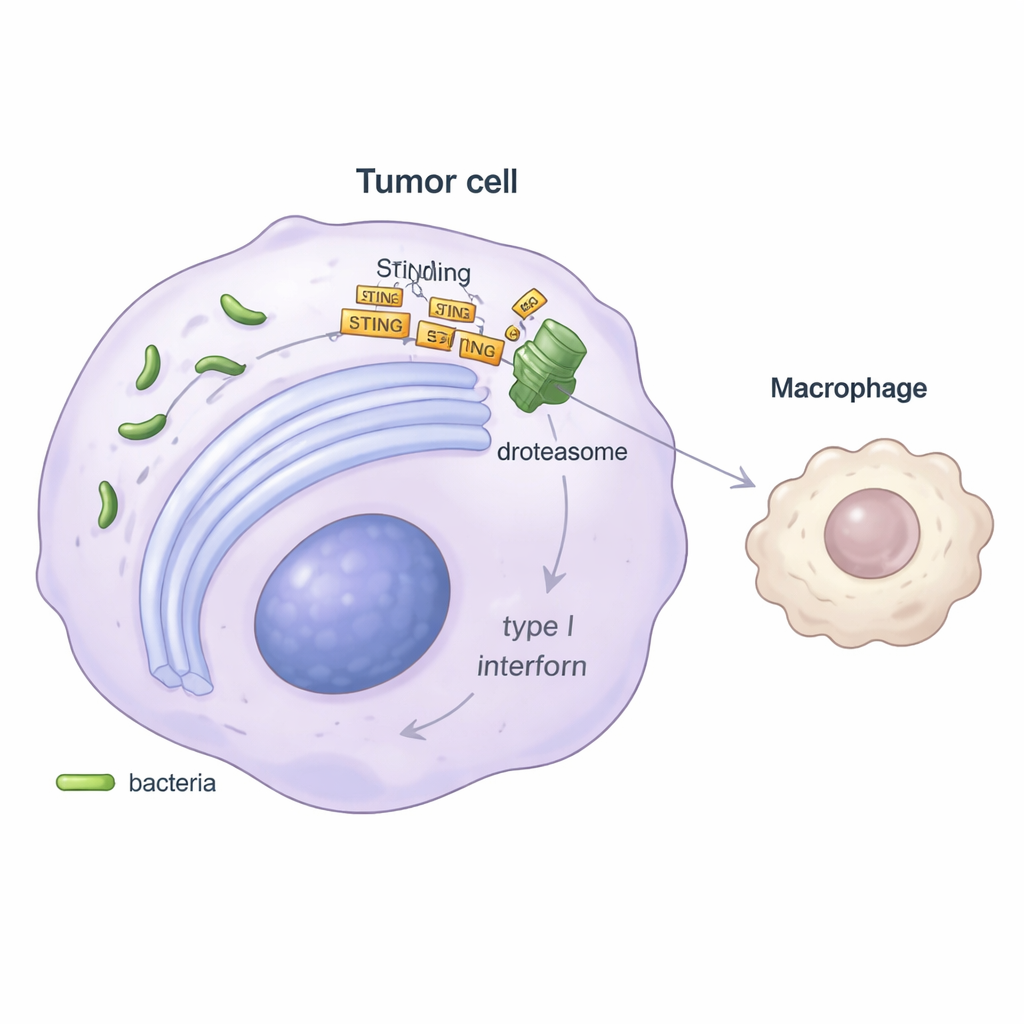
削弱免疫治疗——以及可能的解决办法
鉴于现代免疫疗法如抗PD-1药物依赖强烈的T细胞反应,团队测试了细胞内斯氏假单胞菌如何影响治疗。在小鼠中,携带该细菌的肿瘤对抗PD-1治疗的响应不佳,而无菌肿瘤反应较好,即便联合化疗也无法完全弥补。此类肿瘤中的T细胞表现出活性和增殖标志的降低,显示免疫刺激不足。引人注目的是,当研究者用能有效杀灭斯氏假单胞菌的抗生素左氧氟沙星治疗动物时,肿瘤生长放缓且对抗PD-1治疗的敏感性提高。用临床干扰素药物恢复干扰素信号在某些情况下也能挽救有益的MHC-II阳性巨噬细胞群并恢复T细胞的杀伤功能,这强调了该通路的核心作用。
这对患者意味着什么
对普通读者而言,关键结论是一些胃肠道癌症可能携带内部微生物群,从而帮助它们逃避免疫攻击。斯氏假单胞菌通过在肿瘤细胞内降解STING警报系统,削弱了本应召集巨噬细胞和细胞毒性T细胞的免疫信号。这不仅加速肿瘤生长,也可能帮助解释为何某些患者无法从强效免疫疗法中获益。虽然在临床实践中应用尚需更多研究,但这些发现提示:检测肿瘤中此类细菌——并选择性地用靶向抗生素或稳定STING的药物加以处理——未来有可能改善胃癌和结直肠癌患者的预后。
引用: Feng, H., Chen, K., Xi, Z. et al. Stenotrophomonas promotes gastrointestinal tumor progression via STING degradation in tumour cells and mitigated immune response. Nat Commun 17, 2042 (2026). https://doi.org/10.1038/s41467-026-68649-0
关键词: 肿瘤微生物组, 胃肠道癌症, 斯氏假单胞菌, STING通路, 癌症免疫治疗