Clear Sky Science · zh
NR6A1 对神经嵴细胞的命定、形成与存活至关重要
早期细胞抉择如何塑造面容与身体
在我们出生之前,一类特殊的细胞——神经嵴细胞——穿行于胚胎之中,参与构建面部、心脏、神经等多种结构。当这些细胞发生异常时,新生儿可能出现严重的先天缺陷。该研究揭示了一个此前未被充分重视的分子开关:一种名为 NR6A1 的蛋白,决定了哺乳动物胚胎中神经嵴细胞何时何地形成,以及当该开关失灵时会发生什么。
胚胎中的迁徙“建造者”
神经嵴细胞在发育非常早期沿着正在形成的脑与脊髓边界出现。它们从该组织脱离后进行长距离迁移,构建许多不同结构——从面部骨骼与软骨,到外周神经系统的部分,以及皮肤中的色素细胞。由于它们参与众多器官的形成,即便是微小的形成异常也可能引发广泛的疾病,统称为神经嵴病(neurocristopathies),例如特雷彻·柯林斯综合征等颅面畸形。因此,弄清这些细胞最初如何出现对于解释正常发育与先天缺陷至关重要。
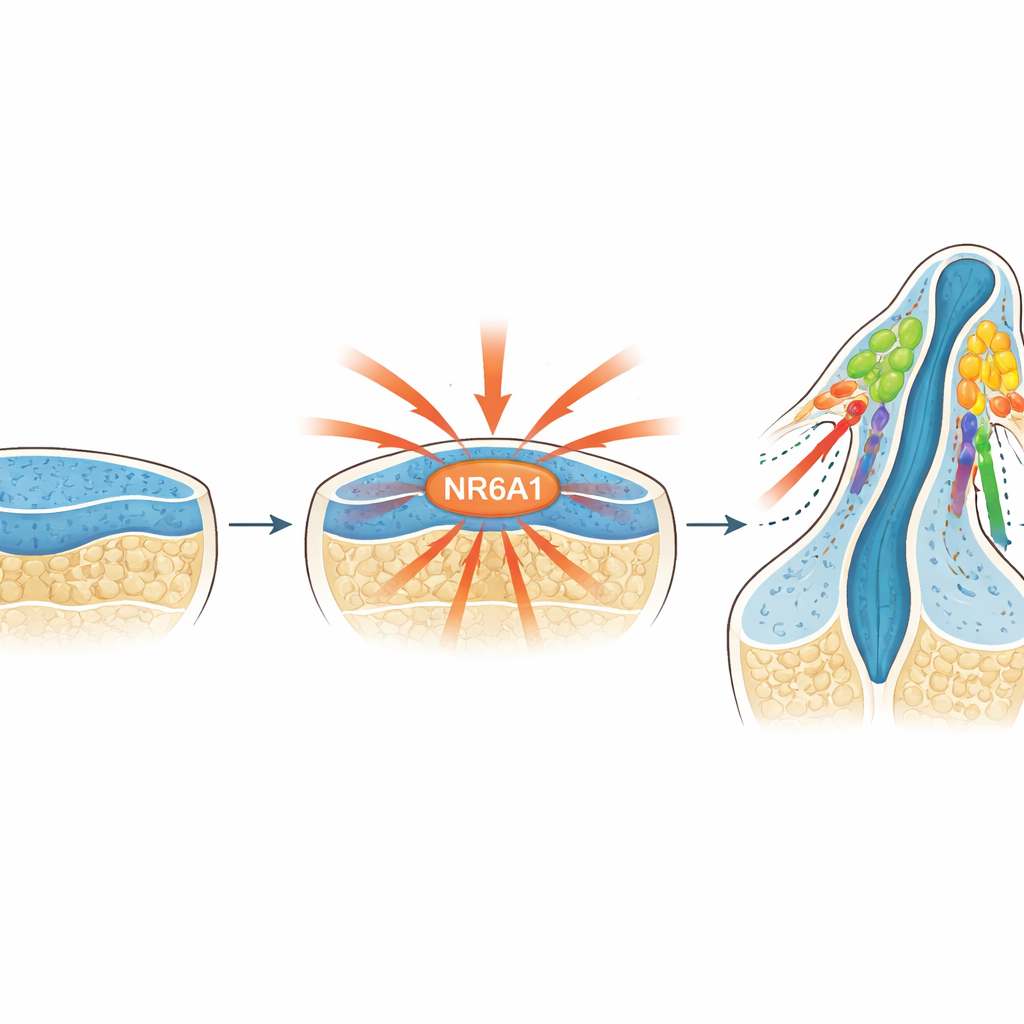
一种新识别的主控开关
研究者聚焦于 NR6A1,这是一类核受体家族蛋白,负责调控基因活动。早期研究提示 NR6A1 可能参与头颅与面部缺陷,但其在神经嵴细胞中的作用尚不清楚。通过追踪植入后小鼠胚胎中的 NR6A1 表达,研究团队发现其空间与时间模式与神经嵴细胞的出现高度一致:NR6A1 在早期神经组织中出现,随后在正在形成的脑与脊髓的背侧集中,并能在细胞刚从该组织脱离、开始迁移时被检测到。
缺失这一开关会怎样
完全缺乏 NR6A1 的小鼠在发育早期即致死,所以团队观察了致死前的胚胎。他们发现神经嵴细胞严重缺乏,尤以将形成颌与颈部部分的第一咽弓后方为甚,迁移中的神经嵴细胞几乎完全缺失。通常标记神经嵴身份并使细胞脱离、迁移的关键基因程序显著下降。与此同时,维持细胞干性、高度增殖状态的基因持续开启,且为数不多形成的类似神经嵴的细胞很快死亡。这些发现表明,缺少 NR6A1 时,神经干细胞无法正确转变为迁移性的神经嵴细胞并难以存活。
关闭“干性”并开启迁移程序
为弄清 NR6A1 如何发挥这种调控作用,作者结合了多种强大的分子技术,包括单细胞 RNA 测序、染色质可及性绘图以及在小鼠与人类干细胞来源的神经嵴细胞中进行的靶向 DNA–蛋白结合测定。他们发现 NR6A1 能物理结合位于调控两类相对立程序基因附近的特定 DNA 基序:一类维持多能性(即成为多种细胞类型的能力),另一类驱动神经嵴身份与细胞迁移。NR6A1 存在时,围绕干性基因(如 Oct4 与 Nanog)的染色质变得不那么可及,这些基因被抑制;而靠近神经嵴及上皮-间质转化相关基因的区域则变得更开放和活跃。在神经嵴形成的关键时间窗口内过表达 Oct4 会模拟 NR6A1 缺失的效应,进一步表明必须沉默干性程序,神经嵴细胞才能出现。
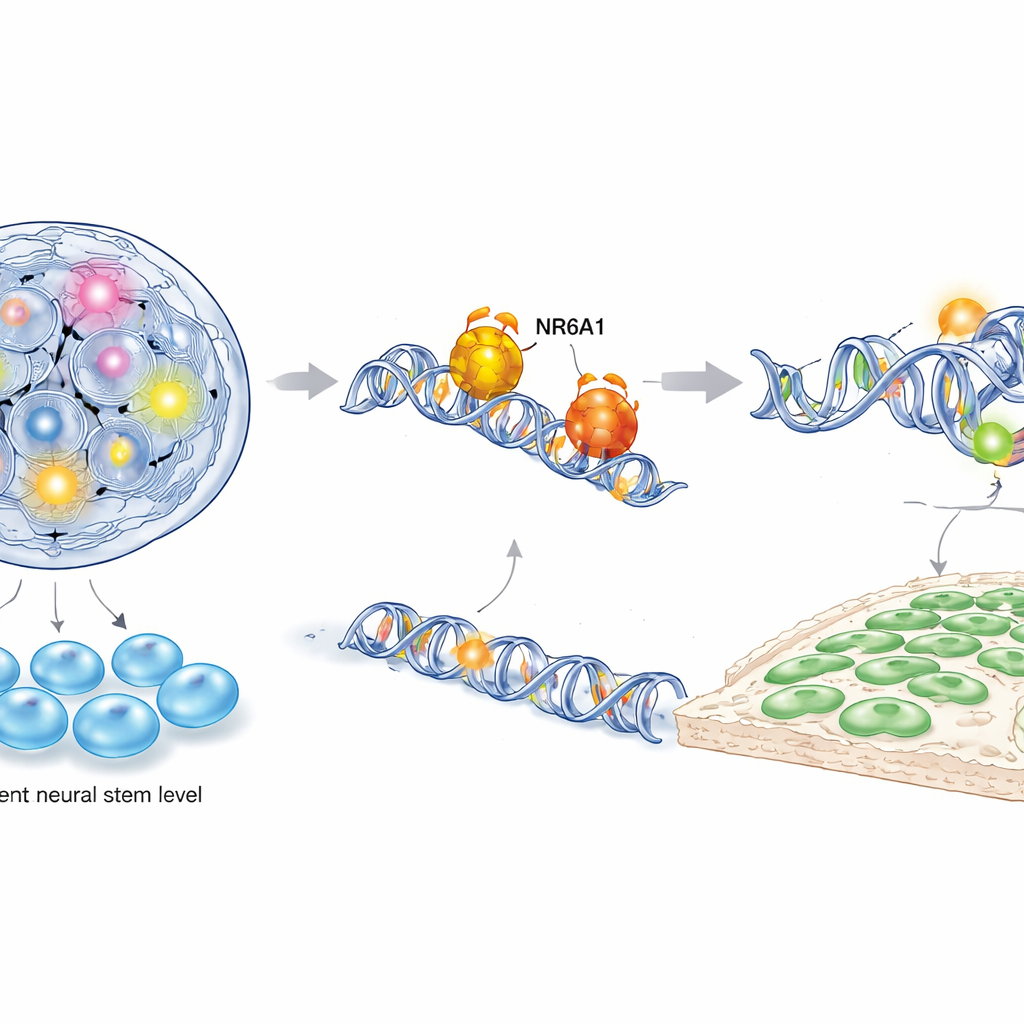
重写早期发育的时间表
该研究还修订了哺乳动物神经嵴细胞开始被命定的时间表。利用一种可诱导的遗传系统在不同时期去除 NR6A1,团队显示在中胚层化早期(mid-gastrulation)之前删除该基因——比传统认为的时间更早——就足以阻断神经嵴基因的激活。相比之下,在更晚阶段删除 NR6A1(包括使用广泛采用的神经嵴特异驱动系)则未见明显缺陷。这说明关于神经嵴命运的关键决定是在这些常规模型开始起作用之前完成的,也解释了为何一些早期小鼠研究可能忽略了对该过程的早期需求。
这对先天缺陷与疾病意味着什么
总体而言,这项工作将 NR6A1 描述为一个核心协调因子,帮助神经干细胞“成长”为神经嵴细胞:它同时关闭多能性程序并启动迁移与存活程序。这种双重作用似乎始于中胚层化期,比此前在哺乳动物中认识的要早,并使小鼠的发育时间与其他脊椎动物更为一致。通过澄清该开关何时及如何运作,研究为重新解释早期遗传实验、识别更合适的研究神经嵴生物学的工具提供了框架,并最终有助于理解乃至预防因这一早期发育抉择失常而产生的神经嵴疾病。
引用: Moore Zajic, E.L., Muñoz, W.A., Dennis, J.F. et al. NR6A1 is essential for neural crest cell specification, formation and survival. Nat Commun 17, 2140 (2026). https://doi.org/10.1038/s41467-026-68647-2
关键词: 神经嵴细胞, NR6A1, 胚胎发育, 多能性转换, 神经嵴疾病