Clear Sky Science · zh
通过综合计算与实验框架设计 MmeFz2-ωRNA 系统以实现高效基因组编辑
为重大医疗问题打造更小的“基因剪刀”
基因编辑已经改变了科学家研究疾病的方式,但要将其转化为安全且可行的药物仍然是重大挑战。一个重要障碍是,如 CRISPR-Cas9 这类当前最强大的 DNA“剪刀”体积大,难以装入患者使用的微小递送载体。该研究介绍了一种基于鲜为人知的 Fanzor2 酶家族构建的新型紧凑基因编辑工具,并展示了人工智能如何快速将其重新设计为未来基因疗法的有力候选者。
一种新型紧凑基因编辑器
目前大多数基因组编辑器,如 Cas9 和 Cas12a,都是由一千多个氨基酸组成的大型蛋白质。如此体积使它们难以塞入腺相关病毒(AAV)——基因治疗的主要递送系统。相比之下,Fanzor2 蛋白要小得多,天然存在于真核生物中,真核生物包括动物和人类。作者们聚焦于该家族中的一个成员 MmeFz2,它使用一种称为 ωRNA 的短 RNA 分子来定位并切割特定 DNA 序列。从纸面上看,MmeFz2 适合用于治疗:体积小且可编程。但在实际的人类细胞中,其活性非常低,目标位点的编辑率不足 1%。研究团队的目标是将这一表现不佳的酶改造为实用工具。
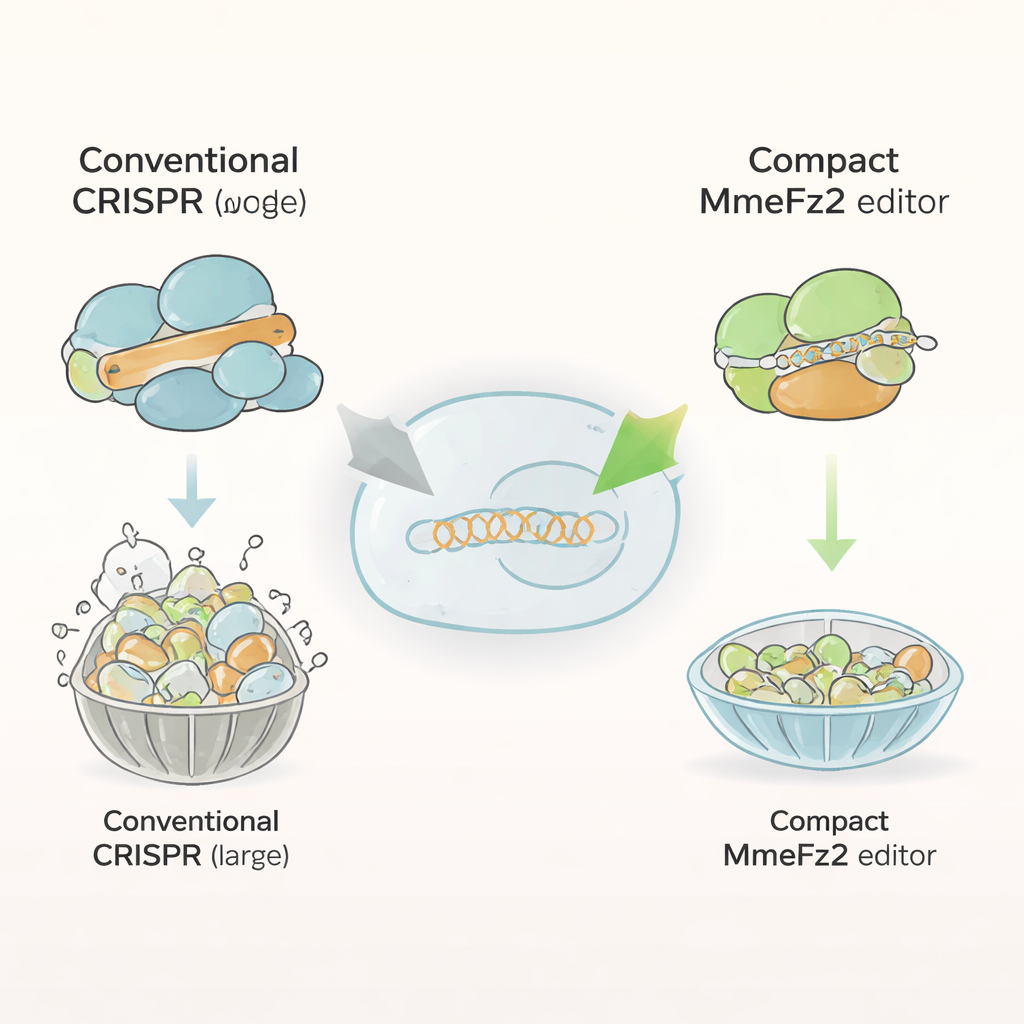
用人工智能重新设计引导分子
首要目标是 ωRNA,即指引 MmeFz2 切割位置的引导分子。研究者利用 AlphaFold3——一款前沿的蛋白–RNA–DNA 复合物 3D 结构预测程序——构建了 MmeFz2 与其 ωRNA 及 DNA 靶标结合的模型。该虚拟结构显示,ωRNA 的部分区域松散、配对不良,且与蛋白接触有限。基于这些信息,团队有系统地替换了 RNA 中不稳定的连接,并去除了可能干扰转录的一段尿苷序列。随后在人体细胞中测试了数十种变体。通过叠加最佳改动并修剪掉不必要的茎环结构,他们制造出一种缩短约 30% 的 ωRNA,但在多个 DNA 位点上实现了接近 20 倍的编辑效率提升。
用机器学习微调蛋白质
接下来,团队对蛋白本身进行了精细改造。他们再次利用 AlphaFold3 映射 MmeFz2 与 RNA 和 DNA 的接触位点,并设计了 100 多处单个氨基酸的替换,旨在增强这些接触或改善柔性。在细胞中筛选这些突变后,他们将性能数据输入 EVOLVEpro——一个基于蛋白质语言模型的机器学习系统,模型以数百万条天然序列进行训练。该工具学习出哪些特征倾向于提高活性,并建议了新的突变组合,预测将更为有效。通过几轮该计算—实验循环,科学家找到了两个优化的酶变体,当与改良的 ωRNA 配对时,相较于起始系统将编辑活性提升了超过 60 倍。
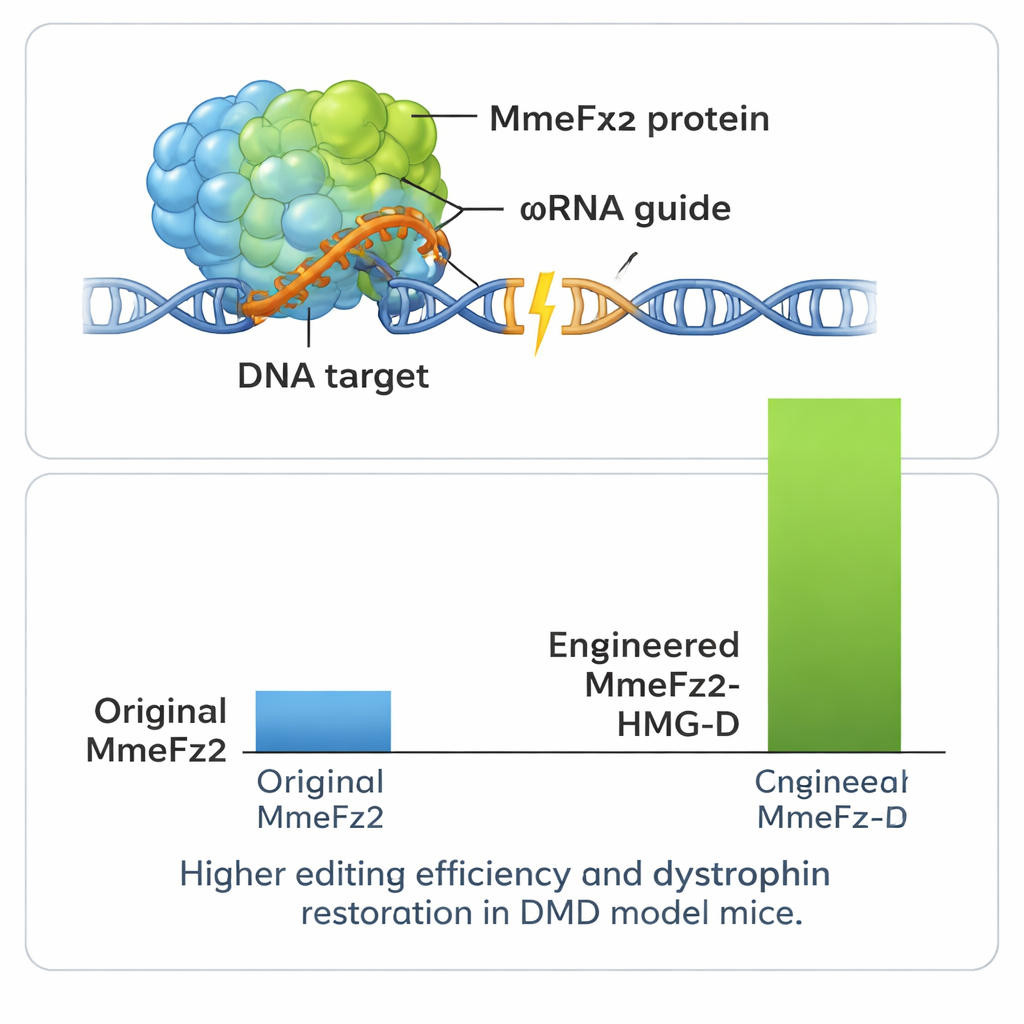
提升效能并在疾病模型中测试
为了进一步挖掘系统性能,作者将 MmeFz2 与小型 DNA 结合域融合,这些结合域可帮助蛋白更好地附着到基因材料上。其中一种称为 HMG-D 的结合域在连接到工程化酶的末端时尤为有效,在某些位点产生了超过 80% 的编辑水平。重要的是,对基因组中预测的脱靶位点进行测试表明,这种性能增强并未带来显著的精度损失。由于整个基因编辑器——包括蛋白和引导 RNA——体积非常紧凑,它可以舒适地装入单一的 AAV 载体,这对于大多数 CRISPR 系统是不可能的。研究团队利用这一优势在杜氏肌营养不良的小鼠模型中进行了验证——该病是一种由抗肌营养蛋白(dystrophin)基因缺陷引起的致命肌肉萎缩性疾病。一次性将 AAV 递送的编辑器注射入腿部肌肉后,检测到基因转录本的修正,并在相当一部分肌肉纤维中恢复了抗肌营养蛋白的表达。
这对未来基因疗法意味着什么
对非专业读者来说,关键信息是:作者已将一种弱小且鲜为人知的基因切割酶改造成一种紧凑、高性能的编辑器,可装入单一病毒载体,并能在现实的动物模型中修复严重的遗传疾病。同样重要的是他们的方法:将基于 AI 的结构预测与机器学习紧密结合目标明确的实验测试,比传统的反复试错更高效地改进了蛋白和其引导 RNA。这种一体化策略可能会加速下一代多种基因编辑器的开发,使更精确、更安全的基因疗法更快地惠及肌营养不良和其他遗传性疾病的患者。
引用: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
关键词: 基因编辑, CRISPR 替代方案, 杜氏肌营养不良, 病毒基因治疗, 生物学中的人工智能