Clear Sky Science · zh
C1q依赖性的α-突触核蛋白清除使巨噬细胞在雄性小鼠中暂时限制肠道突触核蛋白病
为何肠道在脑病中重要
帕金森病以震颤和运动障碍最为人所知,但许多人在出现任何运动症状前多年就经历严重便秘和其他肠道问题。本研究探讨了当与帕金森相关的蛋白在“第二大脑”——肠道内的神经网络中发生错误折叠时会发生什么,以及局部免疫细胞最初如何协助然后失效。理解肠道中这场早期斗争可能为缓解症状并在大脑严重受损前减缓疾病进展开辟新途径。
存在于身体第二大脑的问题蛋白
在帕金森病及相关疾病中,一种称为α-突触核蛋白的蛋白可能发生错误折叠并聚集成有毒缔合体。这些聚集体不仅在大脑中发现,也遍布控制肠道运动的肠神经系统。许多研究者怀疑,在至少部分患者中,错误折叠的α-突触核蛋白可能首先在肠道安营,然后沿神经通路向大脑扩散。作者使用了一种小鼠模型,将预制的α-突触核蛋白纤维注入胃和上小肠。在接下来的两个月里,他们观察到标记的异常α-突触核蛋白在肠道神经元内稳步增加。这种堆积与肠道物质通过速度变慢和粪便排出减少同时发生,类似许多帕金森病患者出现的便秘。
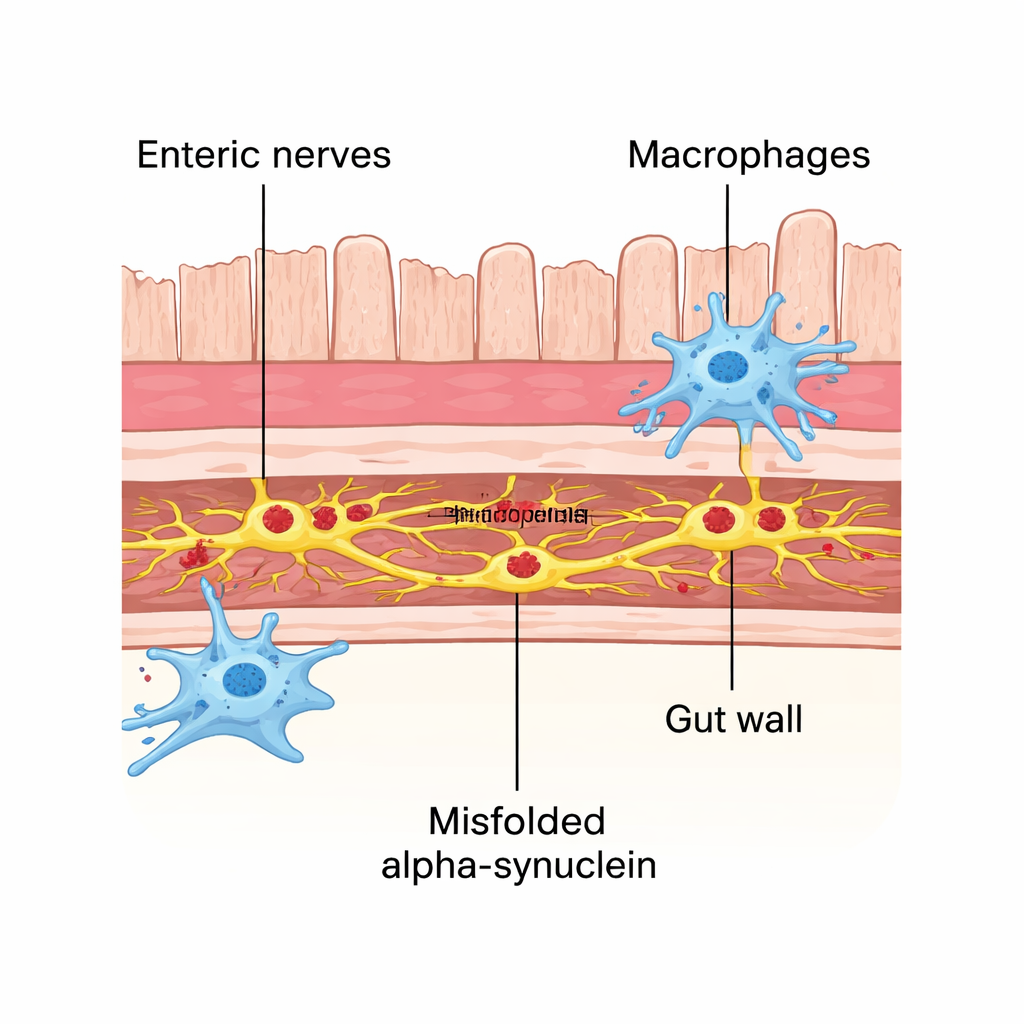
肠道免疫细胞作为第一响应者介入
肠壁中含有常驻免疫细胞——巨噬细胞,它们不断与邻近神经元交流并有助于维持组织健康。在该模型中,这些巨噬细胞不仅对损伤作出反应:它们更频繁地与受影响的神经簇发生物理接触,并在自身内含有错误折叠蛋白的小斑点。当研究者用抗体处理耗尽这些巨噬细胞时,肠神经元中的α-突触核蛋白病理显著增加。这表明肠道巨噬细胞在早期发挥保护作用,充当吞噬并清除有毒蛋白的细胞清道夫,从而在其扩散到邻近神经细胞之前将其移除。
一种有益亦有害的分子标签
为理解这些免疫细胞如何识别要清除的目标,研究团队采用单细胞RNA测序,对数千个单个肠道免疫细胞进行了分析。他们鉴定出肠道肌层中特定的巨噬细胞亚型,这些细胞开启了与吞噬和蛋白降解相关的基因,尤其是补体系统的组分——这是一种更为人熟知于血液中的分子标记途径。其中一个关键成分C1q在这些肠道巨噬细胞中高度活跃。在显微镜下,C1q覆盖在受影响的肠神经元上,巨噬细胞内含有同时对C1q和错误折叠α-突触核蛋白呈阳性的斑点,表明C1q有助于将有毒蛋白标记以便清除。当科学家使用缺失C1q的基因敲除小鼠时,神经元内的α-突触核蛋白病理加重,巨噬细胞吞噬的蛋白团块减少。然而,出人意料的是,这些缺乏C1q的小鼠在暴露于相同纤维后的肠道蠕动性比正常小鼠稍好一些,这暗示着清除有毒蛋白的过程本身也可能扰乱肠功能——很可能通过修剪或削弱控制运动的神经连接来实现。
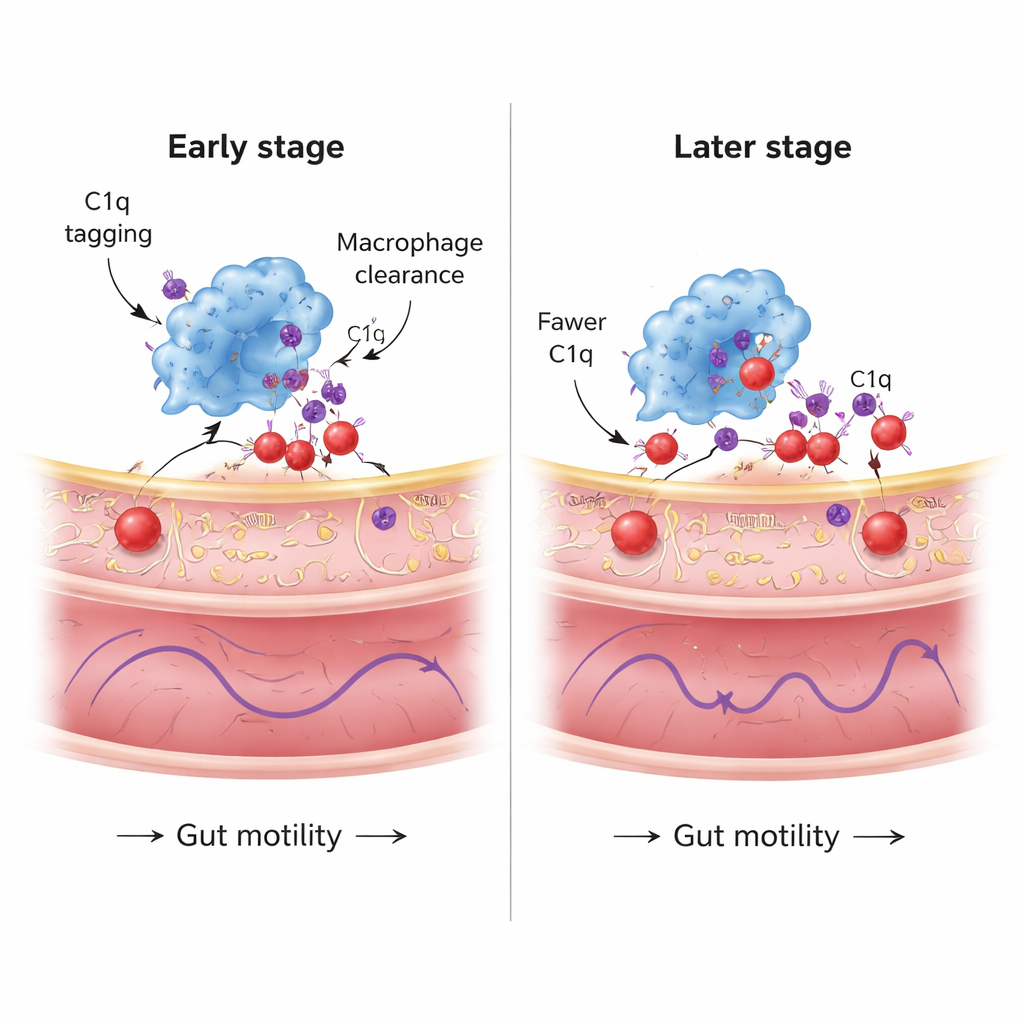
随时间衰减的保护系统
研究还随访了这一路径的长期清除反应。在将α-突触核蛋白引入约一个月后,巨噬细胞显示出强烈的C1q表达,并在其胞体内有许多被C1q标记的蛋白斑点,C1q也大量覆盖在肠神经元上。然而到两个月时,尽管巨噬细胞内整体C1q水平仍在,但被内吞的C1q/α-突触核蛋白斑点数量以及沉积在神经元上的C1q数量已下降。与此同时,肠内的神经病理继续增加。基因分析表明,持续摄取错误折叠蛋白会给巨噬细胞的蛋白处理机制带来负担,激活与错误折叠蛋白、溶酶体乃至细胞死亡相关的应激通路。换言之,巨噬细胞的保护能力似乎是有限的:它们最初能抑制病理,但随着应激积累,其清除α-突触核蛋白的能力减弱。
这对帕金森病与肠道意味着什么
这项工作描绘了肠道免疫细胞如何塑造肠道早期帕金森样变化的细致图景。起初,常驻巨噬细胞通过利用C1q标记并吞噬肠神经元中的错误折叠α-突触核蛋白来限制其扩散。但这一由补体驱动的修剪过程可能损害神经信号传递并减慢肠道,助长便秘。随着时间推移,巨噬细胞因应激负担而衰竭,其清除系统减弱,使更多病理累积,即便肠功能与大脑受累情况出现分化。对患者来说,这提示了一个潜在策略:在肠道中调节巨噬细胞活性或补体信号,既增强安全清除又避免过度突触丧失,或许有望治疗或预防帕金森相关的肠道症状,并可能影响疾病更广泛的进程。
引用: Mackie, P.M., Koshy, J.M., Bhogade, M.H. et al. C1q-dependent clearance of alpha-synuclein allows macrophages to transiently limit enteric synucleinopathy in male mice. Nat Commun 17, 1877 (2026). https://doi.org/10.1038/s41467-026-68641-8
关键词: 帕金森病, 肠神经系统, α-突触核蛋白, 肠道免疫细胞, 补体C1q