Clear Sky Science · zh
调节 Nudt21 水平揭示可变剪接末端选择在组织再生中的剂量依赖作用
细胞如何保持组织年轻
我们的身体不断自我修复。隐藏在皮肤、肠道、骨髓和肌肉中的干细胞悄然替换老化的细胞,使组织保持健康。本文探讨了这些干细胞内部一个看不见的调控层——它们如何完成 RNA 信息的末端处理——并展示了该过程中的细微变化如何决定组织是顺利再生、停滞还是失败。 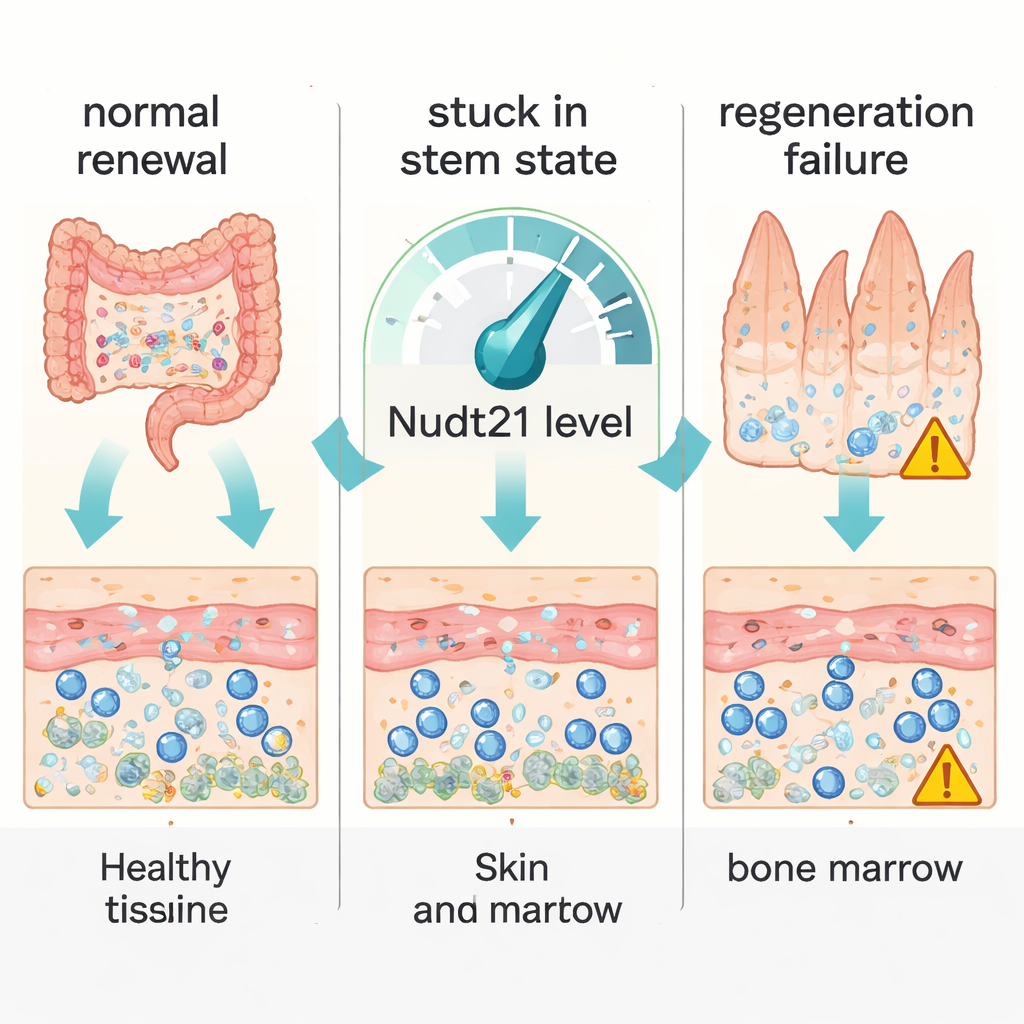
剪切遗传讯息的尾端
细胞中被激活的每个基因首先被转录成 RNA 信息。在该信息被用于制造蛋白质之前,末端会被加上一段化学“尾巴”,这一过程称为聚腺苷酸化。许多基因有多个可能的切割位点,因此相同的讯息可以以更长或更短的尾端结束。这些尾端区域称为 3'UTR,不编码蛋白,但作为其他调控因子的停靠位点,包括微小 RNA(microRNA),它们精细调节蛋白质的生成量。蛋白 Nudt21 帮助细胞选择切割位置,从而决定这些 RNA 尾巴的长度。
同一个控制旋钮却有两种截然不同的效果
研究者构建了小鼠模型,可以在成体组织中将 Nudt21 下调或完全关闭。当 Nudt21 在全身被完全移除时,动物很快生病并死亡,但并非因为心脏或肾脏等“静态”器官衰竭。相反,高翻转率组织——如肠道与食道的上皮、骨髓中的造血系统以及称为卫星细胞的肌肉干细胞——丧失了自我更新的能力。这些组织中的干细胞与祖细胞停止进入细胞周期,无法复制 DNA 和分裂。相比之下,当 Nudt21 水平仅被部分降低时,干细胞仍能增殖,但不再适当地成熟为特化细胞,这表明自我更新和分化对同一控制因子的剂量阈值有不同的响应。
绕过分化制动器的缩短讯息
为弄清细胞内部发生了什么,团队绘制了 RNA 被切割的位置并监测了蛋白质水平的变化。在中度降低 Nudt21 的情况下,约有一千条 RNA 讯息从较长的尾端切换为较短的尾端。由于许多丢失的片段携带微RNA 结合位点,这些缩短的讯息变得更难被沉默。包括重塑染色质的酶和运输蛋白在内的细胞身份与发育关键调控因子被过度生成。这种过度产生扰乱了“竞争性 RNA”网络,在该网络中许多讯息共享相同的微RNA 调控因子。总体效果是干细胞被锁定在不成熟状态:它们保留干细胞标志,但未能启动完成分化所需的基因,即便在强烈的促分化信号下亦然。
当细胞的机器崩溃时
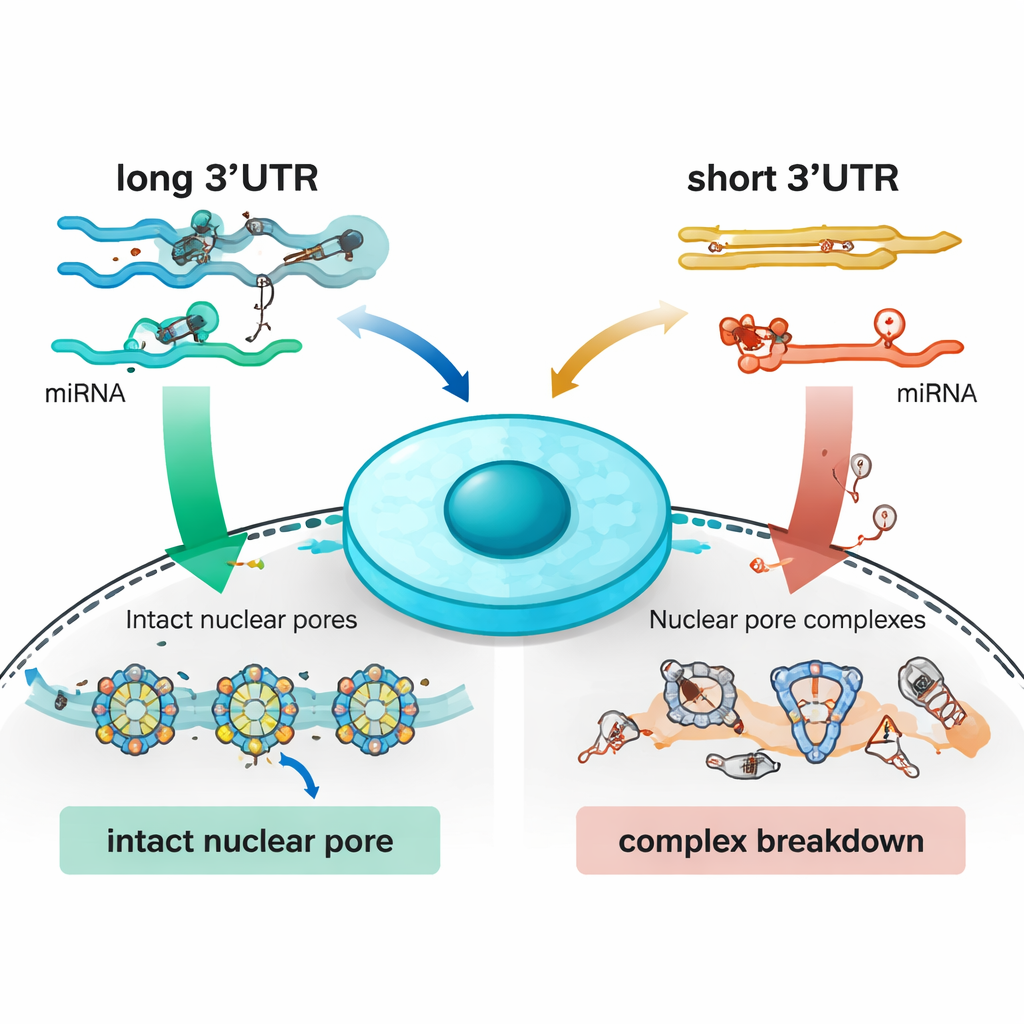
完全丧失 Nudt21 产生了更严重且出乎意料的后果。除了分化阻滞外,许多编码关键多蛋白机器组件的讯息也获得了缩短的尾端。与前者相反,这些讯息往往产生更少的蛋白质,而不是更多。最显著的例子是核孔复合体——跨越核膜、允许 RNA 离开细胞核的大型通道。近一半核孔的构件显示出尾端长度改变并在丰度上下降,导致核表面核孔消失、RNA 在细胞核内堆积并出现 DNA 损伤的迹象。通过选择性删除单个核孔组件 Nup160 的长尾区,研究者可以模拟大部分 Nudt21 完全丧失的效应:核孔变得不稳定,遗传物质在细胞分裂时断裂,干细胞停止自我更新。在参与蛋白质合成和 RNA 加工的其他关键复合体中也观察到类似破坏,表明正确的尾端选择有助于协调这些大型机器的组装。
这对健康、衰老与癌症为何重要
对非专业读者而言,主要信息是:干细胞驱动的修复不仅取决于哪些基因被开启或关闭,也取决于它们的 RNA 讯息究竟如何被完成。Nudt21 像一个对剂量敏感的总调谐器,控制着这一完成步骤。将其稍微调低可以让干细胞继续分裂,但会将它们困在一种难以分化的不成熟状态——这种情形可能类似某些侵袭性癌症。将其调低过多则会导致核心细胞机器(如核孔)崩溃,进而引发 DNA 损伤并丧失再生能力。理解并最终控制这套 RNA 尾端切割机制,或许能开辟提升组织再生、在衰老过程中保护基因组稳定性或选择性促使癌细胞进入致死性停机的新途径。
引用: Tsopoulidis, N., Yagi, M., Brumbaugh, J. et al. Modulation of Nudt21 levels reveals dose-dependent roles of alternative polyadenylation in tissue regeneration. Nat Commun 17, 2005 (2026). https://doi.org/10.1038/s41467-026-68630-x
关键词: 干细胞, 组织再生, RNA 加工, 核孔复合体, 选择性聚腺苷酸化