Clear Sky Science · zh
G9a介导的H3K9me2通过对细胞周期相关基因的表观遗传沉默协调肠上皮再生
为何肠道自我修复至关重要
每天,你的肠道上皮都面临严苛环境:胃酸、食物颗粒和数以万亿计的微生物。然而这层组织不仅幸存下来,还在不断自我修复。当这种修复系统失灵——例如放疗后、炎症性肠病时或严重感染期间——人们会遭受疼痛、出血和危及生命的并发症。本研究揭示了肠细胞内一个隐秘的“开关”,帮助它们决定何时从静止状态切换到修复模式,为可能增强肠道自然修复能力的新疗法提供线索。
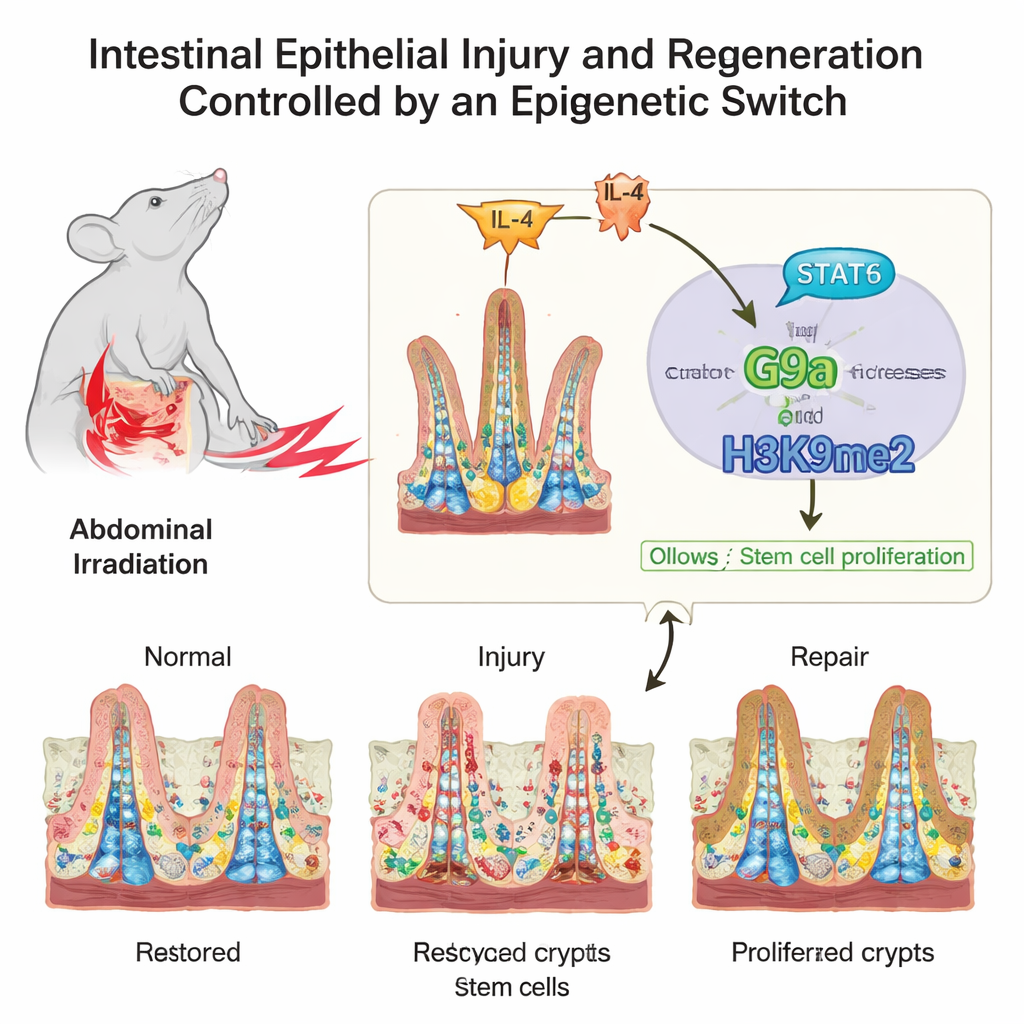
在持续压力下的精巧结构
在显微镜下,肠道内表面像一层绒毛地毯,指状的绒毛负责吸收营养,而称为隐窝的囊袋则是干细胞的栖息地。这些干细胞及其快速分裂的子代必须在稳定更新与应急修复之间取得平衡。作者关注的是包裹DNA的蛋白质——组蛋白上的化学标签如何影响这一平衡。这些标签并不改变基因序列,而更像调光开关,随着肠道从正常状态转入损伤再回到健康,它们对基因簇的开关起到调节作用。
一个随损伤与愈合变化的表观遗传标记
研究者在接受放射线照射的小鼠(放疗期间常见的肠道损伤原因)中扫描了多种组蛋白标记。在这些标记中,称为H3K9me2的标记在肠道从损伤转入修复时显著上升。其“写入”酶——名为G9a的蛋白也呈现相同模式。团队随后检查了来自接受盆腔放疗的患者以及克罗恩病患者的人类样本。在这两类样本中,肠上皮细胞中较高的H3K9me2和G9a水平与更好的组织修复迹象并存,提示这一机制在小鼠与人类之间是保守的。
当修复开关失灵时
为检验该标记是路人还是确实驱动愈合,科学家们在小鼠肠上皮中特异性删除了G9a,或用药物抑制其活性。两种情况下,H3K9me2水平均下降。放射或化学损伤后,这些缺乏G9a的小鼠体重下降更多,肠道更短、受损更严重,且再生隐窝与干细胞数量均低于正常动物。即便没有人为施加损伤,G9a缺失小鼠的肠上皮也呈发育受限:隐窝更浅、绒毛更短,干细胞及其分化后代数量均减少。由这些细胞在体外培养形成的迷你“肠样”结构也生长不良,进一步表明这一分子系统对肠道日常更新至关重要。
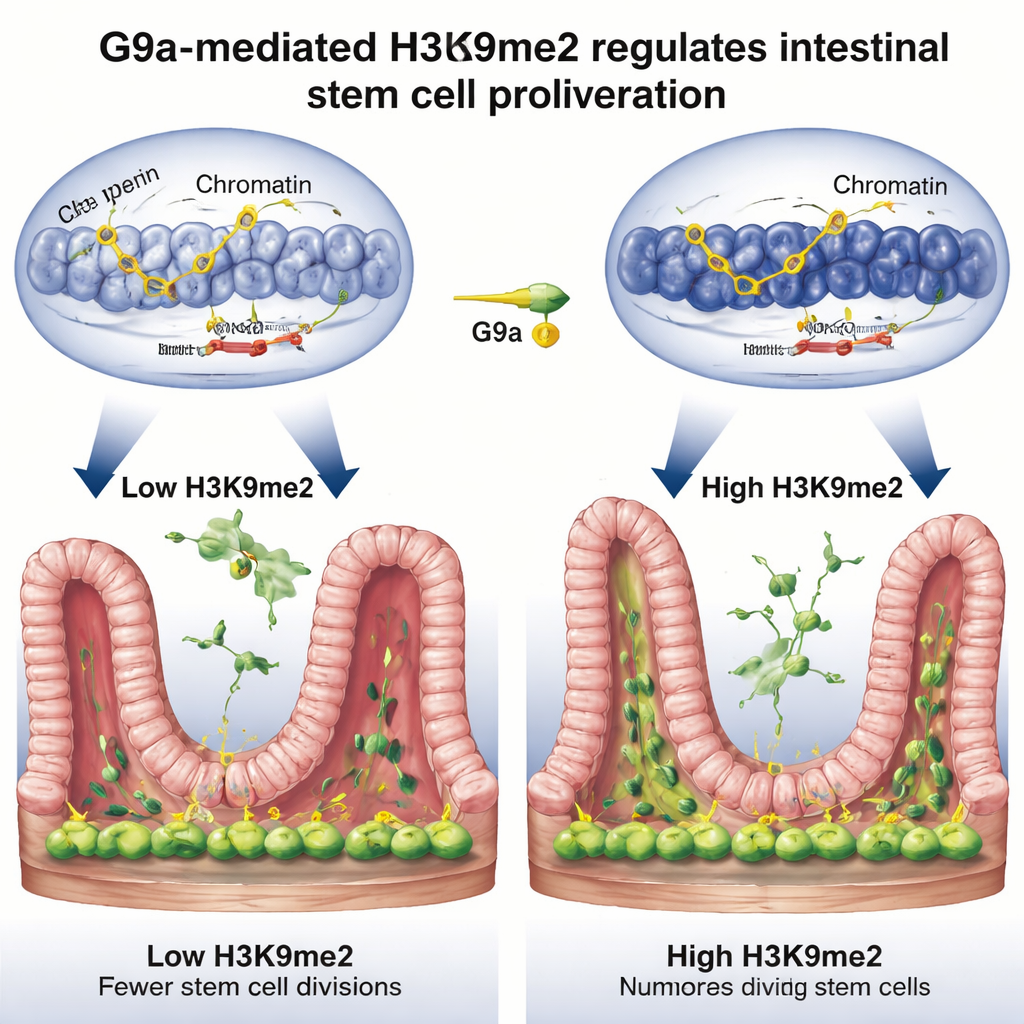
解除细胞分裂的刹车
深入分析后,团队探查了哪些基因受该修复开关控制。通过结合三种强大的全基因组手段,他们发现由G9a放置的H3K9me2倾向存在于通常作为细胞周期刹车的DNA区段上——例如Rb1cc1、Rb1、Cdkn1a和Pten等基因,这些基因减缓或阻止细胞分裂。当G9a缺失时,这些区域上的化学标记消失,周围的染色质变得开放,这些刹车基因的表达增强,导致干细胞增殖迟缓。在损伤后的正常修复过程中,这些基因位点的H3K9me2水平上升,基因活性下降,干细胞得以更自由地分裂并重建上皮。实质上,G9a和H3K9me2暂时压低“停止”信号,使组织能够再生。
从免疫信号到修复的信号链
肠道并非独自运作;它持续接收来自免疫系统的信号。研究者追溯到G9a上游的一个信号通路。损伤后,免疫信使IL‑4水平升高,触发肠细胞内STAT6蛋白的激活。被激活的STAT6直接结合G9a基因的调控区,提升其产量。由此形成一条指挥链:IL‑4激活STAT6,STAT6上调G9a,G9a添加H3K9me2以沉默细胞周期刹车基因,让干细胞扩增并修复受损上皮。
对未来治疗意味着什么
对非专业读者而言,这些发现表明肠道修复不仅受基因本身驱动,还受可逆的化学标记精细调控,这些标记决定基因何时被启用。IL‑4–STAT6–G9a–H3K9me2通路像一个内部控制面板,短暂放松干细胞分裂的刹车以完成修复,然后可被复位。未来,温和增强该通路的疗法——例如在适当时间和部位提高G9a水平的药物或基因工具——可能帮助患者更快地从放疗损伤、炎症性肠病发作或其他损伤肠上皮的情况中恢复,同时将失控细胞增生的风险降到最低。
引用: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
关键词: 肠道再生, 表观遗传学, 干细胞, 组蛋白甲基化, 炎症性肠病