Clear Sky Science · zh
WDR5 重塑 NANOG 浓缩体以驱动转录程序并维持干细胞身份
这对干细胞与癌症为何重要
干细胞具有分化为多种细胞类型的非凡能力,这一特性推动了早期发育、组织修复,同时在某些癌症中也被滥用。本研究揭示了两个关键蛋白——NANOG 与 WDR5——如何协同维持干细胞的可塑状态。研究表明 WDR5 能在物理上重塑 NANOG 在 DNA 上的聚集方式,把细胞核内蛋白质“液滴”的物理学与健康干细胞及白血病中基因的调控联系起来。
决定细胞命运的蛋白质
胚胎干细胞能保持多能性,即能够分化为几乎任何细胞,这要归功于像 NANOG、OCT4 和 SOX2 这样的主调控因子。这些蛋白质控制着整个基因网络的开关。NANOG 尤为核心:它不仅结合 DNA,还招募大型酶复合体在组蛋白上添加激活性化学标记,而组蛋白是包装 DNA 的蛋白。WDR5 是另一个关键因子,帮助组蛋白修饰复合体放置表示基因活性的信息标记。尽管已知 NANOG 与 WDR5 都支持干细胞身份,但它们在分子水平上如何相互作用,以及这种相互作用是否影响它们在细胞核中形成微小液滴或“浓缩体”的方式,尚不清楚。
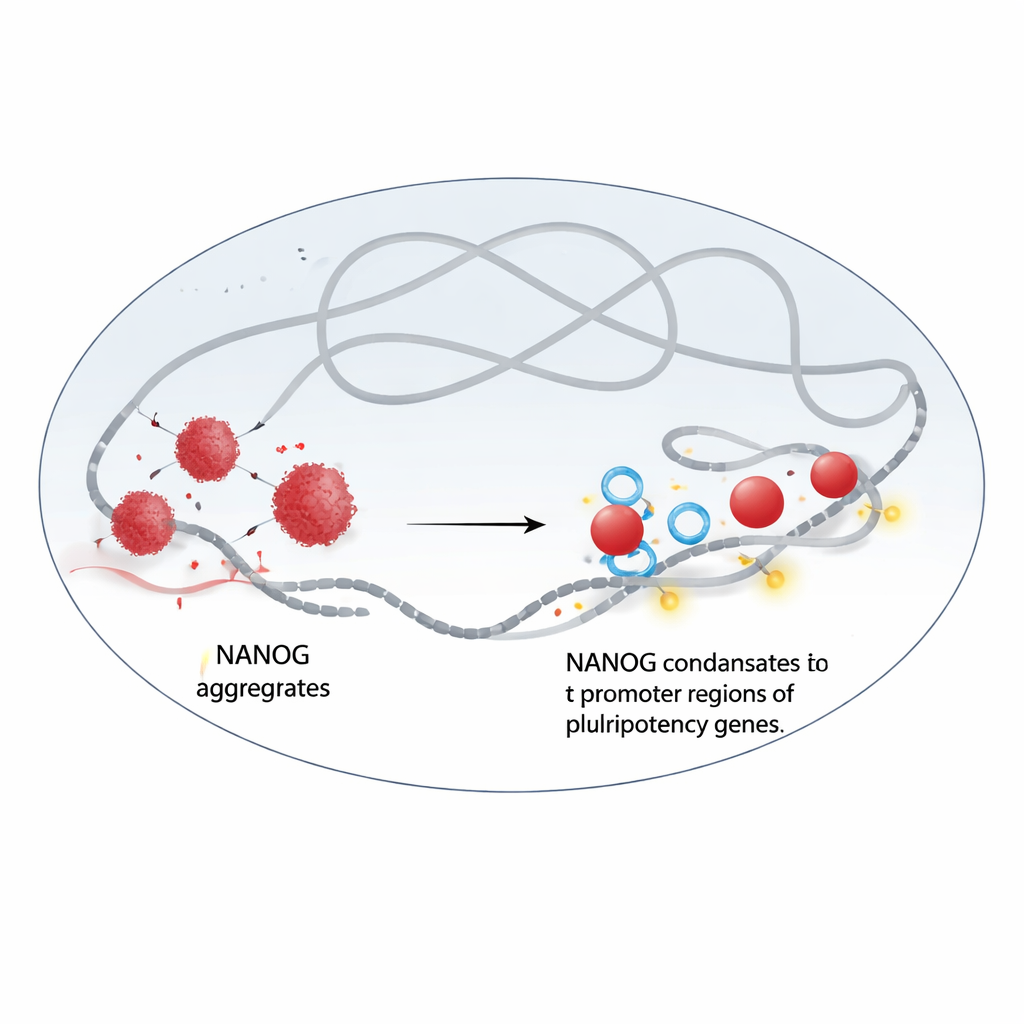
从团块到液滴
作者发现 NANOG 与 WDR5 直接相互作用。当单独纯化时,NANOG 倾向于形成不规则的、类固体的聚集体。通过电子显微镜和荧光实验,团队表明加入 WDR5 会将这些聚集体重组为圆形、类似液体的液滴,表现为动态浓缩体。在活细胞中,NANOG 与 WDR5 在明亮的核内点状结构中共聚,当用一种已知能破坏液–液相分离的化学物质处理时,这些点状结构迅速溶解。发生这种情况时,两者对染色质——存储遗传信息的 DNA–蛋白复合体——的结合显著下降,并且它们在关键多能性基因处的存在明显减少。
一种特殊的分子“握手”
为了解这种伙伴关系的原子细节,研究者解析了 NANOG 的 DNA 结合区与 WDR5 结合的晶体结构。与许多其他 WDR5 结合者使用短柔性回路不同,NANOG 通过一个延伸的表面与 WDR5 结合,该表面包括一个无固定结构的臂和附近的螺旋。NANOG 位于 153 位的一个精氨酸侧链深入插入 WDR5 的中央通道,形成“锁与钥匙”相互作用的关键部分。将该残基突变为丙氨酸(R153A 突变)会在很大程度上消除结合。重要的是,突变的 NANOG 仍能结合 DNA,但 WDR5 无法高效地将其聚集体重构为流动性液滴,表明这一特定接触对形成功能性浓缩体至关重要。
维持干细胞“青春”——以及失败时的后果
当作者将小鼠胚胎干细胞改造为仅表达 NANOG R153A 突变体时,后果十分显著。突变细胞失去了典型多能细胞的紧密穹状集落,变得扁平,这是分化的视觉标志。它们形成的碱性磷酸酶阳性集落减少(这是干性的一项标志),并且许多核心多能基因(如 Nanog 本身、Sox2、Esrrb 和 Klf4)表达下调。同时,与特定谱系相关的基因,包括骨与发育调控基因,被激活。全基因组分析显示 NANOG 与 WDR5 不再在数千个启动子处共同占位,两种关键的活化性组蛋白标记 H3K4me3 和 H4K16ac 在这些共有位点上特异性丧失。在分化早期,这些化学标记和新合成的 RNA 转录本率先下降,早于总体 mRNA 水平的下降,显示出主要是活性染色质维持的失败。
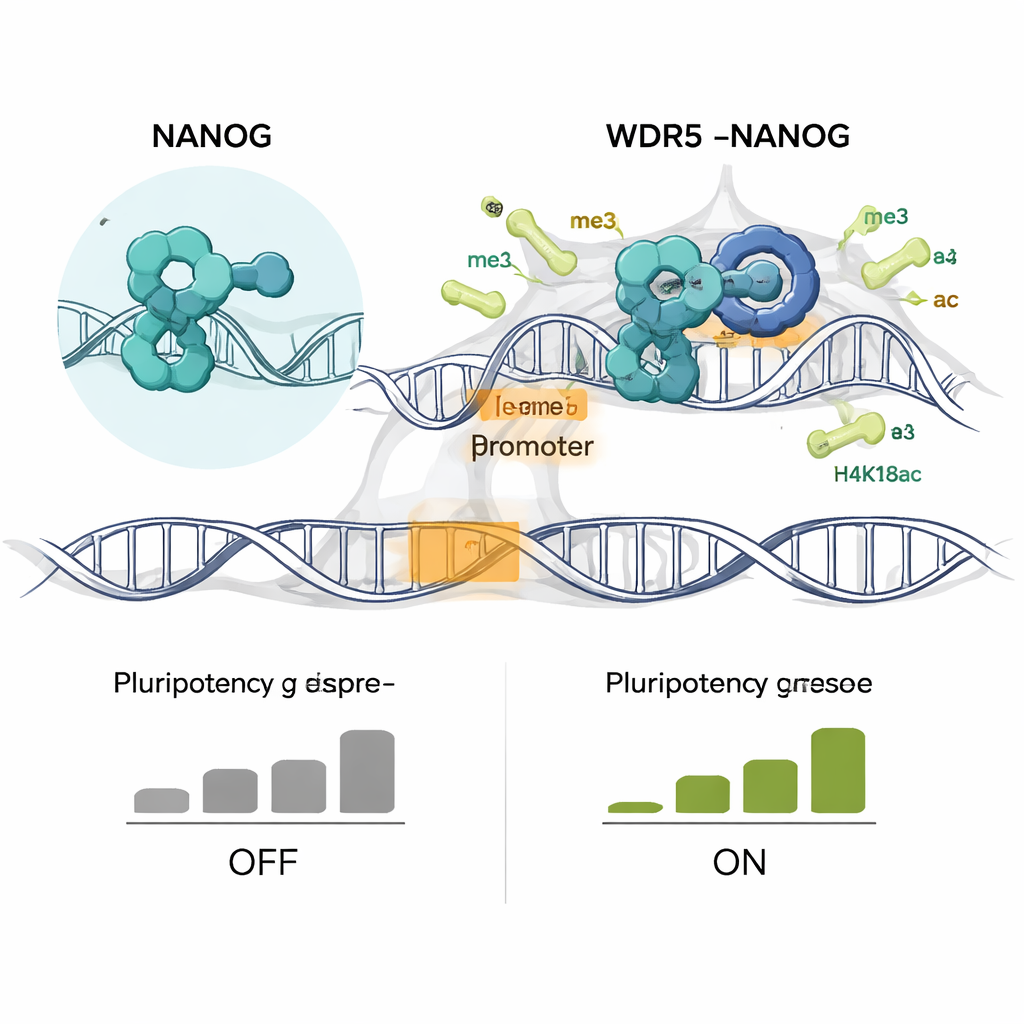
将一个基本机制转化为癌症策略
由于类似的基因网络驱动某些癌症干细胞,团队测试了破坏 NANOG–WDR5 轴是否能抑制急性髓性白血病小鼠模型中的白血病干细胞。小分子药物 C16 能结合 WDR5 的同一口袋,该口袋被 NANOG 利用,因此选择性削弱了 WDR5–NANOG 相互作用。在白血病细胞中,C16 显著减少了克隆形成,耗竭了类干细胞群体,并推动细胞向成熟的髓系命运分化,而对正常造血干细胞的影响远小于一种针对 WDR5 另一结合伙伴的现有白血病药物。RNA 测序显示 C16 关闭了与干性和自我更新相关的基因程序,并增强了分化通路。在小鼠体内,C16 治疗减少了白血病干细胞和祖细胞群体,强调了靶向该蛋白伙伴关系的治疗潜力。
宏观意义:液滴如何决定细胞身份
这项工作揭示了 WDR5 不仅仅是位于染色质上招募酶:它还能在物理上将 NANOG 从惰性聚集体重塑为柔性的液体浓缩体,这些浓缩体驻留在多能性基因的启动子上并吸引激活性组蛋白标记。当这种重塑被阻断——无论是通过 NANOG 的精确突变还是通过破坏它们接触的小分子——干细胞会失去其身份,癌症干细胞会丧失自我更新的能力。对于普通读者来说,关键信息是:蛋白质在 DNA 上组装成液滴的微小变化,可能对细胞保持“年轻”与可塑、走向特定命运或促成疾病具有深远影响。
引用: Wang, D., Shi, X., Xie, J. et al. WDR5 remodels NANOG condensates to drive transcriptional programs and sustain stem cell identity. Nat Commun 17, 1907 (2026). https://doi.org/10.1038/s41467-026-68623-w
关键词: 干细胞多能性, NANOG, WDR5, 相分离, 白血病干细胞