Clear Sky Science · zh
首次与多胎乳腺腺体衰老分歧揭示 IL33+ 混合上皮细胞
妊娠如何重塑终生乳腺癌风险
为什么早育能降低女性终生罹患乳腺癌的风险,而单纯变老却会增加风险?这项研究利用小鼠追踪乳腺细胞“生态系统”随时间的变化,对比从未妊娠的动物与曾经历妊娠的动物。通过观察单个细胞随年龄和生育状况的演变,研究者发现了一类罕见且会变形的细胞类型,这或许有助解释妊娠对乳腺癌长期保护作用的机制。
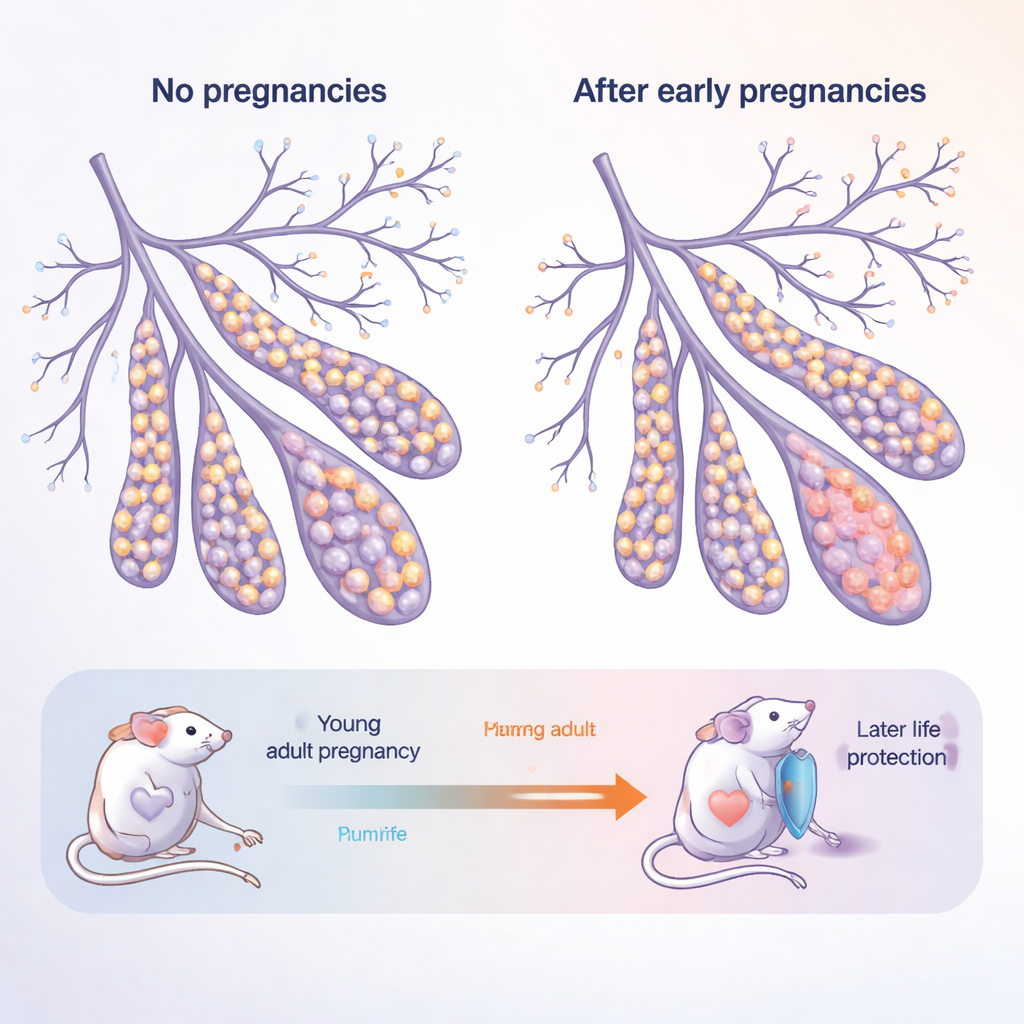
作为活体、可变组织的乳腺
乳腺不是静止器官:在青春期、妊娠期以及泌乳终止后都会发生显著生长和重塑。它由两层主要的上皮细胞构成,衬里导管:内层“腔道(luminal)”细胞接触乳汁和激素,外层“基底(basal)”细胞提供结构并包含类干细胞。作者研究了既有青年成年小鼠,也有老年“绝经后样”小鼠,每组又分为从未妊娠(初产)或经历过多次妊娠(经产)。这一设计模拟了在二十多岁生育然后步入五十岁及以后的女性情形。
衰老与妊娠如何将组织拉向不同方向
随着从未妊娠的小鼠变老,其乳腺向基底细胞比例增加而腔道细胞减少。这些年长、从未妊娠的腺体还产生了更多类器官——由单个细胞在三维培养中生长出的微型结构——表明其细胞异常地倾向于增殖。相反,经历过妊娠的小鼠显示出一种“归一化”的平衡:与年龄相关的基底细胞激增被抑制,且其细胞形成的类器官更少。这表明妊娠留下了持久印记,既改变了细胞命运选择,也收敛了它们的再生能力和潜在的致癌风险。
混合、可变形细胞的发现
为更深入地观察,团队使用单细胞 RNA 测序读取数千个单个乳腺细胞的基因表达。在预期的腔道、基底、免疫和基质细胞之外,他们发现了一小群既不完全属于任一主要层次的细胞。这些细胞同时表达腔道与基底谱系的标记,于是被称为“混合”上皮细胞。显著的是,这类混合细胞在从未妊娠的小鼠中随年龄积累,而在同龄已妊娠的小鼠中则远少见。混合细胞强烈表达名为 Il33 的基因,该基因编码信号分子 IL-33,并伴随表达与早期发育阶段和高度可塑性相关的标记——即能够切换身份或行为的能力。
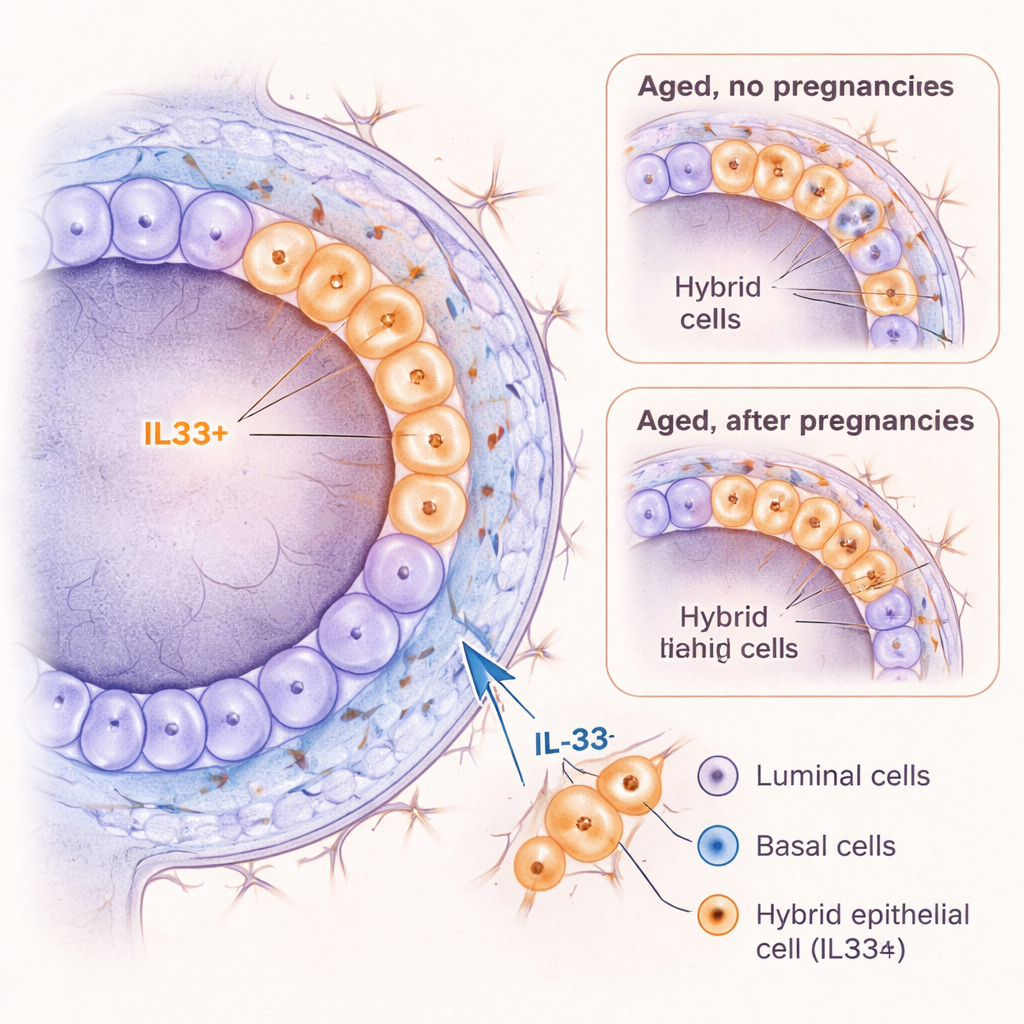
IL‑33 作为不良细胞状态的驱动因子
鉴于 IL‑33 在其他器官中与炎症和癌症有关,研究者探问其是否能主动促使乳腺细胞进入类似混合的状态。当他们在三维培养中用 IL‑33 处理幼年小鼠乳腺细胞时,基底层细胞形成了更多类器官,保持了更原始的身份,并产生了更多带有混合标记 KRT6A 的细胞。在活体幼鼠中,短期注射 IL‑33 导致导管扩张并触发一次细胞分裂高峰,同时出现 KRT6A 阳性混合细胞的暂时增加以及向更基底样细胞的转变。重要的是,当细胞携带与癌症相关的突变(如抑癌基因 Trp53 的丢失)时,IL‑33 进一步促进了它们的生长。综合来看,这些发现表明 IL‑33 有助于营造一种高度可塑且易增殖的细胞状态,这种状态在转变为癌细胞时可能特别脆弱。
来自人类乳腺组织的线索
为检验类似细胞在人类中是否存在,作者重新分析了几项来自正常人乳腺组织的大型单细胞数据集。他们鉴定出一小群人类上皮细胞,类似于小鼠的混合细胞,既显示腔道又带有基底特征,并表达 IL33 及相关基因。多个数据集中 IL33 阳性细胞随年龄变得更常见。在体外培养的原代人乳腺细胞中,IL‑33 处理增加了类器官形成、将细胞推向更基底样的表型,并富集了 CD44 阳性细胞——这是在乳腺癌中常与未成熟、类干样细胞相关的标记。尽管现有的人类样本不足以清晰检验早期妊娠如何改变该群体,但与小鼠的相似之处颇为引人注目。
这对理解乳腺癌保护意味着什么
对普通读者而言,核心信息是妊娠似乎重新布线了乳腺组织的衰老方式。在小鼠中,早期妊娠阻止了富含 IL‑33 的混合细胞累积,这类细胞模糊了乳腺主要细胞层之间的界限,并表现出高度可塑、准备好增殖的行为。IL‑33 本身可以将细胞推向这种具有风险的可变状态,尤其在存在与癌症相关的突变时更是如此。通过减少这些混合细胞的数量或持久性,妊娠可能降低了老化乳腺组织在不利时刻含有“错误”细胞——即更容易演变为癌症的细胞的几率。这一机制性见解最终可能指导出模拟早期妊娠保护作用的策略,而无需真正经历妊娠。
引用: Olander, A., Medina, P., Haro Acosta, V. et al. Divergent aging of nulliparous and parous mammary glands reveals IL33+ hybrid epithelial cells. Nat Commun 17, 1898 (2026). https://doi.org/10.1038/s41467-026-68611-0
关键词: 乳腺衰老, 妊娠与乳腺癌, 乳腺干细胞, IL-33 信号, 混合上皮细胞