Clear Sky Science · zh
配体控制的区域可逆与手性选择性 C–H 氰化反应用于二级胺
为何微小键位的改变对重要药物至关重要
许多畅销药物含有一种小型含氮骨架单元,称为胺。围绕这些胺原子键合方式的细微变化,可能把一种疗效较弱的药物变成强效且精确的治疗剂——也可能使其失活或变得有害。本文介绍了一种新的方法,可随心所欲地修饰这些胺骨架,让化学家精确选择分子上发生反应的位置以及生成哪种镜像形式(手性),两者对于设计更安全、更有效的药物都至关重要。
在拥挤分子上选定一个位置
药物中的胺通常含有若干非常相似的碳–氢(C–H)键,这些键通常表现得几乎相同。化学家希望仅把其中一个氢替换为有用的基团,例如“氰基”(–CN),而不干扰分子其余部分。这很困难,因为标准反应往往按分子本身决定的最活泼位点发生,而不是由化学家选择。在此工作中,作者使用简单且柔性的二级胺,这些胺在氮上带有两条不同的碳链。他们展示了从相同的胺出发,仅通过改变包围铜催化剂的配体,就可以把反应引导到两个相邻位置中的一个——要么靠近小的 N‑甲基基团(所谓的 α′ 位),要么在另一条链上更远一个碳原子处(β 位)。
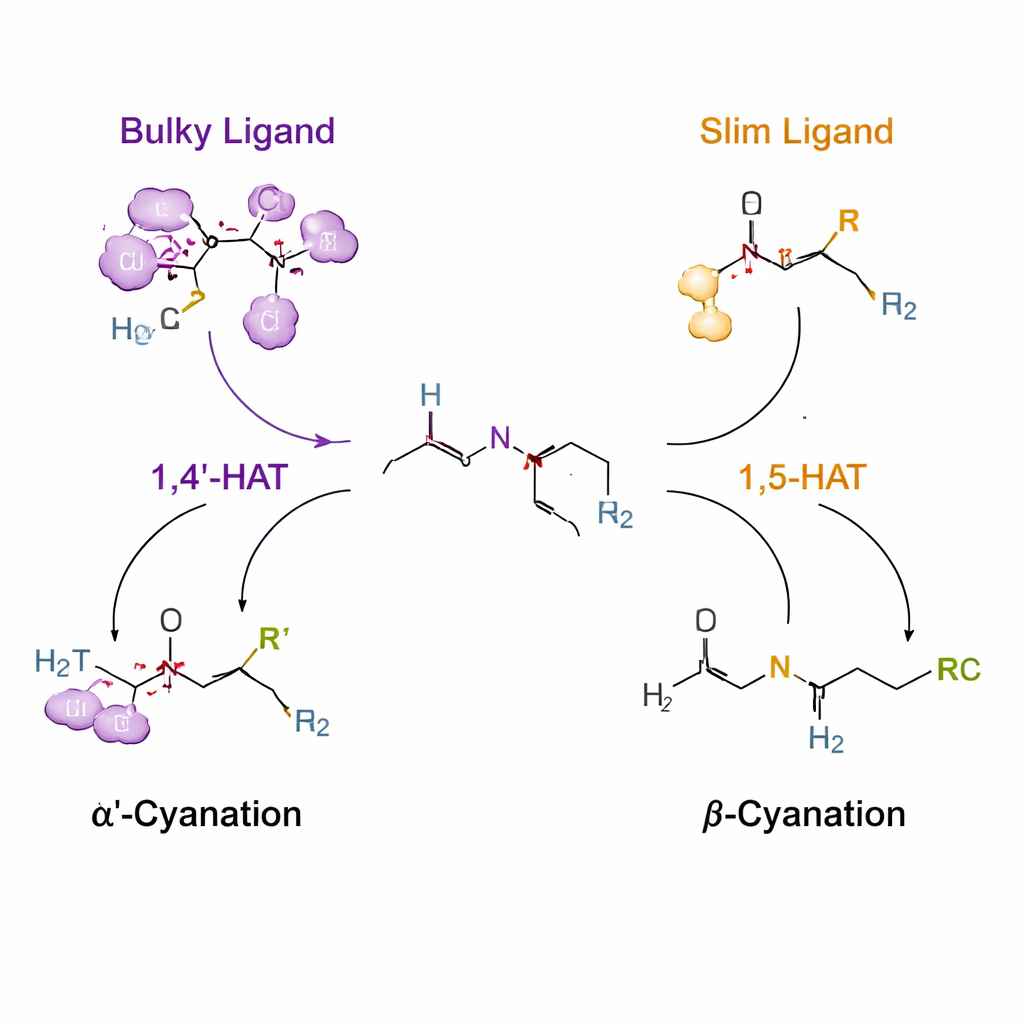
利用受控氢“跳跃”来引导反应活性
关键策略依赖于一种称为氢原子转移的过程,其中短寿命的以氮为中心的自由基从邻近的碳上抽取氢。通常,此类自由基倾向于一定距离,偏好一种六元“可及”方式,称为 1,5‑HAT。作者在胺上引入一个暂时的脲基和氯把手,使得在铜催化下可形成该氮自由基并可从 α′ 或 β 位抽取氢。通过设计配体——包裹铜的有机分子——他们改变了自由基的环境。非常体积庞大的配体(命名为 L14)会把体系推向一种不寻常的 1,4′‑HAT 步骤,定位于 N‑甲基,从而选择性地得到 α′‑氰化产物。较纤细的配体(如 L8)则允许传统的 1,5‑HAT 路径,将反应引导到 β 位。
从位点控制到手性控制
除了选择反应位置,团队还追求对手性的控制,这一点至关重要,因为许多药物以左旋或右旋形式存在,在体内表现不同。为实现这一点,他们将手性配体——自身具有手性形状的分子——引入铜配合物。两个这样的配体 L24 和 L41,在把氰基引入 β 位时(包括苄位(邻近芳环)和烯丙位(邻近碳–碳双键))能高选择性地偏好生成一种镜像体。在广泛的胺起始物上,该方法能以优异的位点选择性和手性选择性得到 β‑氰化产物,并可在克级规模上进行,表明该工艺在合成上实用且稳健。
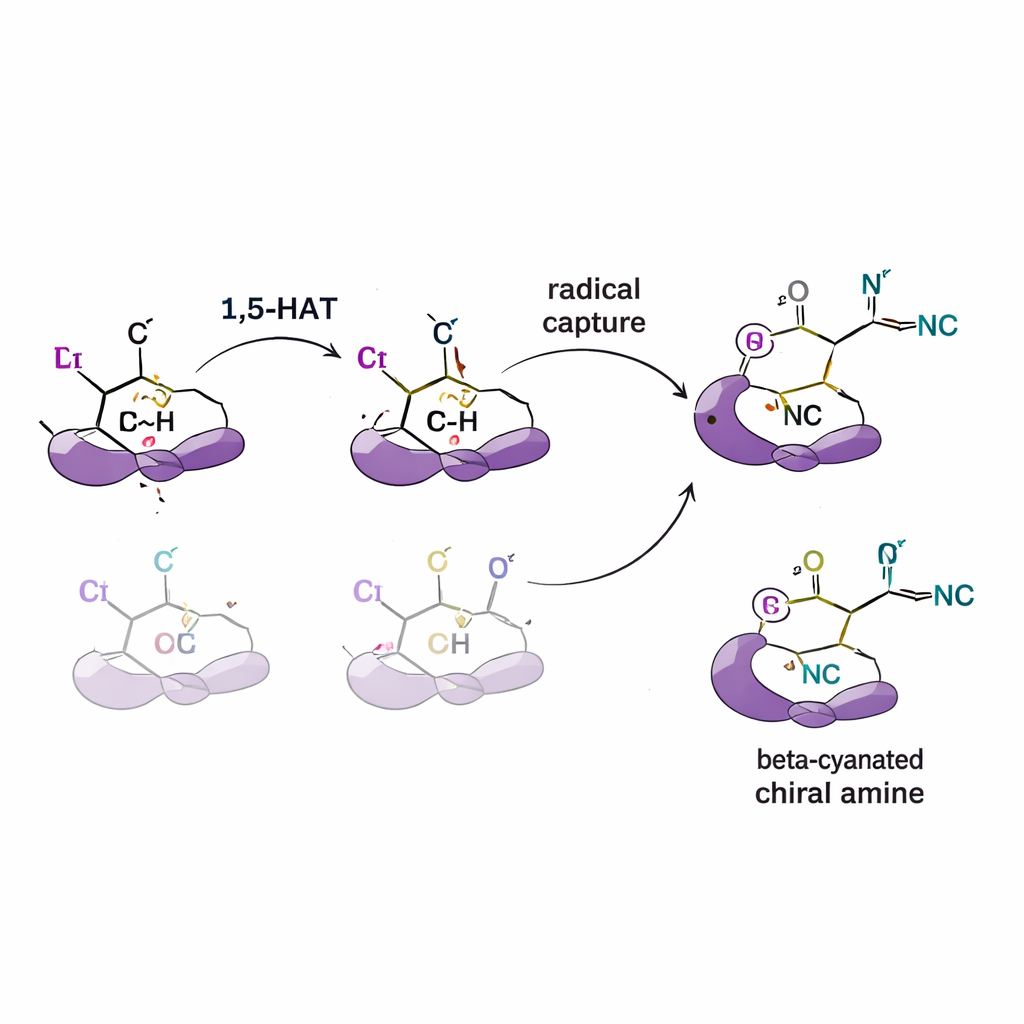
检验选择性背后的机理
为弄清这种控制如何产生,作者进行了一系列机理学实验。通过加入自由基“捕捉剂”,他们确认确实存在反应性的自由基中间体。使用将某些氢替换为氘(氢的较重同位素)的底物,他们检测到动力学同位素效应,指示氢转移步骤是较慢的、决定选择性的步骤。示踪实验也显示氢是以单向的、一步的方式迁移,而非在位点间来回穿梭。互补的计算模拟(密度泛函理论)支持这些发现,表明配体的形状与体积改变了竞争性氢转移通路的能量以及随后自由基与铜和氰根结合以生成优选镜像体的方式。
对未来药物设计的意义
总体而言,这项工作引入了一种灵活策略,能够按需在两个密切相关的位置对常见胺基团进行重构,并对分子手性进行细致控制。化学家仅通过更换铜催化剂上的配体,就能选择将氰基安置在小的 N‑甲基单元上或放在另一侧链的邻位碳上,并能在许多复杂且类似药物的分子中实现。由于氰基是通往许多其他官能团的重要中间体,这种“选位即拨”和“选手性即拨”的方法将有助于更容易地探索并优化由相同基础胺骨架构建的新药物。
引用: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
关键词: 胺官能化, 氢原子搬运, 铜催化, 手性选择性氰化, 药物化学