Clear Sky Science · zh
一种高度动态的单核非血红素铁酶用于两步异腈生物合成
细菌如何构建奇特的化学工具
异腈是体积小却功能强大的化学基团,像瑞士军刀一样多用:它们能抓取金属、参与多种反应,并常作为强效天然抗生素和毒素的“弹头”。一些致病细菌,包括结核病病原体结核分枝杆菌,会把异腈连接到脂类分子上,以帮助从宿主体内夺取金属。本文探讨它们的一种酶——Rv0097——如何在两个精心编排的步骤中完成这项异常苛刻的化学转变。
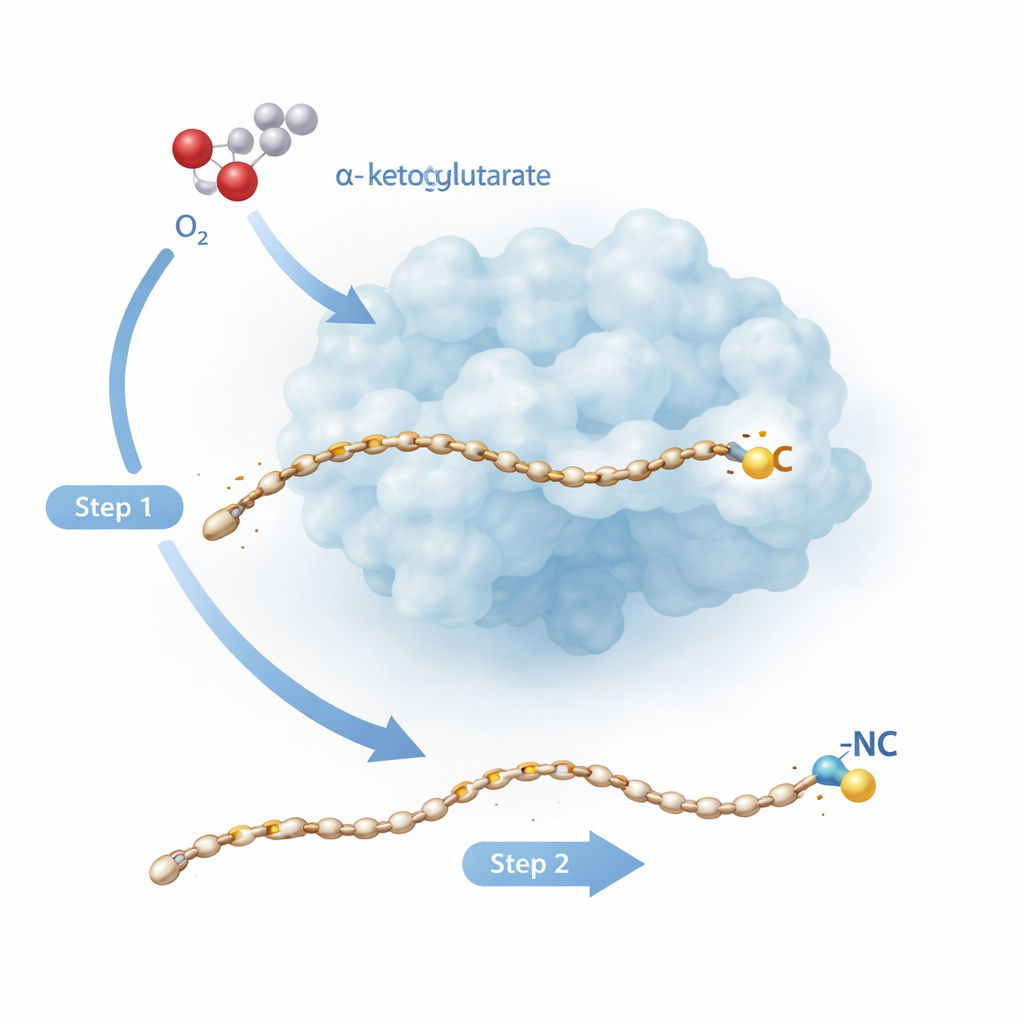
一个两步的分子改造
Rv0097 属于一大家族依赖铁的酶,这些酶通常执行较简单的任务,比如在分子上的单个位点引入氧。在这里,任务更艰难:以“甘氨酰–脂肪酸”构件为起点,酶必须构建一个全新的异腈官能团,其关键的两个原子——碳和氮——都来自相同的小片段甘氨酸。对相关酶 ScoE 的早期研究表明,这不能在一次反应中完成。取而代之的是需要两个独立的反应“半循环”,每个由酶在撕裂辅助分子α-酮戊二酸并与空气中的氧结合时产生的铁–氧种驱动。新的研究转向结核酶 Rv0097,以原子分辨率观察酶如何在同一底物上将这两步自由基反应串联起来而不失控。
将酶在反应中“冷冻”
研究人员使用 X 射线晶体学捕捉了 Rv0097 在不同状态下的十六个高分辨率快照:空状态、与其脂类底物(一个十碳分子称为 CADA)结合、与α-酮戊二酸结合,以及模拟短暂反应中间体的多种组合。这些结构显示 Rv0097 具有分裂的性格。处于静止时,其活性位点大多是封闭的,一个关键氨基酸(苯丙氨酸102)在两种取向之间翻转,保持长脂尾口袋干燥并为疏水结合做好准备。当 CADA 结合时,该残基会定格为单一取向,底物的极性“头部”由带电侧链锚定,而油性尾部则嵌入一个紧密的通道。对这一门控残基对(F102 与附近的甘氨酸 G204)进行突变,要么堵塞口袋,要么让过多水分进入,都会显著降低活性并改变酶偏好的脂链长度。
移动的盖子与动态环
在底物口袋之外,Rv0097 表现得像一个带有可动门的小型机械。团队观察到“打开”和“关闭”的构象,在这些构象中,两段如盖般的区域围绕活性位点分开或合拢。打开时暴露出铁中心并为α-酮戊二酸和底物进入创造通道;关闭时在反应进行时将化学过程与周围水环境隔离。两个柔性的表面环,按其携带的组氨酸和精氨酸分别称为His环和Arg环,作为额外门控。在一些结构中,这些环向内摆动,使精氨酸残基能够抓住α-酮戊二酸;在另一些结构中它们向外摆动,显然形成一条侧通道,借此消耗掉的辅助片段(琥珀酸和二氧化碳)可以离开,而新的α-酮戊二酸可以进入以进行第二步——同时由底物衍生的中间体保持被夹在位。
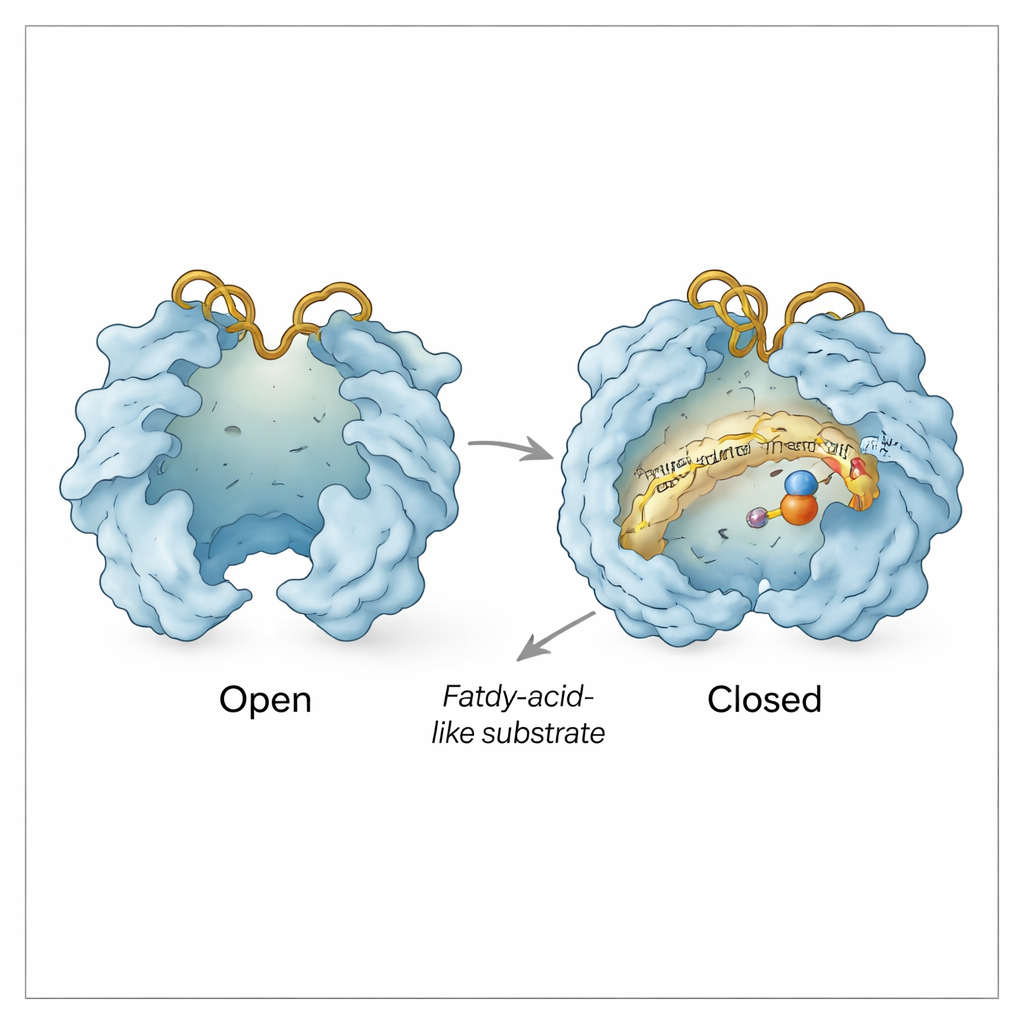
保护脆弱的中间体
生化测定支持这一结构图景。反应的第一半将 CADA 转化为高度活泼的亚胺中间体,该中间体若逸散到溶液中会迅速崩解。通过化学捕获其分解产物,作者表明大部分此类中间体仅在酶仍在场时被检测到,暗示它在两次半反应之间保持与 Rv0097 结合并受到保护。结构揭示了其机制:His 和 Arg 环的细微重新定位,连同附近残基的小幅移动,似乎将中间体封入一个受保护的腔室,同时仍允许像α-酮戊二酸、琥珀酸和二氧化碳这样的小分子通过受控通道进行交换。
这对结核病及更广泛领域的重要性
综上,这些结果将 Rv0097 描述为一个高度动态的单蛋白装配线,它在同一底物上连续两次使用基于铁的化学反应而从不释放危险的半成品。对于结核分枝杆菌来说,这种精确性支撑着异腈装饰分子的合成,帮助它们在体内获得必需金属;遗传学研究表明该途径在感染期间对其存活很重要。对化学家和药物设计者而言,这项工作为工程相关酶以构建新的含异腈化合物提供了蓝图,并提示干扰 Rv0097 的可动盖与门控可能成为开发新型抗生素的一条途径。
引用: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
关键词: 异腈生物合成, 非血红素铁酶, 结核分枝杆菌, 酶动力学, 金属螯合天然产物