Clear Sky Science · zh
破坏铁稳态使胰腺癌对不可逆电穿孔更敏感
将电与铁转向对抗致命癌症
胰腺癌是最难治疗的癌症之一,即便是激进的局部疗法也常常无法阻止其复发。本研究探讨了一种让现有手段——不可逆电穿孔(用短促强劲的电脉冲杀死肿瘤)——更有效且更安全的新方法。通过巧妙干扰癌细胞处理铁的方式,研究者展示了如何将存活细胞推入一种破坏性的死亡形式,从而潜在地降低肿瘤复发的几率。
为什么仅靠电脉冲并不够
不可逆电穿孔(IRE)通过在肿瘤内或周围插入细电极并发射快速高压脉冲来治疗肿瘤。这些脉冲在细胞膜上打出永久孔洞,杀死许多癌细胞并引发免疫反应。但电场并非完全均匀。接受到稍弱脉冲的区域可能留下存活的癌细胞,而这些幸存者能够播散并形成新肿瘤。团队在暴露于亚致死电场的胰腺癌细胞和小鼠肿瘤中仔细观察时发现,这些细胞并没有通过依赖铁的铁死亡而死亡,反而开启了广泛的抗氧化防御程序。包括帮助中和铁相关损伤的关键保护基因在内的基因表达上调,使细胞得以抵御打击并恢复。
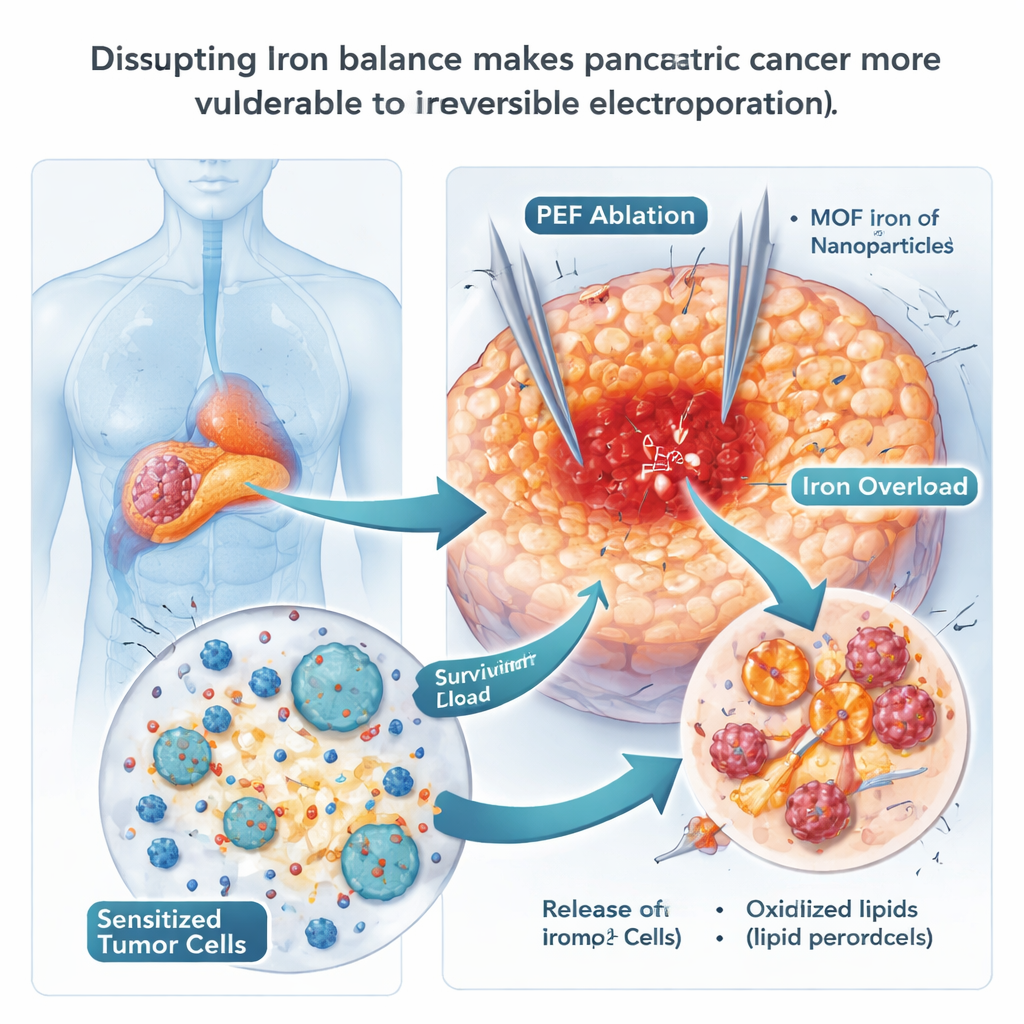
用铁纳米粒子推动细胞走向自毁
因为铁死亡依赖铁,科学家们测试了富铁纳米粒子是否能将癌细胞逼入绝境。他们使用了特殊设计的含铁金属有机框架颗粒(MOF-Fe),这些颗粒在细胞的酸性区室内能快速释放铁。在培养皿中,摄取这些颗粒的胰腺癌细胞积累了游离铁并在膜脂中出现氧化,这些都是铁死亡的典型特征,且形成的菌落大大减少。在小鼠中,将 MOF-Fe 与 IRE 结合比单独任一治疗更能延迟肿瘤再生,且肿瘤表现出更多氧化损伤的迹象。然而,这种益处是暂时的:大约三周后,肿瘤开始反弹,表明癌细胞找到了适应铁超载的方法。
瞄准细胞的“铁保险柜”
为了解释这种耐受性,团队分析了 MOF-Fe 处理后发生变化的蛋白质。其中一个显著的蛋白是重链铁蛋白 1(FTH1),它是细胞铁储存复合体的一部分——相当于分子层面的防火保险柜,用来存放多余的铁。当实验性地提高 FTH1 水平时,癌细胞对铁死亡的抵抗能力增强;当降低 FTH1 时,细胞则变得更易感。这指向了 FTH1 作为抵御铁驱动性死亡的核心保护屏障。研究者随后设计出一种分子 C20U4V,由花生四烯酸(一种高度可氧化的脂肪)连接到一种“PROTAC”脚手架上,PROTAC 可以将特定蛋白引导到细胞的降解机器。在 MOF-Fe 存在时,C20U4V 结合铁蛋白并招募其被标记并降解,显著降低了 FTH1 水平,阻止细胞将铁安全封存。
从细胞培养到微型肿瘤与小鼠模型
当 MOF-Fe 与 C20U4V 联合使用时,胰腺癌细胞显示出更高的氧化应激、更多受损的膜脂、线粒体健康受损,以及显著降低的再生能力。这种协同效应在三维的患者来源类器官中也很明显——这些由真实患者培养的微小类肿瘤结构在药物组合作用下体积和数量都崩溃。由于 C20U4V 是疏油性的且不溶于水,团队将其封装到对活性氧敏感的微胶束(M-C20U4V)中,这些微胶束可在血流中循环并在受损、应激的肿瘤组织中释放药物。在皮下和胰腺内种植肿瘤的小鼠模型中,IRE、MOF-Fe 与 M-C20U4V 的三联组合比任何单独或双联疗法都更能缩小肿瘤并延长生存期。处理后的肿瘤显示出较少的分裂细胞、更多铁死亡标志物以及更多 T 细胞和其他免疫细胞浸润,表明该策略不仅直接杀死癌细胞,还帮助免疫系统识别并攻击肿瘤。
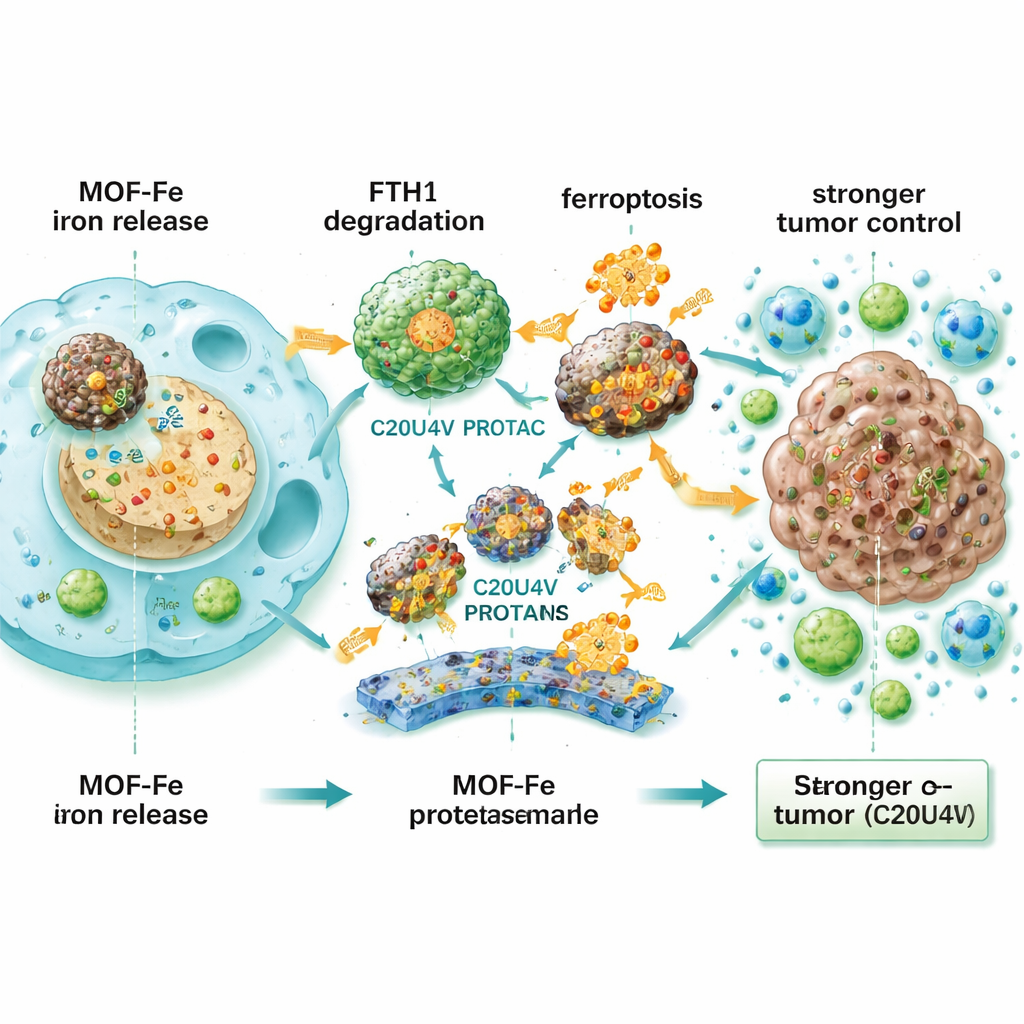
这对患者意味着什么
对非专业读者来说,关键思想很简单:胰腺肿瘤在电脉冲消融后常常会逃逸,因为部分癌细胞存活并迅速适应。这项工作表明,通过给这些细胞加载铁并同时禁用它们的“铁保险柜”,可以将它们逼入一种难以抵抗的自我毁灭状态。尽管该方法仍处于实验阶段,并需在人体中进行广泛的安全性和可行性测试,但这表明,通过微调肿瘤处理铁这一基本元素的方式,可能将一种不完美的局部治疗转变为对抗这种最致命癌症之一的更有力一击。
引用: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
关键词: 胰腺癌, 不可逆电穿孔, 铁死亡, 铁纳米粒子, PROTAC 治疗