Clear Sky Science · zh
人体1型先天淋巴细胞控制白血病干细胞分化并限制急性髓性白血病发展
为什么我们自身的免疫细胞在白血病中很重要
急性髓性白血病(AML)是一种侵袭性的血液癌,即使经过强烈化疗也常常复发。一个关键原因是存在一小群“起始”白血病细胞,能够重新启动疾病。这项研究表明,免疫系统中一个不太为人所知的分支—1型先天淋巴细胞(ILC1s)—能够将这些起始细胞推离危险的增殖路径,并在实验模型中帮助减缓白血病进展。研究还描绘了一个可能的途径,可将捐赠的脐带血制造成有益的ILC1s,作为未来的治疗手段。
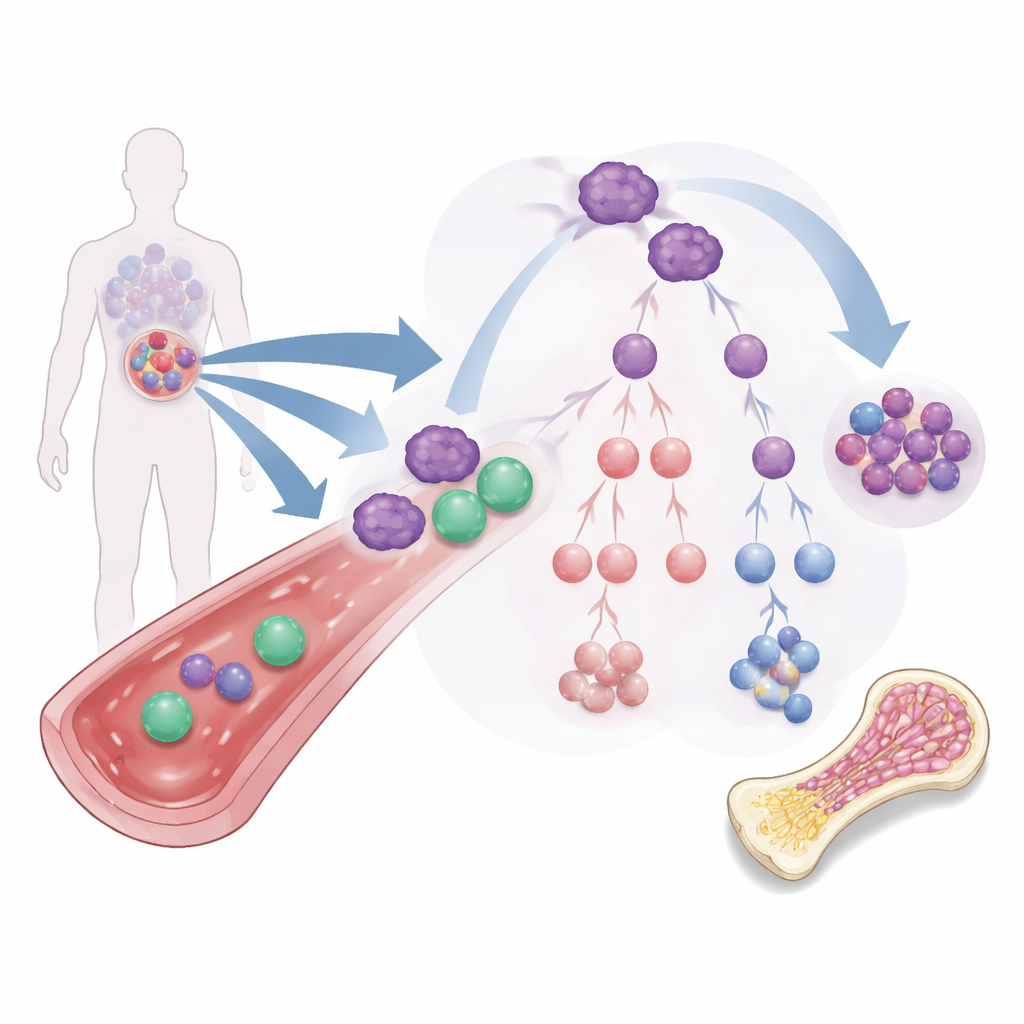
难缠的白血病起始细胞问题
大多数AML疗法针对在血液和骨髓中循环的白血病细胞大军。但更罕见的一小部分,被称为白血病干细胞,更像种子:它们能自我更新、抵抗常规药物并重新播种癌症。这些细胞可以沿多个分支成熟为不同类型的白血病细胞,其中一些仍保有自我更新能力或能保护癌细胞免受免疫系统攻击。正因为这种分支式的“家谱”,仅仅缩小可见的白血病并不足够;疗法必须改变这些起始细胞的命运或将其完全清除。
患者中缺失的一道防线
ILC1s是快速反应的免疫细胞,不需要事先暴露即可识别威胁。研究人员比较了健康志愿者与AML患者血液中的ILC1s,发现患者的ILC1s总体较少,且功能较弱。通过单细胞RNA测序和流式细胞术,团队显示患者的ILC1s产生较低水平的关键杀伤分子和重要免疫信号,且表面激活受体较少。值得注意的是,ILC1s比例较高的患者通常白血病原细胞较少,这提示当这些细胞存在且功能正常时,它们有助于抑制疾病。
健康ILC1s如何将白血病细胞引离有害路径
为了解ILC1s对白血病干细胞的实际影响,团队在实验室中将二者共同培养。来自健康供体的ILC1s并不是简单地消灭干细胞;相反,它们改变了这些细胞的成熟方向。一种ILC1信号TNFα将干细胞推入一种中间状态,并减少它们向更危险、快速分裂的白血病细胞转化的比例。它还抑制了干细胞转变为类巨噬细胞(这些细胞通常抑制免疫反应并扶持白血病)的能力。另一种信号IFNγ则限制了干细胞向某些高度耐药形式发展的进程。当研究人员用抗体阻断这些信号时,保护作用消失,表明ILC1s通过特定的化学信号引导白血病的发展。
将脐带血转化为免疫疗法
由于成年血液中天然ILC1s稀少,团队寻找可再生来源。他们证明可从捐赠的脐带血干细胞在培养中诱导出一类特定的ILC1s,这类细胞缺乏表面标志CD161,但仍具备相应的转录因子和杀伤工具。这些体外生长的ILC1s扩增约700倍,能攻击白血病干细胞同时保留正常造血干细胞,并携带强效的细胞毒分子。将这些ILC1s转入携带人类白血病干细胞的特化小鼠后,白血病生长减缓、存活期延长,这一效果依赖于IFNγ。在并列测试中,它们的表现至少与同样生成的自然杀伤细胞相当。
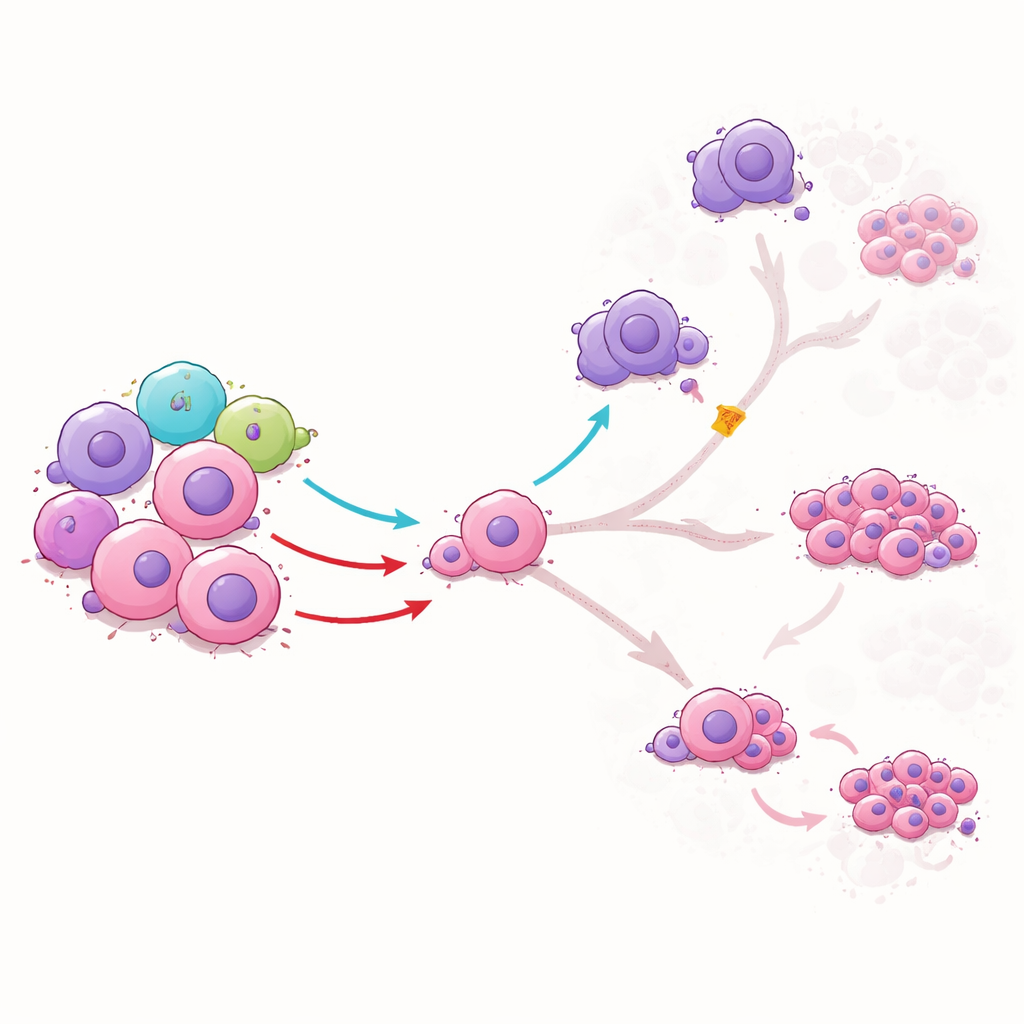
这对未来治疗可能意味着什么
总体而言,研究揭示在AML中,一种自然的免疫制动器——ILC1群体既被缩减又被削弱。从健康供体提供或由脐带血生成的ILC1s可以将白血病干细胞从最有害和最具治疗抵抗性的命运中引离,减少支持白血病的类巨噬细胞,并在小鼠模型中减缓疾病发展。对非专业读者来说,关键信息是科学家们不仅在学习如何消灭癌细胞,还在学习如何用人体自身的快速反应免疫细胞“引导”最早的白血病种子朝更不危险的方向发展。随着进一步开发以及更安全、可扩展的制造方法,基于ILC1的细胞疗法未来有望成为现有治疗的补充,从而降低AML复发的风险。
引用: Li, Z., Ma, R., Tang, H. et al. Human type-1 innate lymphoid cells control leukemia stem cell differentiation and limit acute myeloid leukemia development. Nat Commun 17, 2377 (2026). https://doi.org/10.1038/s41467-026-68582-2
关键词: 急性髓性白血病, 白血病干细胞, 先天淋巴细胞, 癌症免疫治疗, 脐带血