Clear Sky Science · zh
HIF 在肾透明细胞癌中维持 EPAS1 表达的转录调控回路
为何要更仔细地审视肾癌
透明细胞肾细胞癌是最常见的肾癌类型,许多患者现在接受针对一种名为 HIF‑2α 的蛋白的抑制药物治疗。这些药物可以缩小肿瘤,但并非对所有人都同样有效。本研究提出了一个简单但重要的问题:是什么让部分肾脏肿瘤产生大量 HIF‑2α?理解这一“开关”能否帮助我们预测谁最可能从治疗中获益,以及如何设计新疗法?
失控的氧感受器
健康的肾细胞使用一种名为 VHL 的保护蛋白来严格控制氧感受因子——即 HIF 蛋白。当氧气充足时,VHL 将 HIF 蛋白标记以便降解,从而阻止它们开启促进血管生成和细胞分裂的基因。在透明细胞肾癌中,VHL 通常丧失或受损。因此,HIF 家族的一员 HIF‑2α(由 EPAS1 基因编码)免于降解并积累。早期研究显示,高水平的 HIF‑2α 活性与肿瘤生长更快和预后更差相关,而抑制 HIF‑2α 在部分患者中可减缓或阻止肿瘤。然而,提升 EPAS1 基因活性的分子步骤尚未被充分理解。
癌基因的隐匿 DNA 开关
研究者使用患者肿瘤样本、单细胞数据和癌细胞模型,发现透明细胞肾脏肿瘤中 HIF‑2α 信使 RNA 明显高于正常肾组织或其他肾肿瘤类型。随后他们在 EPAS1 基因组区域中搜索表明活跃调控 DNA 的化学和结构标记。结果发现了一个强大的增强子——一种远距离基因开关——位于 EPAS1 约上游 70,000 个碱基处,且特异性地在透明细胞肿瘤中处于活跃状态。在肿瘤细胞中,该增强子的染色质开放、带有激活标记并物理环接触 EPAS1 启动子,而在正常肾小管细胞中该区域大多沉默。该增强子的活性在大型癌症数据集中与较高的 EPAS1 水平相关。 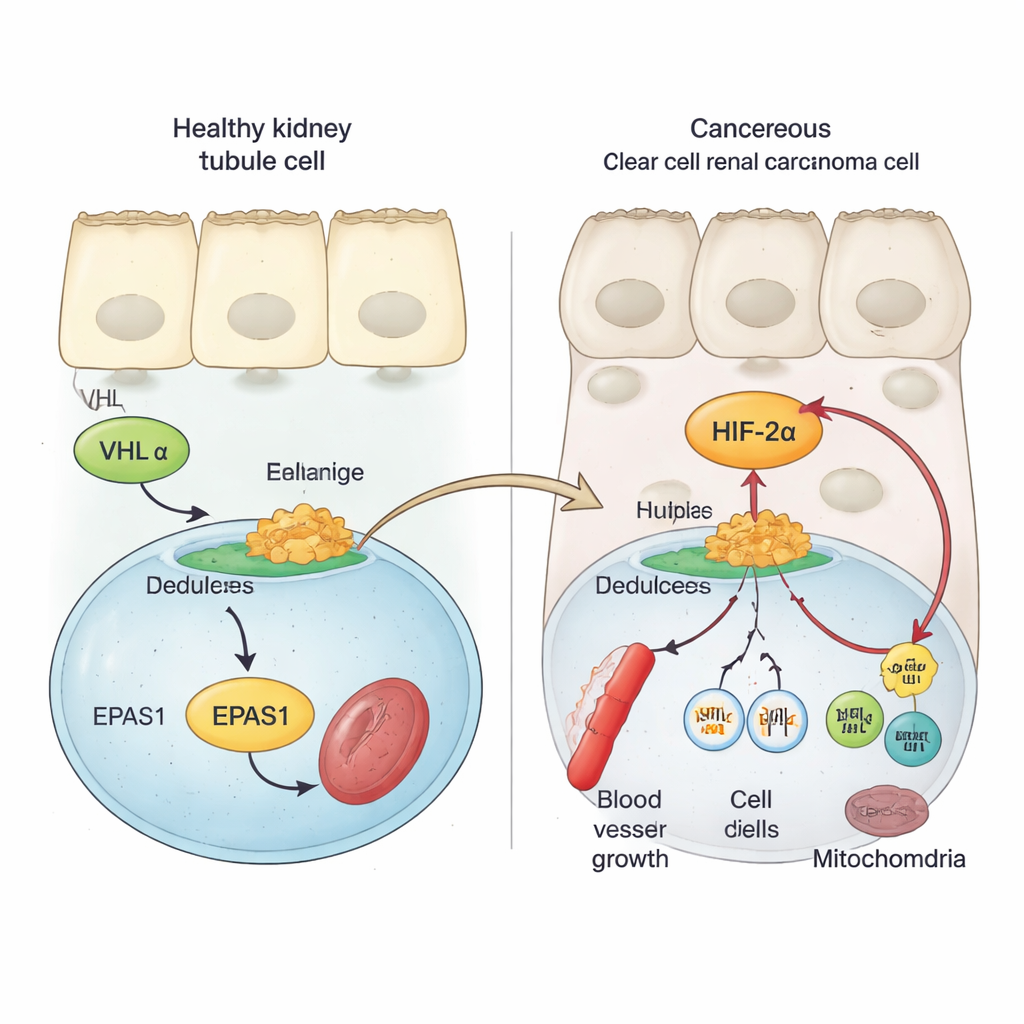
由肾脏特异性因子驱动的自我强化回路
研究发现 HIF 蛋白不仅对低氧作出反应——它们实际上还促进自身的产生。当研究人员恢复 VHL 或去除一个关键的 HIF 伴侣蛋白(HIF‑1β)时,EPAS1 水平下降且该增强子变得不那么可接近。蛋白–DNA 直接结合的精确映射显示 HIF 结合于 EPAS1 上游的两个增强子区域,包括该透明细胞特异性增强子。在肾脏肿瘤细胞中,该增强子也被 PAX8 和 HNF‑1β 占据,这些转录因子参与界定肾细胞身份并已知支持肿瘤生长。破坏 PAX8 或 HNF‑1β,或在增强子内突变它们的结合位点,会降低 HIF‑2α 的 RNA 和蛋白水平并削弱增强子活性。综合这些发现表明存在一个自我调节回路:HIF‑2α 与肾系谱因子协同,增强 EPAS1 增强子的活性,反过来推动更多 HIF‑2α 的产生。
遗传风险与肿瘤行为在同一回路上交汇
在全基因组研究中,EPAS1 区域长期被标为肾癌风险热点,某些遗传变异与更高的癌症发生率及肿瘤中的 VHL 突变相关。通过将遗传数据与基因表达测量相结合,作者显示携带关键 EPAS1 变体高风险等位基因的个体,其肿瘤中往往具有更高的 HIF‑2α 水平——即使在实验上稳定 HIF 时,这一差异在正常肾小管细胞中也可见到。这表明遗传DNA差异可以调节该增强子的响应强度,使一些肾脏在 VHL 丧失后更容易提升 HIF‑2α。对胶质母细胞瘤细胞的实验证明相同增强子也可在某些脑肿瘤中被利用,暗示这一调控模块可能在其它依赖 HIF‑2α 的癌症中被复用。 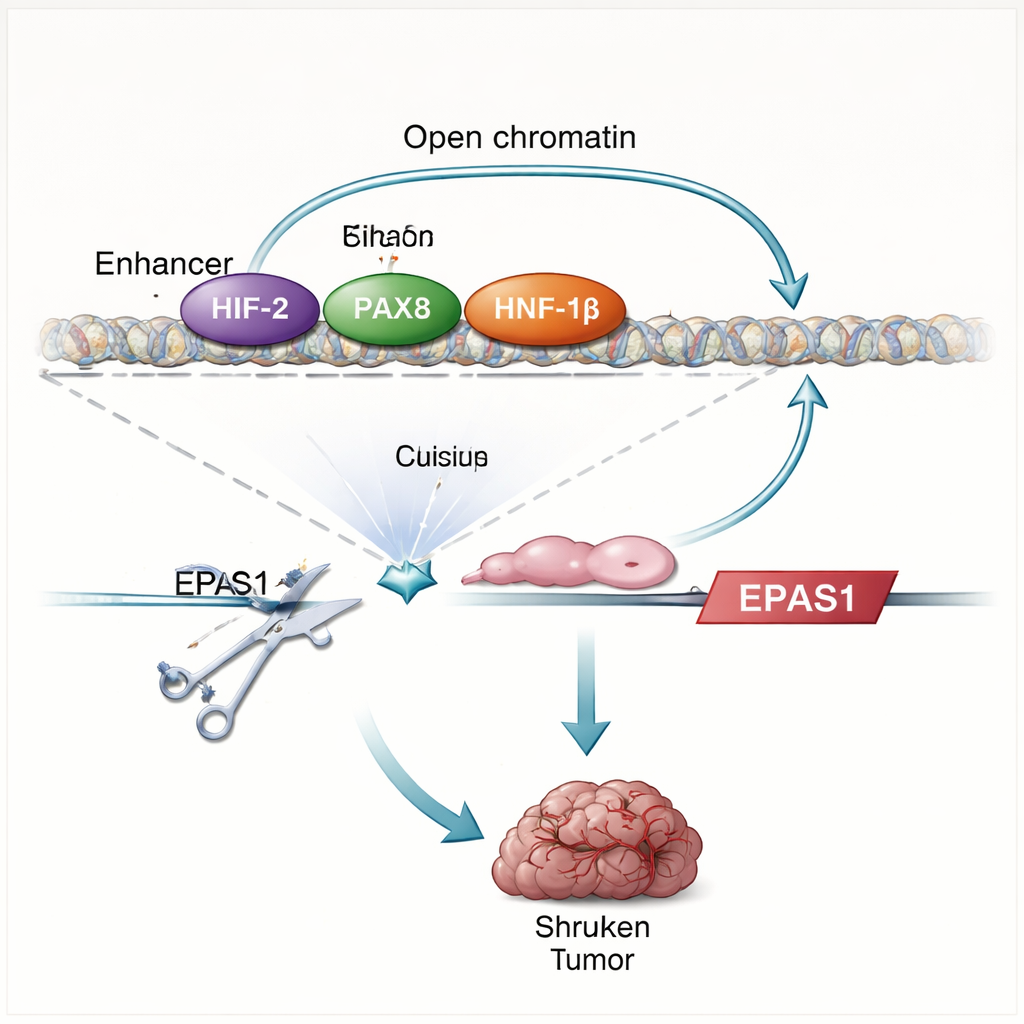
打破回路以抑制肿瘤生长
为测试该增强子的必要性,研究团队利用 CRISPR 基因组编辑破坏了肾癌细胞系和新鲜患者肿瘤细胞中该增强子内的 HIF 结合基序。此类切割将 HIF‑2α 的 RNA 水平降低约三分之一到二分之一,降低了如 CCND1 和 VEGFA 等已知 HIF‑2α 靶基因的表达,并削弱了更广泛的缺氧基因程式。当经编辑的细胞被移植到小鼠体内时,它们大多无法形成肿瘤,与对照细胞形成鲜明对比。增强子破坏后基因变化的模式与用临床药物直接阻断 HIF‑2α 的效果高度相似,强调了这一单一 DNA 元件在这些癌症中作为 HIF‑2α 通路主要驱动因子的作用。
这对患者和治疗意味着什么
对非专业读者而言,核心信息是:作者发现了一个自我放大的 DNA 开关,使一种主要的促癌蛋白 HIF‑2α 在透明细胞肾脏肿瘤中持续开启。该开关既依赖于 VHL 安全刹车的丧失,也依赖肾脏特异性的辅助因子,并受遗传变异影响。因为该增强子在许多透明细胞肿瘤中高度活跃且与 HIF‑2α 通路的强度紧密相关,测量其活性——或直接针对该增强子——可能帮助识别最可能从现有 HIF‑2α 抑制剂中获益的患者,并在肿瘤耐药时提供新的关闭该通路的方法。
引用: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
关键词: 透明细胞肾细胞癌, HIF-2α, EPAS1 增强子, VHL 突变, 肾癌遗传学