Clear Sky Science · zh
使用环状二芳基碘化物的亲旋选择性中断CuAAC反应
这项新化学的重要性
化学家长期以来依赖一种简单的“点击”反应来快速且干净地把分子构件连接在一起,这一手法支撑着从药物发现到自愈材料等诸多领域。本文描述了对经典点击反应的一个巧妙改造,使科学家能够构建更复杂的三维分子并精确控制其手性——这些结构在现代药物和先进材料中非常受重视。
让经典点击反应担任新角色
出发点是铜催化的叠氮–炔环加成,通常简称CuAAC。它在温和条件下可靠地将两个小组分——叠氮和炔——连接成一个五元环三唑。传统上,铜促成三唑环形成后,反应就此终止。然而近年化学家学会了“中断”该过程,在短暂存在的铜–三唑中间体被第三个组分捕获,从而构建更复杂的产物。到目前为止,这类中断尚未能以通用方式控制分子的手性,限制了其在合成复杂手性分子方面的用途。
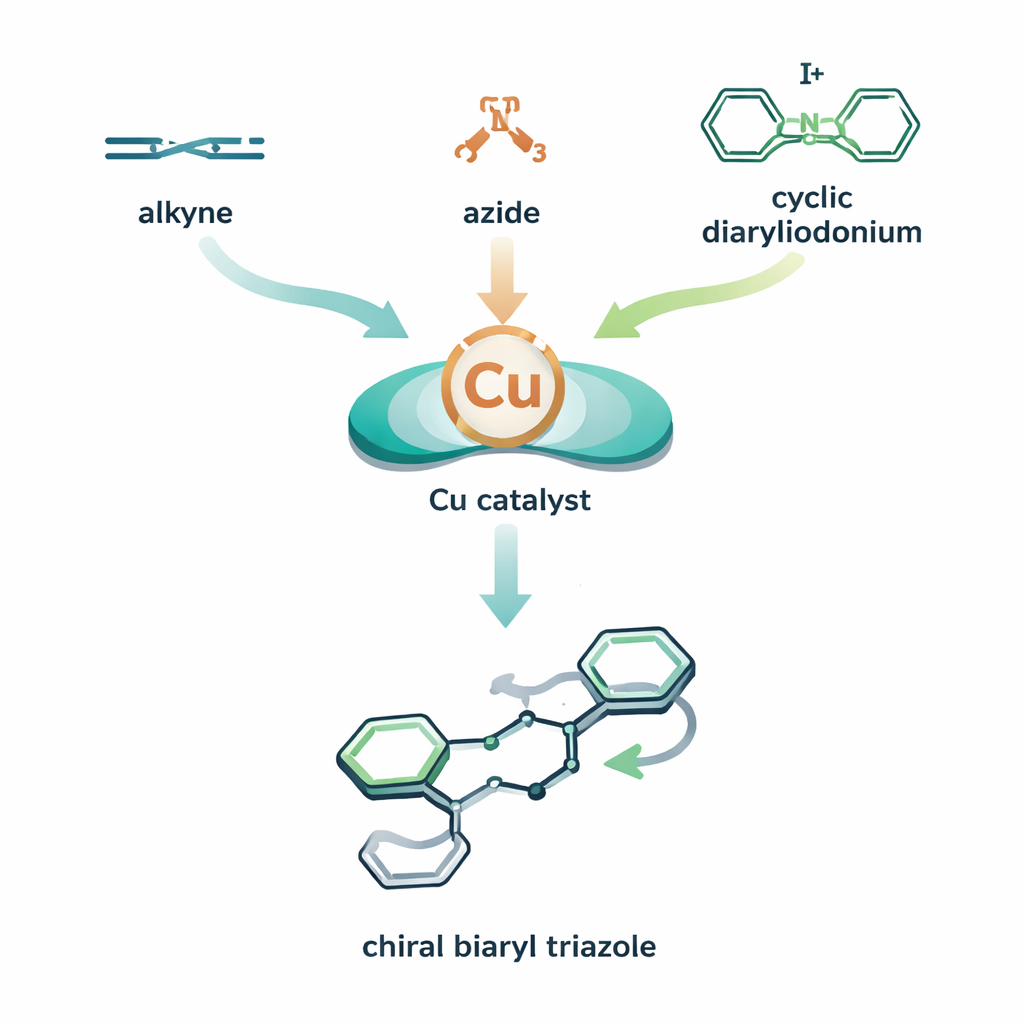
一个三件套分子拼图的转折
作者将两个基于铜的反应循环组合成一个协调的过程。在他们的设计中,铜催化剂先促使炔与叠氮形成铜–三唑中间体。在该中间体被中和之前,第三个组分——一种环状、高活性的含碘分子,称为环状二芳基碘化物——被引入。铜插入该环并打开它,将其中一个芳环缝合到三唑上。结果是一个联芳三唑:两个环系通过一条可作为手性轴的键相连,类似于可向左或向右扭动的螺旋桨。通过将铜与精心挑选的手性配体配对,团队使反应偏向形成其中一种扭转,从而实现高的亲旋选择性(对轴向“手性”的控制)。
检验方法的通用性和可靠性
为评估该反应的通用性,研究者系统地改变了三个构件中的每一个。他们表明,许多不同的炔,包括带有富电子、贫电子和杂芳环的炔,都可以参与并仍能得到良好产率和对一种手性形式的强烈选择性。某些体积较大的取代基提高了选择性但可能降低产率,显示了位阻与效率之间的权衡。叠氮供体在由简单酯或酰胺基团或苄位衍生时表现最佳,这类多种叠氮都能提供高度富集的手性产物。环状二芳基碘化物组分也可以调节:有些取代既能保持产率又能保持选择性,而另一些,尤其是靠近反应性碘中心的取代,会减慢反应或降低性能。总体而言,该研究提供了一系列通过一步法可获得的新型轴向异构联芳三唑。
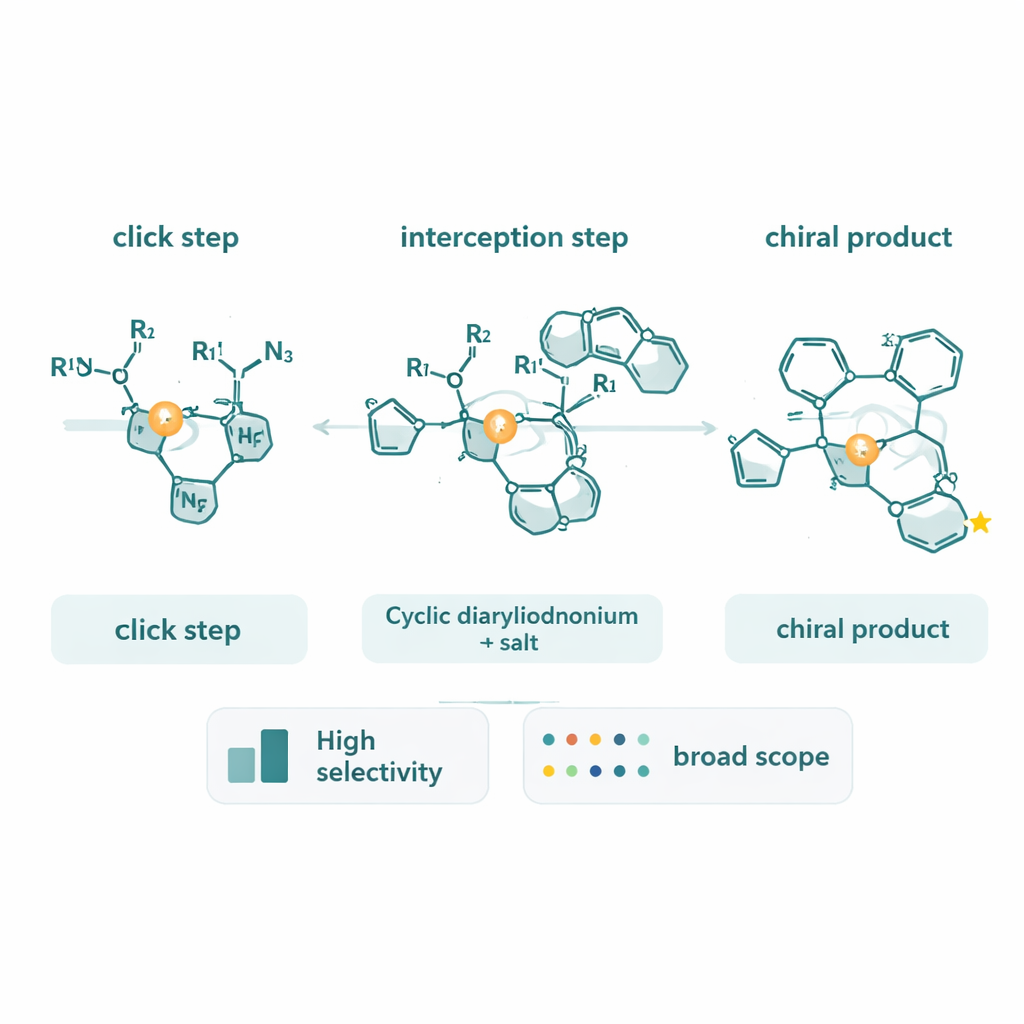
窥探反应机理
除了合成新分子外,团队还投入大量工作以弄清反应的实际机理。使用氘标记炔,他们观察到一种不寻常的逆动力学同位素效应,指向一个速率限制步骤,其中炔碳改变其成键性而非简单地断裂C–H键。基于量热学的反应进程分析显示,反应速率强烈依赖于炔和叠氮的浓度,但对环状二芳基碘化物的依赖很弱。这些测量支持这样一个图景:铜–三唑复合物的形成与转化以及其向二芳基碘化物环的氧化加成共同决定了反应节奏。他们还发现,手性三唑产物本身可以与铜结合并使催化剂变慢,提示了进一步优化体系的途径。
对未来的意义
通俗地说,研究者教会了一种已知的点击反应一个新把戏:它不再只是把两块拼件快速连接起来,而是帮助把三种成分组装成复杂的、类似螺旋桨的分子,并几乎专一地形成一种优选扭转。这样为制备手性联芳三唑提供了一条可放大的途径,这类结构在潜在药物分子、催化剂和功能材料方面具有价值。机理学见解——尤其是关键中间体如何被截获以及产物如何毒化催化剂——为设计更高效、更具选择性的该类化学反应提供了路线图。对非专业读者而言,关键结论是:这一已强大的分子“乐高”工具变得更通用,使化学家能够在三维形态上以更精细的控制构建更复杂、更有用的结构。
引用: Li, Y., Yang, S., Duan, L. et al. Atroposelective interrupted CuAAC reaction using cyclic diaryliodoniums. Nat Commun 17, 944 (2026). https://doi.org/10.1038/s41467-026-68574-2
关键词: 点击化学, 铜催化, 手性联芳, 轴向异构体, 三唑