Clear Sky Science · zh
一种微生理学人类微型膀胱揭示尿液与尿路上皮在组织韧性及尿路致病性大肠杆菌复发中的相互作用
为什么尿液状态很重要
我们大多数人会把尿液简单地看作代谢废物,但其成分会随饮食、饮水和健康状况持续变化。该研究表明,这些变化并非无关紧要的背景噪声:它们可以直接影响膀胱抵御尿路感染(UTI)的能力,以及抗生素治疗后感染复发的容易程度。通过一个在实验室培养的微型“迷你膀胱”,研究者揭示了浓缩尿液如何悄然削弱膀胱组织,并为致病细菌提供新的藏匿与耐受治疗的方式。
在实验室构建微型膀胱
为探索这些隐秘动态,团队在微流体芯片上构建了一个拇指大小的人类“微型膀胱”。他们将人类膀胱表面细胞接种到柔软的三维支架中,诱导其形成几层有序结构,类似真实的膀胱上皮。最顶层的“雨伞”细胞形成了紧密、抗漏的屏障,而更深的层包含能够随时间更新组织的细胞。该装置还允许类尿液在中央通道流动,并能对组织施加缓慢的伸展与放松,模拟膀胱充盈与排空的周期。结构学测试和高分辨成像证实,这一微型器官的表现与真实膀胱高度相似。
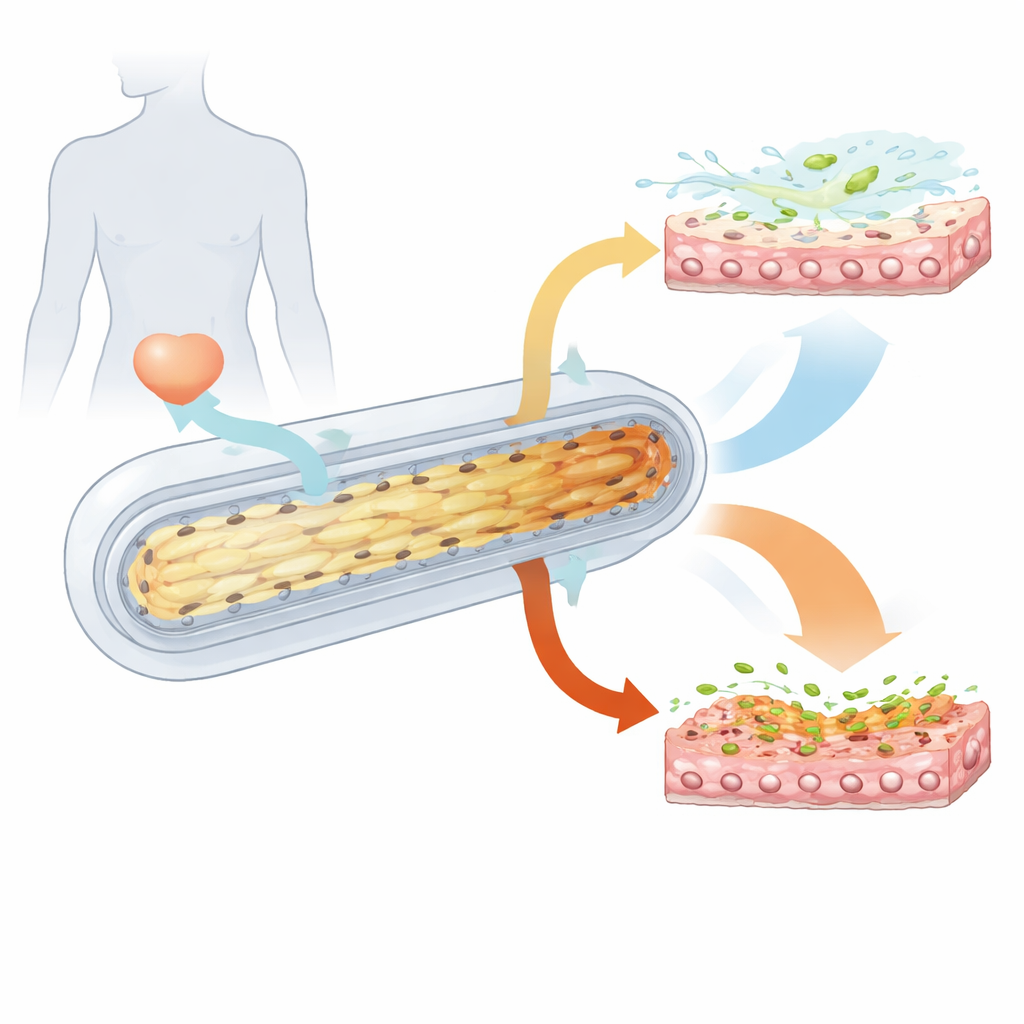
当尿液变得“苛刻”
人体尿液会因补水和健康状况而呈稀释或高度浓缩的状态。研究者配制了两种合成尿液混合物:一种“低溶质”,一种“高溶质”,分别对应天然人尿成分的低端和高端。当微型膀胱在高溶质尿液中持续培养数日,组织逐渐退化。死亡细胞增加、总细胞数下降,细胞间原本紧密的连接变得渗漏。基因表达显示细胞间黏附减少、组织更新能力减弱以及先天免疫信号被抑制。相比之下,低溶质尿液支持细胞生长、紧密连接更强以及膀胱上皮的健康分化。简言之,反复暴露于非常浓缩的尿液会使组织在结构上变弱,并降低其发起早期免疫防御的准备度。
脆弱组织如何助长感染
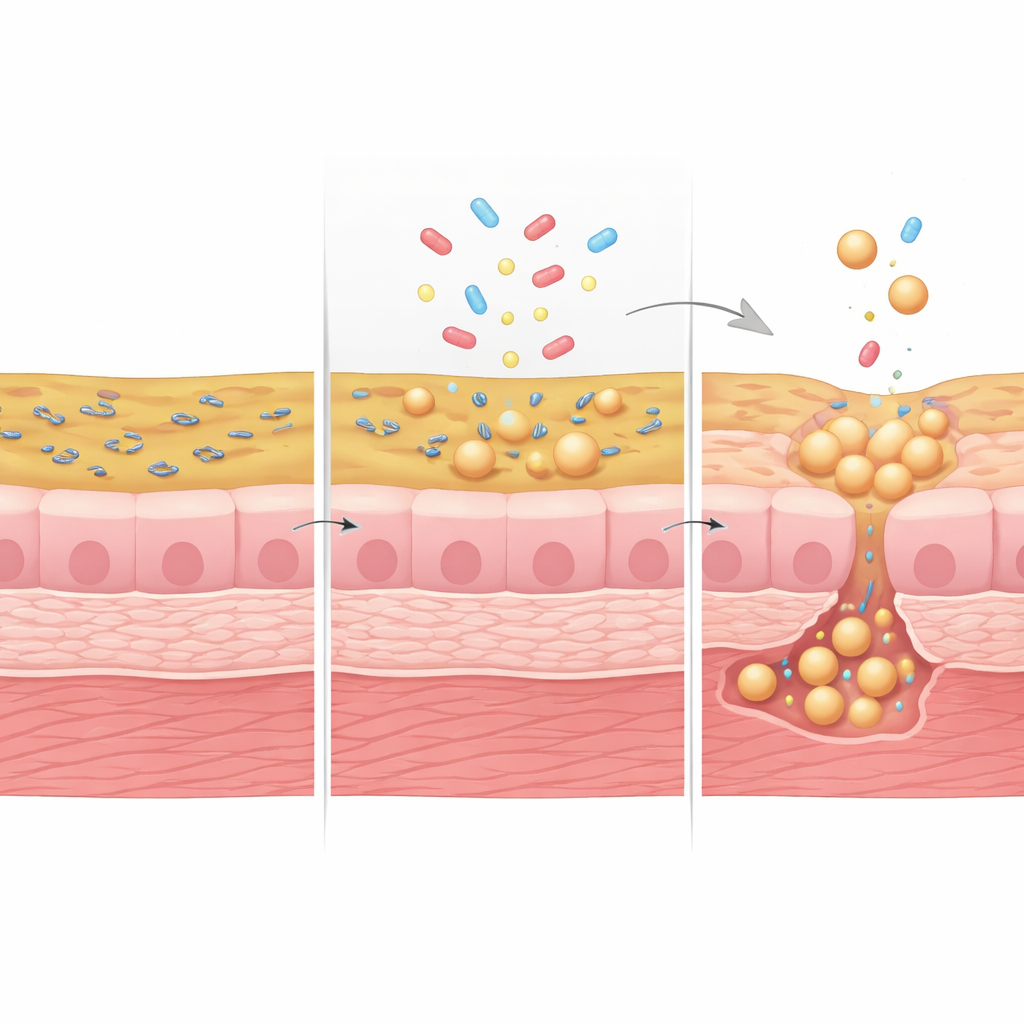
随后团队用尿路致病性大肠杆菌(UPEC)感染微型膀胱,并定期冲洗通道以模拟排尿。每次“排空”后,许多细菌被冲走,但有些细菌依然附着或侵入膀胱上皮,并逐渐形成隐匿的组织相关群体。通过用糖类D-甘露糖阻断细菌的主要附着机制,研究者减少了这一嵌入群体并观察到组织损伤减轻,表明附着于组织表面与内部的细菌在排尿间隙帮助重新播散尿中细菌。当微型膀胱先暴露于高溶质尿液时,更多细菌渗入组织,且像环丙沙星等常规抗生素更难清除这些组织内细菌,尽管尿液中游离的细菌仍然能被有效洗除。
抗生素后隐藏的幸存者
使用磷霉素(一种常用的靶向细菌细胞壁的抗生素)时,情况更为显著。在高溶质尿液中,磷霉素对减少细菌负荷效果不佳,游离细菌常从杆状变为体积大、脆弱、缺乏细胞壁的球形体。在复发性UTI患者的尿液中也曾观察到类似的球形形式。借助先进的三维电子显微镜结合荧光成像,研究者发现这些球形细菌不仅漂浮在尿液中,还嵌入在膀胱细胞之间和深层组织之下的微型膀胱壁内。这些受庇护的形式经受住了治疗,随后促成细菌重新生长,部分解释了症状短暂好转后感染为何会再次爆发。
这对患者意味着什么
这项工作表明,膀胱环境不仅是背景板,而是在感染与治疗结局中发挥积极作用的因素。浓缩尿液削弱膀胱上皮、抑制其免疫防御,并允许细菌侵入更深处并采取特殊的无细胞壁状态,这些状态使其难以被抗生素和免疫细胞清除。新的微型膀胱平台展示了尿液成分、膀胱组织健康与细菌行为之间的紧密联系。对于易复发UTI的人群,使尿液更浓缩的因素——例如饮水不足或某些疾病——可能会通过削弱组织韧性和促成隐藏的细菌储库而悄然增加风险。理解并最终调整这一微环境,连同更有效的抗生素策略,或许是打破反复感染循环的关键。
引用: Paduthol, G., Nikolaev, M., Sharma, K. et al. A microphysiological human mini-bladder reveals urine-urothelium interplay in tissue resilience and UPEC recurrence in urinary tract infections. Nat Commun 17, 2322 (2026). https://doi.org/10.1038/s41467-026-68573-3
关键词: 尿路感染, 膀胱类器官, 尿路致病性大肠杆菌, 抗生素耐受性, 尿液浓度