Clear Sky Science · zh
对内分泌耐药ER阳性/HER2阴性乳腺癌行术前帕博昔布联合阿那曲唑反应的生物标志物:一项二期试验
这项研究对患者和家庭的重要性
许多患有一种常见类型乳腺癌的女性最初对阻断激素的药物有良好反应,但其肿瘤常会随后产生耐药并再次生长。本研究提出了一个紧迫的问题:在这些难治的病例中,将一种更新的阻断细胞周期的药物加入标准激素治疗是否有助益?我们能否在肿瘤中找到预示谁会受益和谁不会受益的警示信号?
聚焦难缠的乳腺癌
该试验聚焦于雌激素受体阳性、HER2阴性的乳腺癌,这是最常见的亚型。所有34例患者均已在术前接受过标准的激素治疗(芳香化酶抑制剂),但仍显示肿瘤细胞活跃增殖,故被认为是“内分泌耐药”。研究者随后在术前用激素药阿那曲唑与阻断细胞周期的帕博昔布联合治疗这些患者。他们使用Ki67这一标志来测量肿瘤细胞的分裂速度。如果Ki67在两周后降到非常低的水平,该肿瘤即被认为达到“完全细胞周期停滞”,表明癌细胞分裂已被有效抑制。
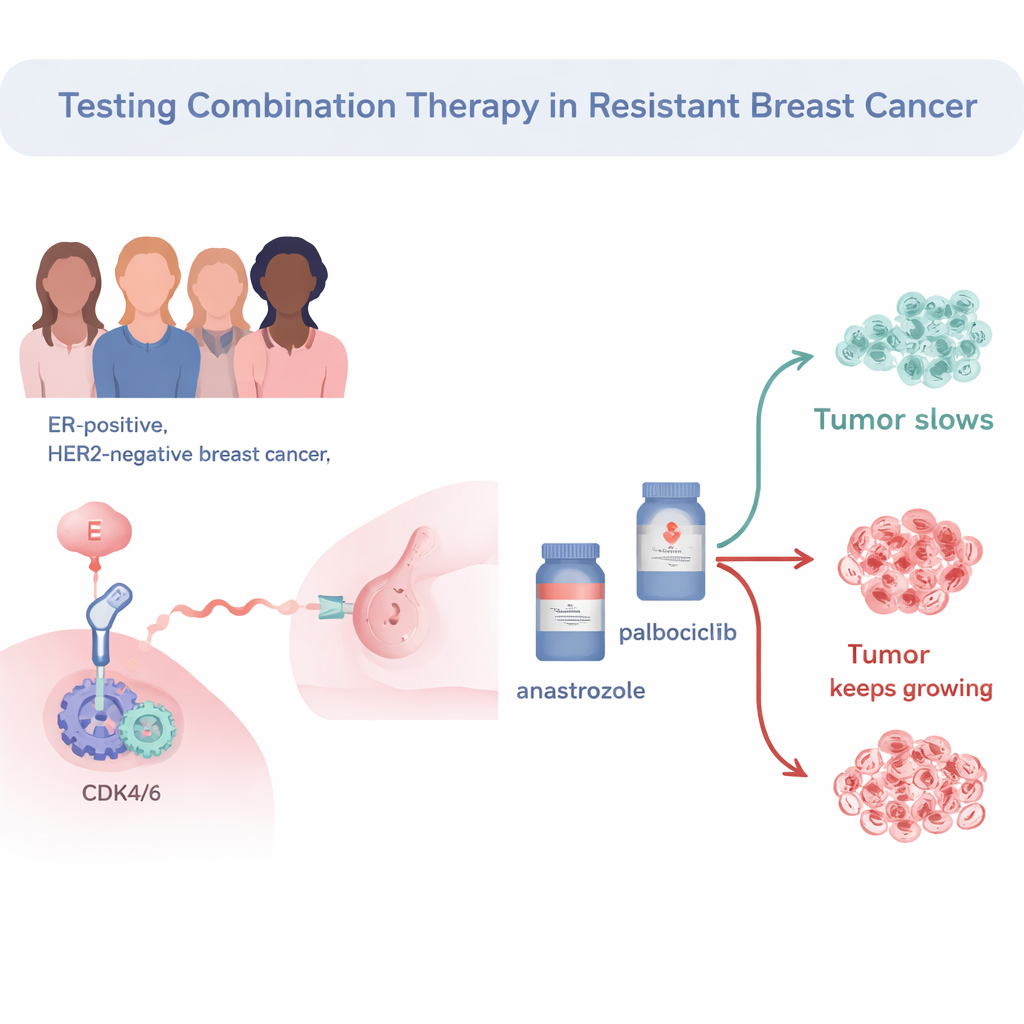
谁对该药物组合有反应?
在33例可完全评估的患者中,57.6%在仅两周的联合治疗后达到了完全细胞周期停滞。若采用更宽松的阈值——仅当Ki67降至10%以下即划为“敏感”——约有三分之二的肿瘤被认为有反应。那些Ki67仍然高企的患者往往具有更具侵袭性的肿瘤:分级更高、体积更大且起始Ki67水平更高。他们也更可能属于所谓的“非腔型(non‑luminal)”分子亚型,这些亚型通常比典型的激素驱动“腔型A”肿瘤表现得更具侵袭性。
是什么让某些肿瘤产生耐药?
研究团队并不限于简单的反应率,而是对肿瘤样本进行了深入分析,包含DNA测序、RNA测序和蛋白质谱。耐药肿瘤并非由单一突变决定;相反,它们表现出一种“过度活跃的回路”模式。与敏感肿瘤相比,耐药肿瘤的雌激素受体信号减弱,但驱动细胞分裂和生长的通路更强,例如细胞周期基因、mTOR生长通路,以及若干炎症和干扰素相关网络。它们还表现出更高水平的免疫“刹车”,即免疫检查点,包括能帮助肿瘤逃避免疫监视的IDO1和PD‑L1等基因。
从通路发现到潜在新疗法
为检验这些过度活跃的通路是否可成为治疗靶点,研究者建立了实验室细胞模型,这些模型已对帕博昔布等CDK4/6抑制剂产生耐药。这些耐药细胞展示出与患者肿瘤相同的增强细胞周期和干扰素/炎症信号特征。当暴露于阻断JAK‑STAT信号通路(干扰素下游关键通路)的药物时,一种药物帕克替尼(pacritinib)在抑制耐药细胞及患者来源的肿瘤类器官生长方面尤其有效。这提示,将CDK4/6抑制剂与某些针对JAK的药物联合,可能是对付已绕过现有组合疗法的肿瘤的有前景策略。
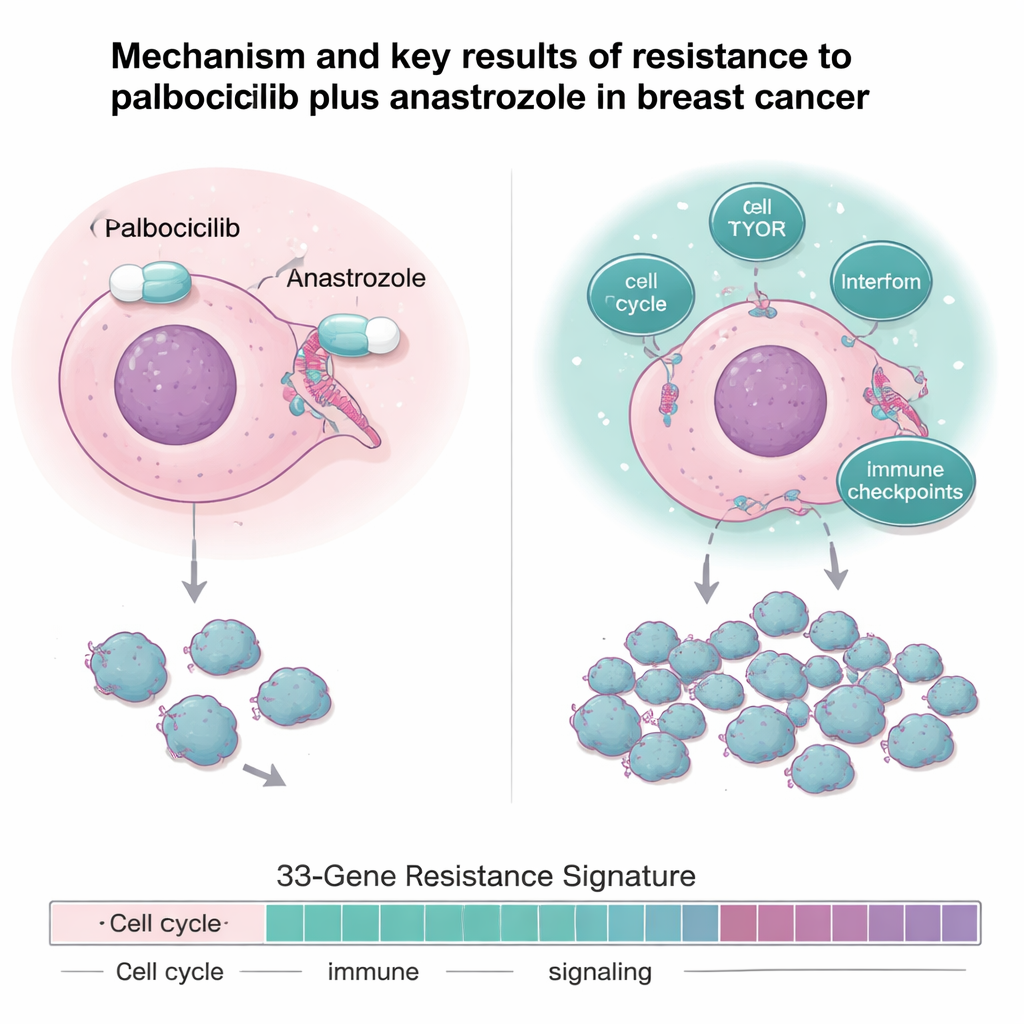
预测结局的基因指纹
通过在两项相关试验中比较敏感与耐药肿瘤,研究者构建了一个由33个基因组成的“耐药签名”,涵盖参与细胞分裂、DNA修复、生长信号、代谢及免疫/炎症反应的基因。这一基因指纹在区分试验中的敏感与耐药肿瘤方面非常准确。重要的是,当将相同的33基因模式应用于一组由常规临床中接受CDK4/6抑制剂加激素治疗的151例转移性乳腺癌患者时,那些耐药签名得分高的患者具有更短的疾病进展时间和更短的总体生存期。换言之,这一在治疗前测得的基因模式可提示哪些患者较不可能从标准基于CDK4/6的方案中获得长期益处。
对未来护理的意义
对于面临内分泌耐药ER阳性乳腺癌的人群,这项研究既带来一定的安慰也提供了一条路线图。它表明,将帕博昔布加入阿那曲唑后,仍有超过一半的耐药病例能够被抑制肿瘤生长。与此同时,研究显示一些肿瘤依赖于替代的生长和免疫相关通路,使其更难控制。新定义的33基因签名以及发现像帕克替尼这样的JAK靶向药能够抑制耐药细胞,指向了更个体化的治疗:及早识别那些不太可能对标准联合治疗有反应的患者,并尽早将他们纳入测试直接针对肿瘤备选生存通路的新药物组合的临床试验。
引用: Kong, T., Mabry, A., Highkin, M. et al. Biomarkers of response to neoadjuvant palbociclib plus anastrozole in endocrine-resistant estrogen receptor-positive/HER2-negative breast cancer: a phase 2 trial. Nat Commun 17, 949 (2026). https://doi.org/10.1038/s41467-026-68570-6
关键词: ER阳性乳腺癌, CDK4/6抑制剂, 内分泌耐药, 肿瘤生物标志物, 帕博昔布 阿那曲唑