Clear Sky Science · zh
打破细胞壁以实现对硅藻的高效DNA递送
作为微小绿色工厂的藻类
硅藻——漂浮在海洋中的微小藻类——悄然承担着约五分之一的全球有机碳固定,既为海洋食物网提供能量,也帮助封存二氧化碳。科学家希望把这些耐受性强、生长迅速的生物改造为微小的绿色工厂,用来生产燃料、食品和特种化学品。但有一个主要障碍:要可靠地将新DNA引入硅藻细胞竟意外地困难。这项研究直面这一实际问题,描述了将遗传指令和基因组编辑工具穿过硅藻坚韧外壳的新方法。
软化海洋微生物的外壳
这项工作以模式硅藻Phaeodactylum tricornutum为中心,该物种在实验室中广受青睐,因为其基因组已被良好绘制并且已有一些基础遗传工具。作者推断,作为任何DNA必须跨越的第一道物理屏障,细胞壁是关键瓶颈。通过用一种名为alcalase的酶处理细胞,他们部分或全部去除了这层壁,形成易碎的“球状体”和“原生质体”,这些细胞更容易被穿透。随后使用电穿孔——短促的电脉冲开启临时孔洞——成功转化的数量显著跃升,与早期方法相比大约提高了两个数量级。即使是极少量的DNA,低至一纳克,也足以恢复出工程化细胞。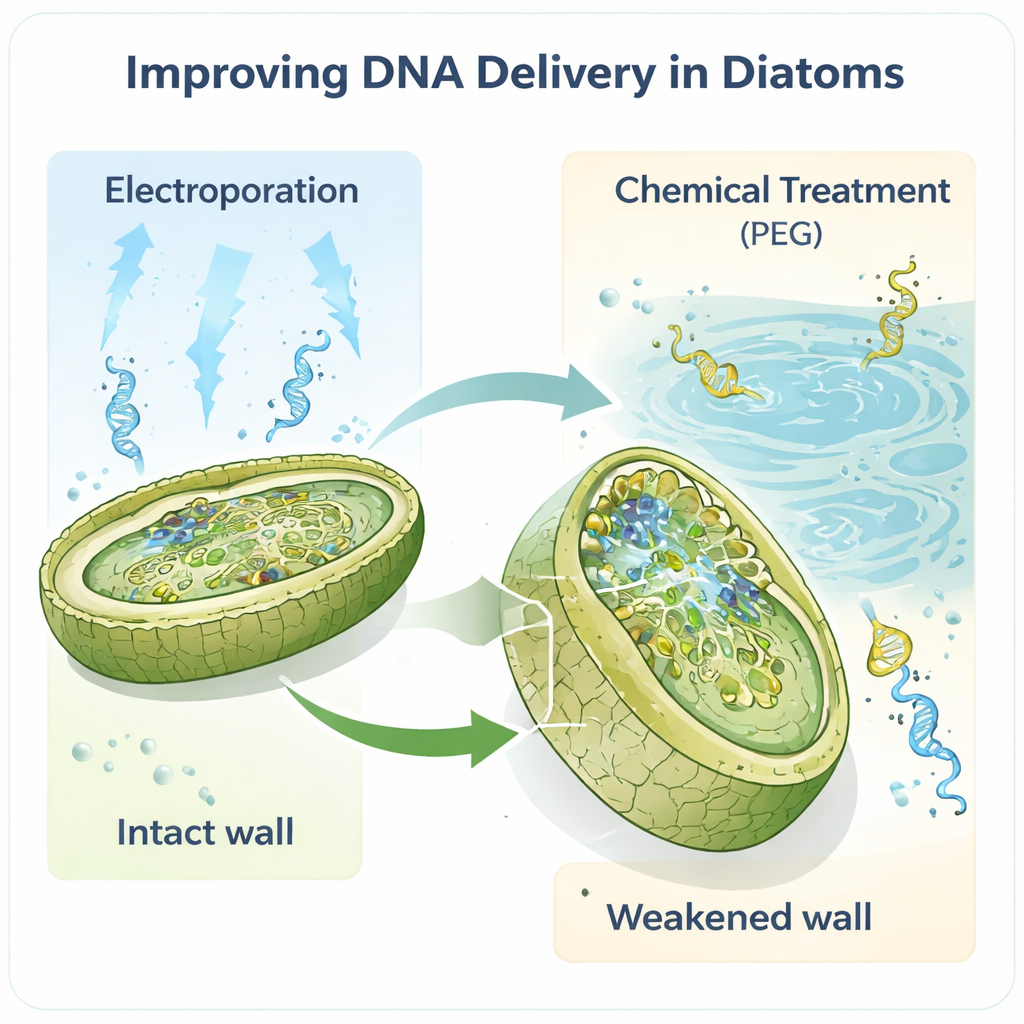
无需经由细菌的快速DNA递送
传统的硅藻改造方法常依赖细菌作为“信使”携带大型环状DNA分子(称为表位体)进入藻类。尽管有效,这种途径速度慢、技术要求高,并可能使脆弱的DNA构件不稳定。新的方案表明,电穿孔和改良的聚乙二醇(PEG)化学方法都能将表位体直接送入硅藻,绕过细菌中转步骤。值得注意的是,长达55.6千碱基对的表位体都能被完整递送并回收。相同策略在第二种物种Thalassiosira pseudonana中也有效,该物种具有更重的矿化细胞壁,表明这是一套通用的工具包,而非仅对某一物种有效的技巧。
让细胞自行构建遗传圈
在探究电穿孔DNA在细胞内的行为时,团队发现了一个令人惊讶的能力:硅藻可以自行拼接DNA片段。线性表位体片段进入细胞后,通过不精确的“非同源”连接或更准确的、基于重叠的“同源定向”修复被修复为环状。作者将这一过程称为“硅藻体内组装”(diatom in vivo assembly,简称DIVA)。通过设计重叠片段,他们诱导细胞将两段、三段或四段片段高效率地组装成完整表位体,有时甚至整合了小型合成盒子,添加荧光标签或新功能。这一能力将硅藻细胞核变成微型DNA加工车间,有望替代通常在酵母或大肠杆菌中进行的耗时组装步骤。
仅用蛋白复合体进行基因组编辑
除了添加表位体外,研究者还展示了他们可以借助优化后的电穿孔方法将预制的CRISPR–Cas9蛋白‑RNA复合体直接递送入硅藻细胞。以控制对一种有毒腺嘌呤类似物敏感性的基因PtAPT为目标,他们产生了数千个耐药突变体,而未在基因组中引入任何额外DNA。许多突变体在靶位点携带小的插入或缺失;有些甚至捕获了作为缓冲电击而加入的“运载”DNA片段。团队随后在一步中共同递送CRISPR复合体和表位体,发现大约十分之一的菌落同时携带基因组编辑与可选择的表位体——这是一种高效追踪通常看不见的基因变化的方法。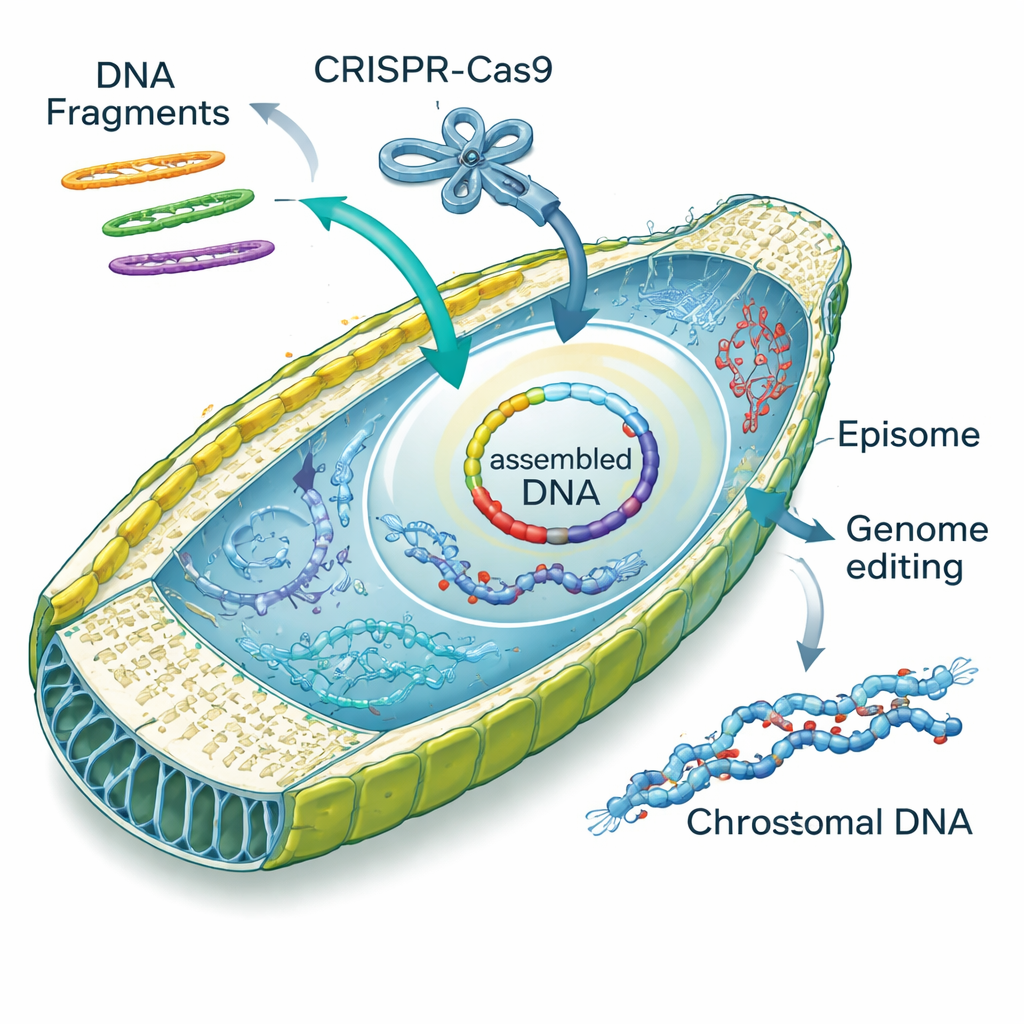
迈向可持续未来的定制硅藻
对非专业读者而言,关键结论是硅藻正在快速接近成为实用且可编程的生物体。通过温和打破或软化细胞壁,作者将一个挑剔、低产的过程转变为稳健的流程——它使用少量DNA,适用于大型遗传构件,甚至允许细胞自行组装和编辑DNA。这些进展缩短了从计算机设计序列到活体经验证株的路径。从长远看,这类工具可加速构建具有完全合成染色体的硅藻,并将这些海洋微生物用于更清洁的燃料、对气候更友好的化学品以及新的生物学发现的开发。
引用: Walker, E.J.L., Pampuch, M., Deng, L. et al. Breaking the cell wall for efficient DNA delivery to diatoms. Nat Commun 17, 1848 (2026). https://doi.org/10.1038/s41467-026-68562-6
关键词: 硅藻生物技术, 基因转化, CRISPR基因组编辑, 合成生物学, 微藻工程