Clear Sky Science · zh
微生物激活 GLP-2R 可缓解胃肠道炎症
为何对肠道有益的蛋白很重要
在全球寻找可持续方式养活不断增长的人口的过程中,科学家们正把目光从农田转向用于生产微生物食物的大型钢罐。本研究探讨了一种微生物来源的蛋白是否能不仅仅作为营养来源。研究者提出问题:一种由无害细菌制成的蛋白,能否既满足膳食需要,又能积极保护肠道免受炎症侵袭——而肠道炎症正是炎症性肠病和化疗引起的肠道损伤等疾病的核心问题?
一种新型微生物蛋白
本研究关注的蛋白来源于一种土壤细菌 Methylococcus capsulatus Bath(简称 McB)。McB 并非以活菌形式被食用,而是被加工成微生物裂解物——一种粉状的破碎细胞混合物,以商品名 FeedKind® 生产。小鼠食用了以该裂解物提供大部分蛋白的饲料,饲料分为简单型或更接近人类饮食的“复杂”型。研究团队随后追踪这种饮食如何改变肠道微生物群落、巡逻肠道的免疫细胞,以及肠道抵御不同损伤的能力。
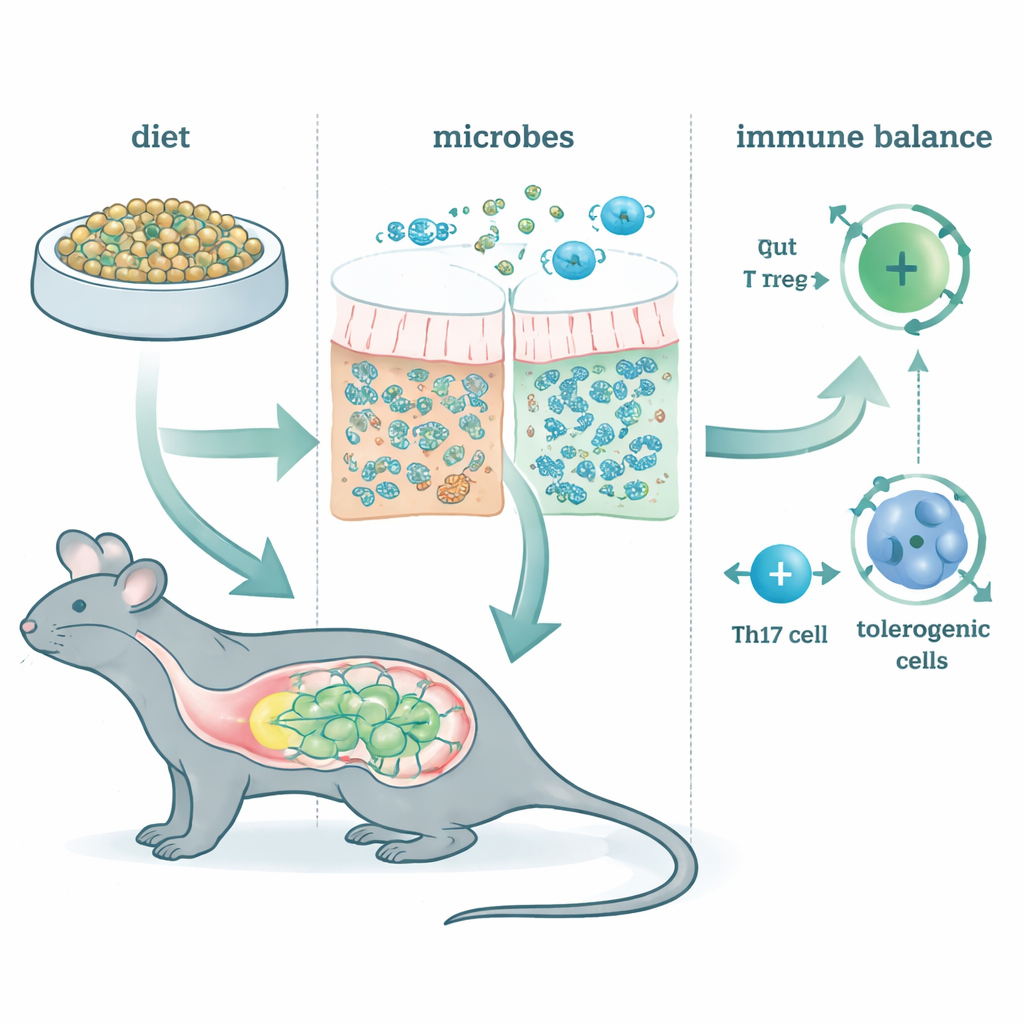
重塑微生物邻里
不论动物所吃的基础饮食如何,摄入 McB 都能迅速且持续地改变肠道微生物群落。粪便中几乎检测不到 McB 本身的成分,表明这些物质在肠道中几乎被完全利用了。取而代之的是少数几种来自 Lachnospiraceae、Bacteroidaceae 等科的细菌繁盛起来。基因组分析显示,这些群落富集了产生短链脂肪酸的发酵通路——短链脂肪酸是已知可滋养肠道细胞并影响免疫的小分子。换句话说,McB 更像是一种有针对性的燃料,能够重塑驻留微生物的代谢活动,而非传统意义上的蛋白质替代品。
教导免疫系统学会耐受
作者接着检查了决定肠道对进入物质是平静反应还是激烈反应的关键 T 细胞类型。其中一类、外周诱导的调节性 T 细胞(pTreg),有助于防止对食物和共生微生物的过度反应。另一类 Th17 细胞则取决于其“状态”,既可能驱动有害炎症,也可能维持健康屏障。McB 饮食显著增加了整个肠道的 pTreg,即便在用抗生素清除大部分肠道微生物的情况下仍然如此。相比之下,McB 对 Th17 细胞的影响依赖于肠道细菌的存在和正常功能。在微生物完整的动物中,McB 将 Th17 细胞推向更具耐受性的状态——产生更多 IL‑10、炎性降低。当发酵被阻断时,这种耐受性转变消失,强调了 McB 部分通过重定向微生物与免疫之间的对话来发挥作用。
损伤期间保护肠道
为了检验这些变化是否能转化为真实世界的保护,研究者用两种强烈的肠道损伤模型对小鼠进行挑战。一种是化疗药物 5‑氟尿嘧啶,会引起广泛损伤并使吸收营养的指状绒毛萎缩。另一种是诱导结肠炎的化学物质(DSS),作为大肠炎症模型。服用 McB 饮食的小鼠体重下降较少,绒毛和结肠长度保持较好,出血性病变更少,组织学损伤评分在两种模型中均较低。这些益处在实验性去除 CD4 T 细胞后仍然存在,提示 McB 对肠道的保护作用不仅仅依赖适应性免疫细胞,还涉及对肠上皮的直接影响。
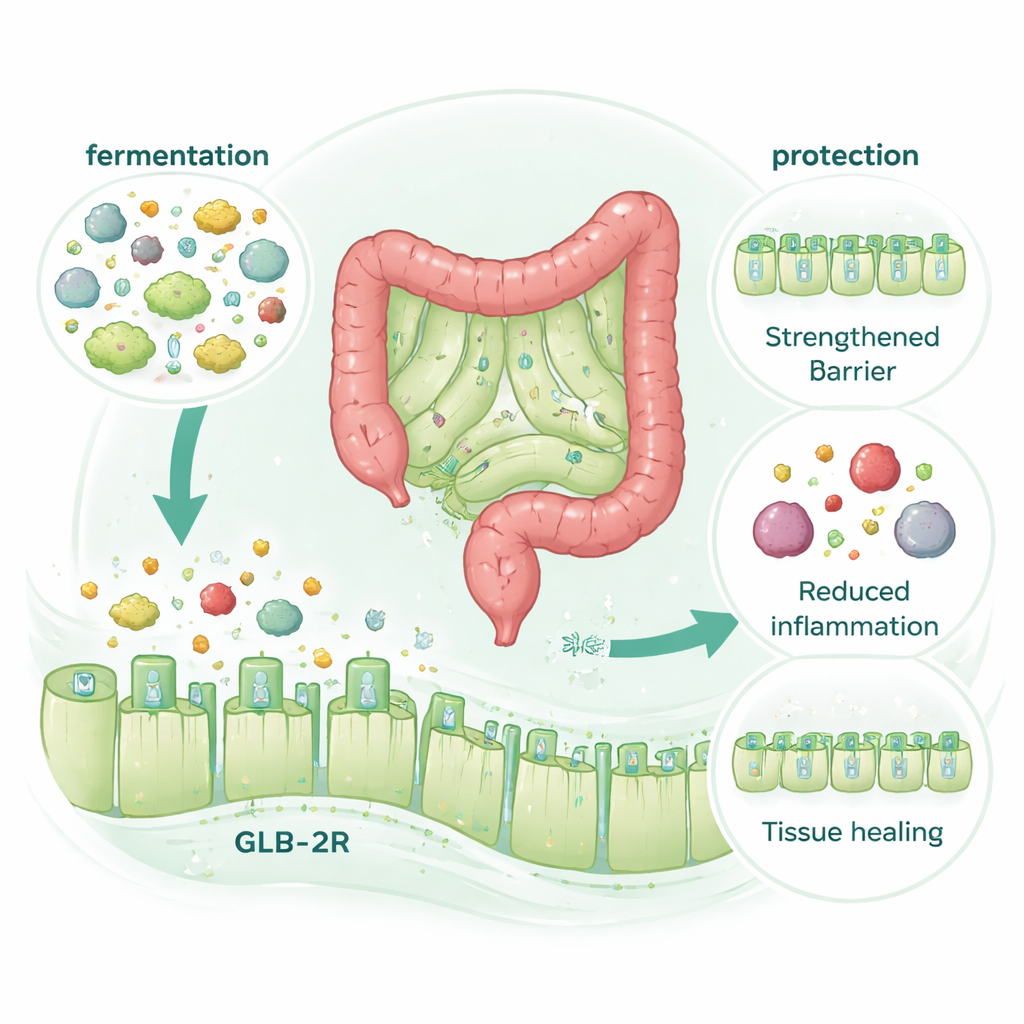
涉及一种激素受体,但并非额外分泌激素
一个令人意外的发现是,McB 的保护效应绝对依赖于肠道中修复促进激素 GLP‑2 的受体(GLP‑2R),而与相关的 GLP‑1 受体无关。当小鼠缺乏 GLP‑2R 时,McB 无法再防护其免受化疗或结肠炎的损伤。然而,McB 本身并未增加血液中 GLP‑2 的水平,即便在严格控制消化和激素降解的条件下也是如此。相反,当结肠中的微生物发酵被化学阻断时,这些益处消失了,尽管总体微生物组成变化很小。这指向一种机制:McB 被微生物分解产生的小分子充当了 GLP‑2 的“模拟物”,激活其受体以强化屏障并促进修复,而并非通过额外释放激素来实现。
对未来食品的潜在意义
对普通读者而言,结论是:某些未来的蛋白来源可能不仅设计为气候友好,还能主动支持肠道健康。在小鼠中,一种可规模化生产的 McB 裂解物既将免疫重编程为耐受状态,又通过两条部分独立的路径帮助肠道抵御严重损伤:直接提升调节性 T 细胞,以及通过发酵驱动的 GLP‑2 受体激活促进组织修复。尽管仍需开展人体研究,该工作表明微生物来源的蛋白可能形成一类新的“智能”食品——既能喂养我们、与自身微生物协作,又能默默增强肠道对炎症的天然防御。
引用: Yang-Jensen, S.K., Choi, B.SY., Nägele, N.S. et al. Microbial activation of the GLP-2R mitigates gastrointestinal inflammation. Nat Commun 17, 1839 (2026). https://doi.org/10.1038/s41467-026-68551-9
关键词: 肠道炎症, 微生物蛋白, 微生物组, GLP-2 受体, 调节性 T 细胞