Clear Sky Science · zh
以太脂质通过调节铁摄取影响癌细胞命运
一种鲜为人知的脂质如何揭示癌症的薄弱环节
癌症常被描述为一种“基因疾病”,但这项研究表明,构成细胞外膜的脂质同样重要。研究者发现,一类特殊的脂质——以太脂质,帮助危险的癌细胞从周围环境中摄取铁,这既促进了它们的扩散能力,也增加了它们对一种新近认知的细胞死亡形式的脆弱性。理解细胞膜、铁代谢与肿瘤行为之间这一隐秘联系,或可为选择性清除最具侵袭性的癌细胞开辟新疗法途径。
以不同视角看待癌细胞
大多数癌症研究聚焦于DNA突变及其编码的蛋白质。这项工作将注意力转向细胞膜——包围每个细胞的那层薄薄的脂质壳。在那层膜中存在多种脂类,各自具有不同的形状和物理特性。作者关注的是以太脂质,它们在许多哺乳动物细胞的磷脂中约占五分之一,但相对鲜有研究。研究发现,高转移性且具干样特征的癌细胞在膜中富集以太脂质,使膜张力较低且流动性较高。这些物理特性反过来改变了细胞摄取铁的方式,而铁既能推动肿瘤生长,又能引发一种名为铁死亡的、依赖铁的破坏性细胞死亡过程。
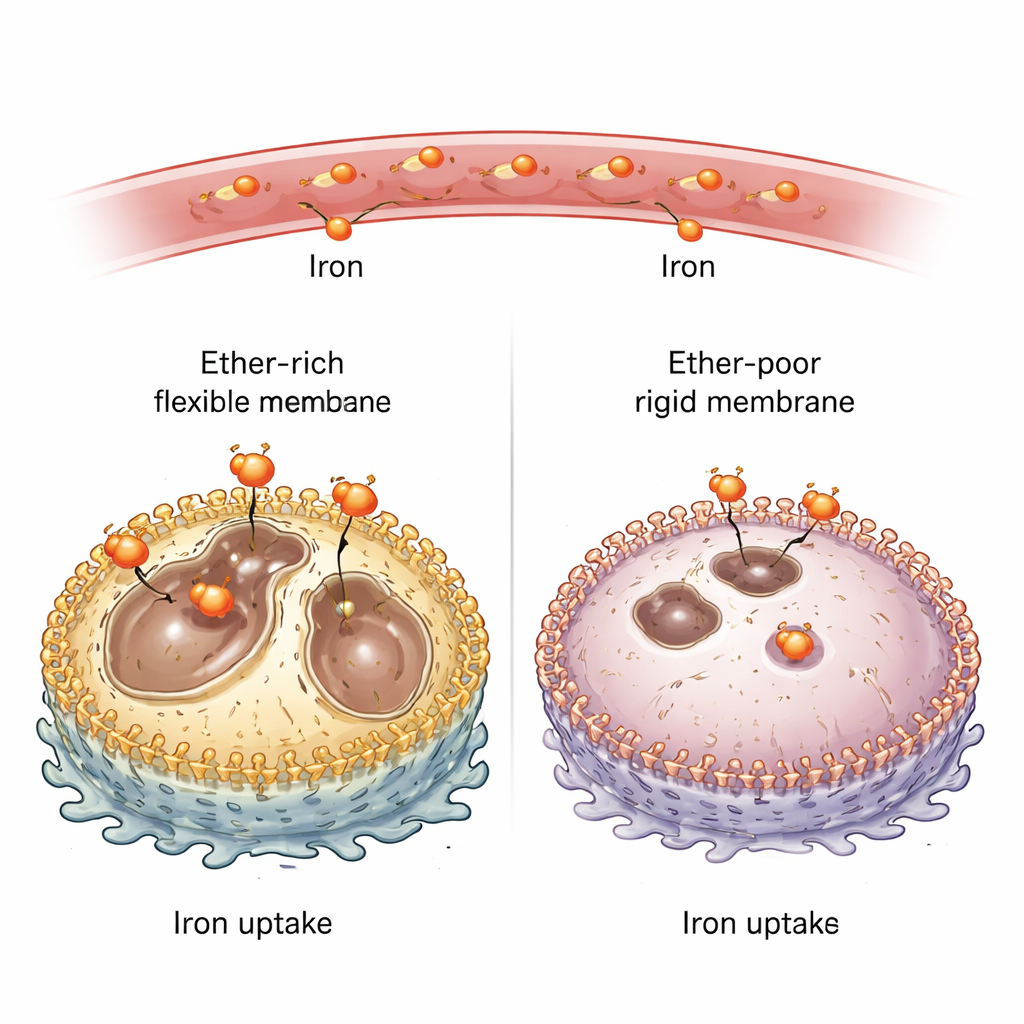
将膜脂与铁摄入联系起来
为探究以太脂质的作用,研究团队在多种小鼠和人类癌细胞系中敲除合成此类脂质所需的关键酶。没有这些酶后,质膜中的以太脂质从大约四分之一骤降到只有少数百分点。令人惊讶的是,这些缺乏以太脂质的细胞携带的“氧化还原活性”铁大幅减少——无论在培养中还是在植入小鼠的肿瘤中都是如此。当科学家从外部补充额外铁源时,细胞的铁含量回升,并重新对促铁死亡药物敏感。这表明以太脂质不仅仅是可氧化的燃料;它们积极控制进入细胞的铁量。
一种专门的铁门:CD44通路
研究者随后探究膜成分如何改变铁的摄取。细胞通常通过一种众所周知的蛋白——转铁蛋白受体来摄取铁,但侵袭性、干样的癌细胞还依赖另一条途径:表面蛋白CD44,它能内吞与透明质酸(一种糖类分子)结合的铁。通过追踪荧光探针,团队显示敲除以太脂质几乎不影响转铁蛋白受体介导的摄取,但显著减慢了CD44介导的内吞——这是一种不依赖网格蛋白(clathrin)的替代物质进入细胞的路线。恢复以太脂质或以脂质体形式补回它们可使该CD44通路恢复功能。破坏CD44本身或降解透明质酸会降低细胞内铁水平,证实了这条依赖以太脂质的通路是这些癌细胞的主要铁入口。
更柔软的膜如何改变细胞行为
为什么以太脂质对CD44影响显著,但对经典的铁受体影响不大?答案在于物理学。利用能拉出细小膜丝的精密工具,作者显示富含以太脂质的膜张力较低,更易变形。当去除以太脂质时,膜张力升高,脂质更加紧密排列,使膜变得更坚硬。这些变化强烈阻碍依赖于柔性、类似“筏状”膜片的内吞形式——正是CD44所使用的方式——而对基于网格蛋白的摄取影响较小。以太脂质还帮助稳定“脂筏”,即膜中CD44聚集并准备被内吞的微小有序岛屿。简言之,以太脂质调整了膜的物理景观,从而有利于CD44驱动的铁摄取。
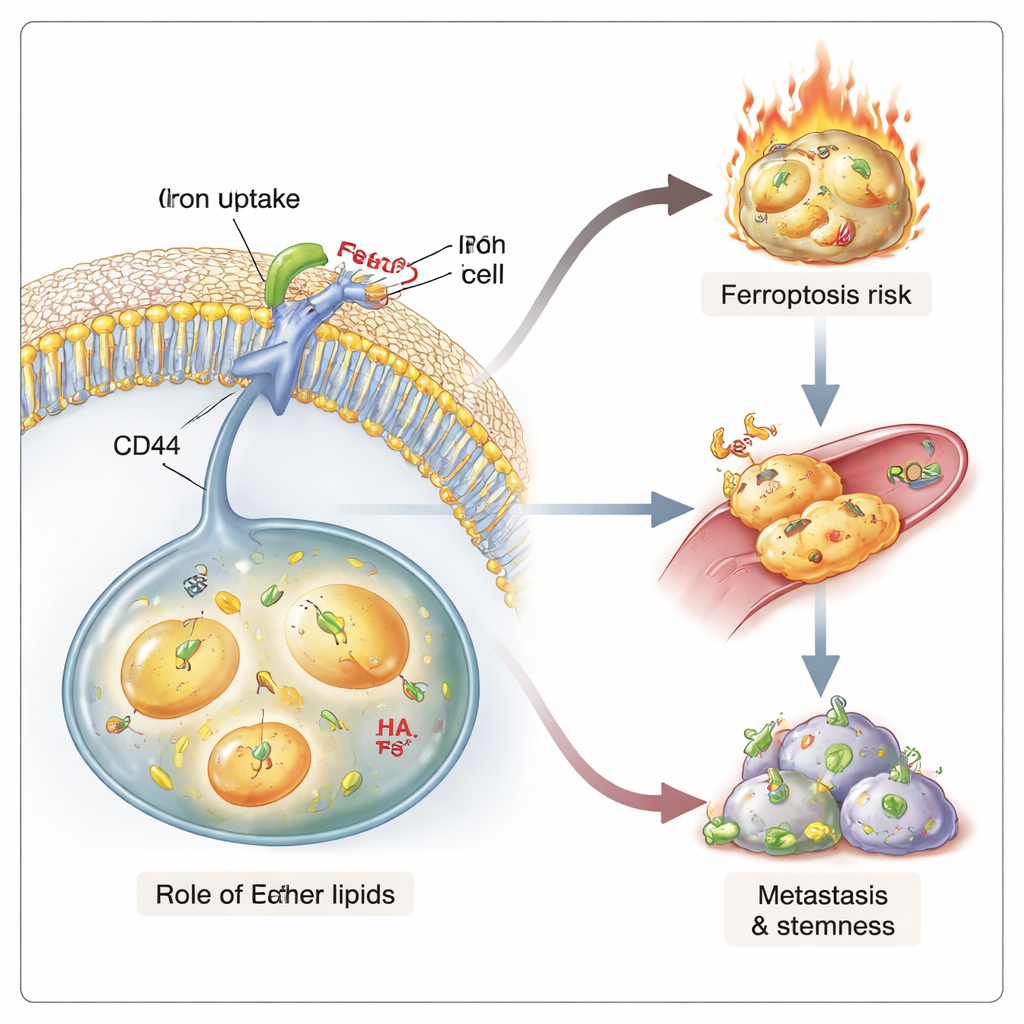
既助长扩散又促成自我毁灭
高铁含量和低膜张力与使癌症致命的性状有关:在新处种植肿瘤的能力和对疗法的生存能力。在三维微血管模型中,富含以太脂质的癌细胞更容易从类血管结构中挤出——这是转移的早期步骤。在小鼠体内,缺乏以太脂质的癌细胞形成的转移灶更少,尽管其原发肿瘤的生长速度相近。这些细胞的“干性”也下降,表现为在培养中形成乳球的能力减弱以及在稀释接种实验中启动肿瘤的能力降低。与此同时,富含以太脂质的细胞由于携带更多可被氧化的脂质和更高的铁负荷,在遇到特定药物或免疫信号时更容易发生铁死亡。因此,以太脂质创造了一种双刃状态:它们支持侵袭性、干样的行为,同时通过铁驱动的脂质损伤使这些细胞变得可以被选择性杀死。
这对未来癌症治疗意味着什么
对非专业读者来说,核心信息是:并非所有癌细胞同样危险,细胞外膜有助于决定它们的威胁性和脆弱性。以太脂质重塑细胞表面,使铁可以通过一扇专门的门流入,既为转移性、干样细胞提供能量,又使它们积累自我毁灭的原料。通过改变以太脂质的生成、破坏基于CD44的铁摄取,或谨慎诱导铁死亡,疗法有望选择性靶向这些难治的癌细胞群体,同时尽量保护正常组织。通过揭示这类鲜为人知的脂质如何将膜物理学、金属代谢与细胞命运联系起来,这项研究为更聪明、更精确的癌症干预开辟了新路径。
引用: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
关键词: 以太脂质, 癌症干细胞, 铁摄取, 铁死亡, 转移