Clear Sky Science · zh
1,3-和1,4-连接多糖在肠细胞中的摄取依赖于网格蛋白/动力蛋白1/Rab5依赖的内吞作用
为什么大分子糖比我们想象的更重要
许多由植物和真菌糖类(多糖)制成的药物和保健补充剂以片剂或粉末形式口服。几十年来,科学家们普遍认为这些长链、亲水的糖链太大,无法完整穿过肠壁进入血液。本研究推翻了这一教条,表明若干类型的多糖实际上可以利用高度组织化的细胞摄入系统穿过肠细胞——为口服“糖类药物”打开了新的可能性。
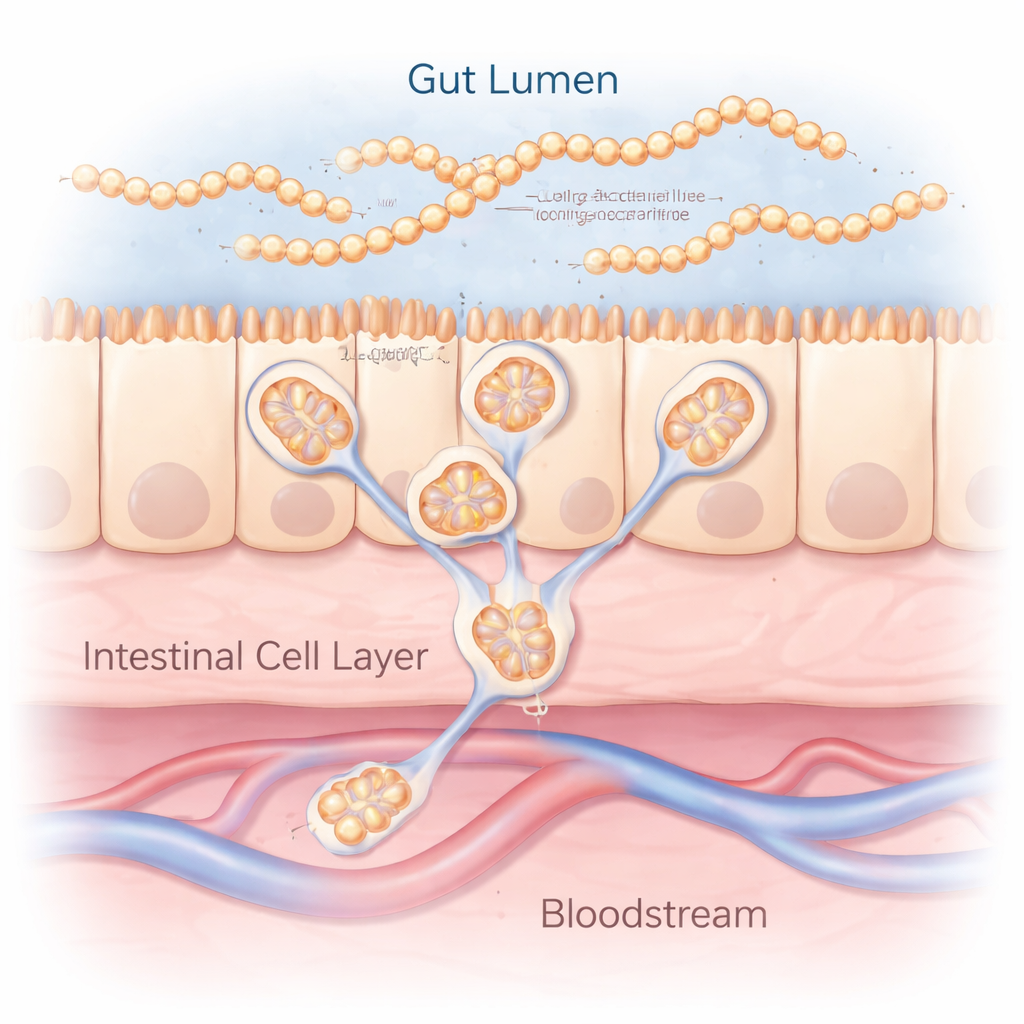
突破常规的长糖链
多糖是由简单糖单元组成的长链,是生命的四大构建模块之一,与蛋白质、脂肪和DNA并列。多糖已构成数十种药物的基础,从像肝素这样的抗凝药到用于关节健康的软骨素硫酸盐。然而大多数多糖需通过注射给药,因为人们认为其体积庞大且高度亲水,口服时无法进入血液。作者针对这一观点,研究了一组具有不同链连接方式和电荷的天然多糖,包括来源于蘑菇的β-葡聚糖(GFPBW1)和来自植物的α-葡聚糖(WGE)作为模型化合物。
穿过肠壁而不被分解
首先,研究团队测试了这些大分子糖是否能穿过生长在膜上、类似人类肠上皮的细胞层。通过化学标记和色谱分析,他们发现多种多糖以出乎意料的高效率通过了细胞层。重要的是,运输前后的“指纹”极为相似,表明这些链并不需要被切割成小片段即可通过。随后研究者在活体大鼠和小鼠中口服给予标记的GFPBW1和WGE。在血样和肝脏组织中,他们检测到完整、被标记的多糖——体积仅有轻微变化——证明至少有一部分这些大分子能经受消化、穿过肠上皮并进入循环系统。
细胞的货物闸门:网格蛋白介导的内吞
这么大的分子如何通过单个肠细胞?研究指向一种称为网格蛋白(clathrin)介导的内吞途径,这一过程通常用于内吞激素、营养物质,乃至病毒。在显微镜下,进入的多糖与网格蛋白共定位,网格蛋白是一种在细胞膜上形成向内芽生小凹陷的支架蛋白。当研究者用化学方法阻断网格蛋白或通过基因工具耗减其重链(CLTC)时,细胞培养中的多糖摄取急剧下降。特异性在肠上皮缺失网格蛋白的转基因小鼠在口服给药后吸收的多糖也显著减少。结合实验还显示模型多糖可直接与网格蛋白结合,进一步支持它们通过这种被覆小窝系统搭载进入细胞的观点。
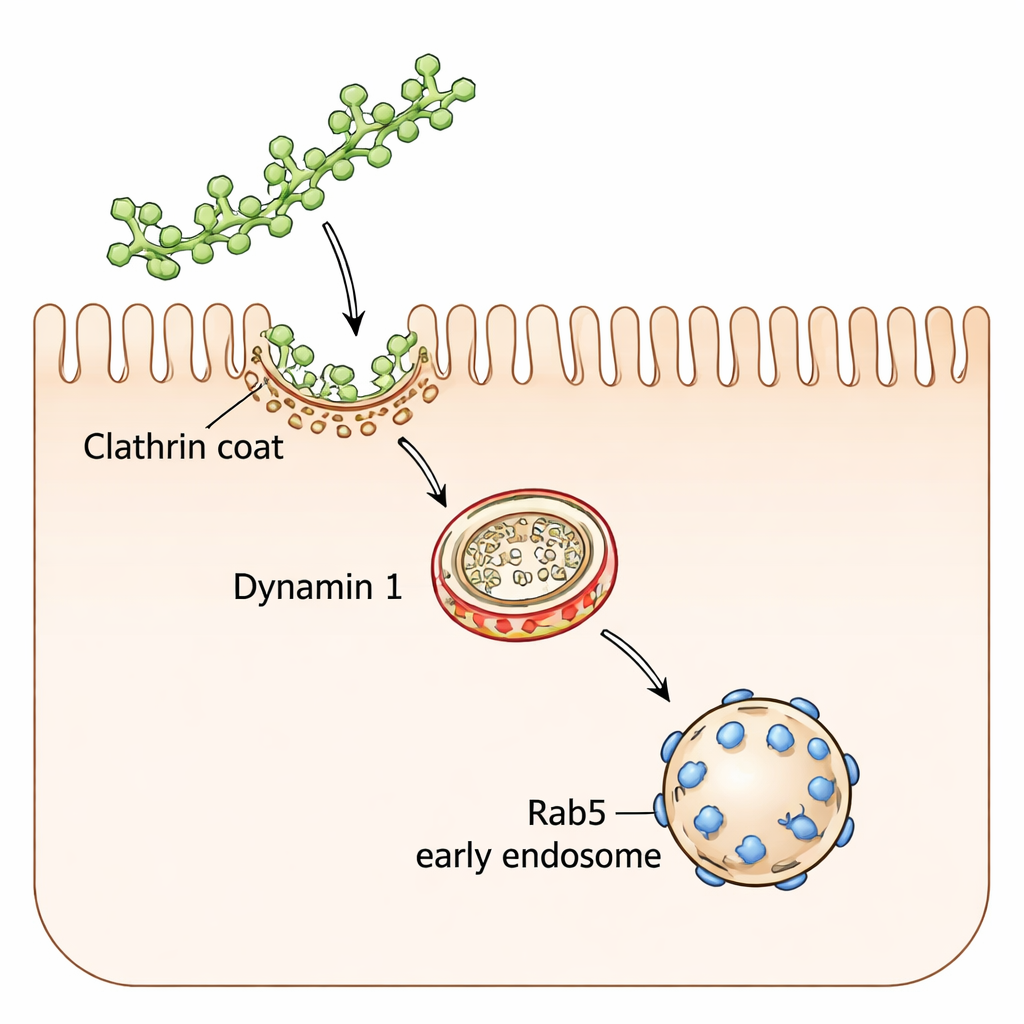
细胞内的关键帮手与交通信号
网格蛋白并非单独行动。动力蛋白1(dynamin 1)——像收紧环一样切断芽生囊泡的蛋白——被证明是必要的:抑制或敲低动力蛋白1会抑制多糖进入,而提高其水平则增强摄取。另一个伙伴Rab5——早期内体的调控者,细胞的初级分拣站——也至关重要。被内吞的多糖常与Rab5共定位,而在所有组织中缺失Rab5的动物显示肠道摄取大大减少。进入细胞后,这些糖通过一系列细胞器运输,包括早期内体、溶酶体(细胞的回收中心)、高尔基体和内质网,尽管在正常肠细胞与类似肿瘤的细胞之间具体路径存在差异。
作为糖类“停靠站”的特异性细胞表面受体
研究还揭示了一层选择性。某些膜受体——负责感知细胞外信号的蛋白——对特定多糖是必需的。免疫受体Dectin-1对β-葡聚糖GFPBW1很重要,而一种称为BMPRIA的生长因子受体在WGE的摄取中发挥主要作用。表皮生长因子受体(EGFR)也支持两种糖的进入,尽管并不总能检测到直接的物理结合,这表明存在更复杂的间接机制。当这些受体被沉默时,相应多糖的摄取下降;当它们被过表达时,摄取增加。此外,细胞内的两条主要信号通路——Wnt/β-连环蛋白和NF-κB——也参与调节细胞内吞糖类的能力。
这对未来片剂和粉末意味着什么
总体而言,该研究表明一些大型天然多糖可以完整地从肠道被摄取进入血液,过程依赖一个以网格蛋白、动力蛋白1、Rab5和特定膜受体为核心的协调系统。对非专业读者而言,关键信息是“太大无法被吸收”并非不可逾越的规则:我们的肠细胞具有可以导入某些复杂糖类的主动通道。理解这些通道及其蛋白帮手,可能有助于设计新的口服可用的多糖类药物和补充剂,使其可靠地到达体内靶点,某些治疗或可因此免除注射给药的需要。
引用: Liao, W., Cao, D., Wang, Y. et al. 1,3-and 1,4-linked polysaccharides uptake in intestinal cells relies on clathrin/dynamin 1/Rab5-dependent endocytosis. Nat Commun 17, 1831 (2026). https://doi.org/10.1038/s41467-026-68542-w
关键词: 多糖吸收, 肠道内吞作用, 网格蛋白 动力蛋白 Rab5, 口服碳水化合物药物, β-葡聚糖摄取