Clear Sky Science · zh
脂肪细胞中骨质抑制蛋白的 loop3-LRP4 相互作用:骨质抑制蛋白干扰全身脂质与葡萄糖代谢所必需
为何骨骼与血糖息息相关
大多数人把骨骼视为无生命的支架,但骨细胞会默默分泌激素,与全身器官交流。这项研究揭示了其中一种骨源蛋白——称为骨质抑制蛋白(sclerostin)——如何将两种在老年女性中常见的问题联系起来:脆弱的骨骼(骨质疏松)与2 型糖尿病。研究者通过揭示骨质抑制蛋白与脂肪细胞之间的特定“握手”机制,勾勒出一种可能在不增加心脏负担的情况下同时强化骨骼并改善血糖与胆固醇的方法。
出问题的骨信号
骨质抑制蛋白主要由骨细胞合成。它通常抑制骨形成,并且有些出人意料地也有助于保护血管。团队集中研究该蛋白的一个小片段,称为 loop3,探讨它是否参与脂质和糖代谢紊乱。他们发现,伴有绝经后骨质疏松且合并2 型糖尿病的女性,以及新诊断的糖尿病患者,其血液中的骨质抑制蛋白水平均高于不伴糖尿病的可比人群。在以高脂饮食模拟代谢压力的小鼠中,随着体重增加、血脂上升和血糖控制变差,骨质抑制蛋白水平也随之升高。这些模式提示,过量的骨质抑制蛋白可能在代谢疾病中不仅仅是旁观者。
解析一个小环却有大影响
为了解 loop3 的功能,研究者构建了骨质抑制蛋白被改变或其 loop3 片段被删除的小鼠模型。过度表达正常骨质抑制蛋白的小鼠在白色脂肪库中堆积更多脂肪,脂肪细胞增大,循环游离脂肪酸升高,葡萄糖耐受性和胰岛素反应比正常小鼠更差。当通过基因手段删除或对 loop3 进行微小突变时,这些问题有所缓解:脂肪垫变小、脂肪细胞缩小、血脂下降、糖代谢改善。令人注意的是,当用一种专门设计的类似 DNA 的药物(适配体)与 loop3 结合并阻断其功能时,也出现了类似的益处,而血液中骨质抑制蛋白的总量并未改变。
脂肪细胞如何“听到”骨信号
研究组随后将视角聚焦到脂肪细胞,观察 loop3 如何传递有害信号。他们关注脂肪细胞表面的一种受体蛋白 LRP4,该受体此前已知可帮助骨质抑制蛋白在骨组织中发挥作用。通过细胞培养实验,他们显示 loop3 能物理结合脂肪细胞 LRP4 的特定部分。此接触触发一系列改变,增强细胞合成与分解脂质的能力并增加从血液中摄取葡萄糖,导致脂肪细胞体积增大且功能过度活跃。当科学家微调 LRP4 中的关键构件使 loop3 无法对接,或加入一种模拟 LRP4 对接位点的小阻断肽时,骨质抑制蛋白对脂肪堆积和糖摄取的影响明显减弱。在细胞和小鼠体内,阻断这一路径恢复了更接近正常的脂肪细胞大小并改善了葡萄糖耐受性。
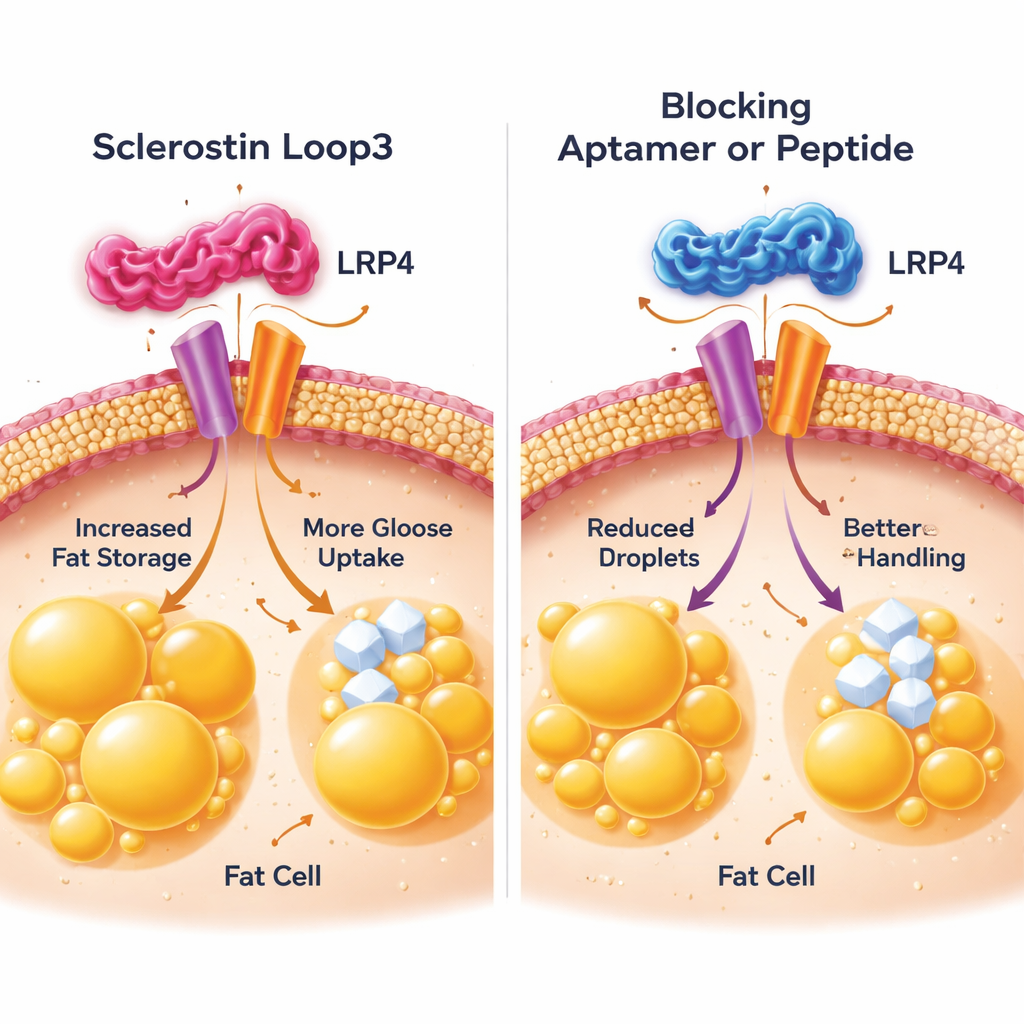
更强的骨骼,更健康的代谢
现有用于治疗骨质疏松的骨质抑制蛋白抑制药物虽然能促进骨形成并改善代谢,但监管机构已警示其可能增加严重心脏事件的风险。该团队早期的工作显示,loop3 对骨质抑制蛋白抑制骨形成的作用至关重要,但并不参与其对心脏的保护作用。本文进一步显示,通过基因修改或针对 loop3 的药物干预可以在多种小鼠模型中改善全身脂质与糖代谢,同时增加骨量与骨强度。与现有药物不同,这一策略未引发另一种骨相关抑制因子 DKK1 的补偿性升高,而 DKK1 的上升会削弱长期疗效。
这对病人意味着什么
简言之,这项研究认为,一种骨源激素的极小片段可通过直接与脂肪细胞对话,推动骨骼健康变差与代谢疾病的发生。通过中断骨质抑制蛋白的 loop3 片段与脂肪细胞上 LRP4 受体之间的交流,可能设计出既能增强骨骼、又能使血脂与血糖恢复正常,同时保留骨质抑制蛋白心脏保护功能的治疗方法。对于常同时面临骨质疏松和2 型糖尿病的绝经后女性,针对 loop3 的疗法未来或能提供一种更安全、持久的双重管理选择。
引用: Jiang, H., Tao, X., Yu, S. et al. Adipocytic sclerostin loop3-LRP4 interaction required by sclerostin to impair whole-body lipid and glucose metabolism. Nat Commun 17, 1812 (2026). https://doi.org/10.1038/s41467-026-68526-w
关键词: 骨质抑制蛋白, loop3, LRP4, 骨质疏松, 2 型糖尿病