Clear Sky Science · zh
棕榈酸触发的 B7H3 棕榈酰化促进免疫逃逸
这项研究为何对癌症患者重要
大多数人都听说过新型免疫疗法可以帮助免疫系统攻击癌细胞,但许多常见的结直肠(肠)癌患者收效甚微。本研究揭示了结直肠肿瘤用以抵御免疫攻击的一种隐蔽生化伎俩,并指出了一类新型药物——小肽——可能使免疫疗法对这些患者更有效。
当前肠癌免疫疗法的障碍
结直肠癌是全球最常见的癌症之一。像 PD-1 和 PD-L1 抑制剂这样的免疫“刹车”解除药物,已经改变了少数携带大量 DNA 错误(即 MSI-H 肿瘤)患者的治疗效果。不幸的是,大多数结直肠癌为微卫星稳定型(MSS),对这些治疗反应不佳。作者把注意力集中在另一种刹车分子 B7H3 上,它位于肿瘤细胞表面,抑制杀伤性免疫细胞,尤其是 CD8+ T 细胞的活性。他们发现 B7H3 蛋白在 MSS 肿瘤中明显升高并与更差的生存相关,即便 B7H3 基因的转录并未增加。这种不一致引出了一个关键问题:是什么使肿瘤细胞中 B7H3 蛋白如此丰富?
一种常见脂肪如何帮助肿瘤伪装
研究团队怀疑肿瘤代谢可能在稳定 B7H3 中发挥作用。通过比较 MSS 与 MSI-H 结直肠肿瘤的基因表达与小分子谱,他们发现许多与脂质相关的通路存在差异,其中一种脂肪酸——棕榈酸——尤为突出。在体外将结肠癌细胞暴露于多种脂肪分解产物时,只有棕榈酸显著提高了 B7H3 蛋白水平。进一步实验揭示了原因:棕榈酸参与一种称为棕榈酰化的化学修饰过程,在该过程中一条脂肪链被连接到蛋白质的特定位点。该修饰由酶 ZDHHC24 在 B7H3 的单个半胱氨酸位点完成,使 B7H3 更加稳定并在肿瘤细胞表面累积。
阻断“垃圾”通路以消灭免疫刹车
细胞通常通过类似回收和垃圾处理的系统清除不需要或受损的蛋白。研究者表明 B7H3 主要通过一种称为自噬的“自我吞噬”通路降解,该通路使用受体蛋白 SQSTM1/p62 将靶物标记以便销毁。当 B7H3 被棕榈酰化时,它与该受体结合较差,从而逃避自噬降解,导致免疫刹车长期高表达。若将棕榈酰化位点突变以阻止脂肪标记,或删除 ZDHHC24 酶,B7H3 更容易被导入细胞的“垃圾袋”并被降解。在小鼠模型中,缺乏棕榈酰化 B7H3 的肿瘤生长更慢,在免疫缺陷动物中其固有生长速率未改变,但表现出显著更多的 CD8+ T 细胞和更强的肿瘤杀伤活性。这说明该修饰主要通过削弱免疫反应起作用,而非改变癌细胞的增殖速度。
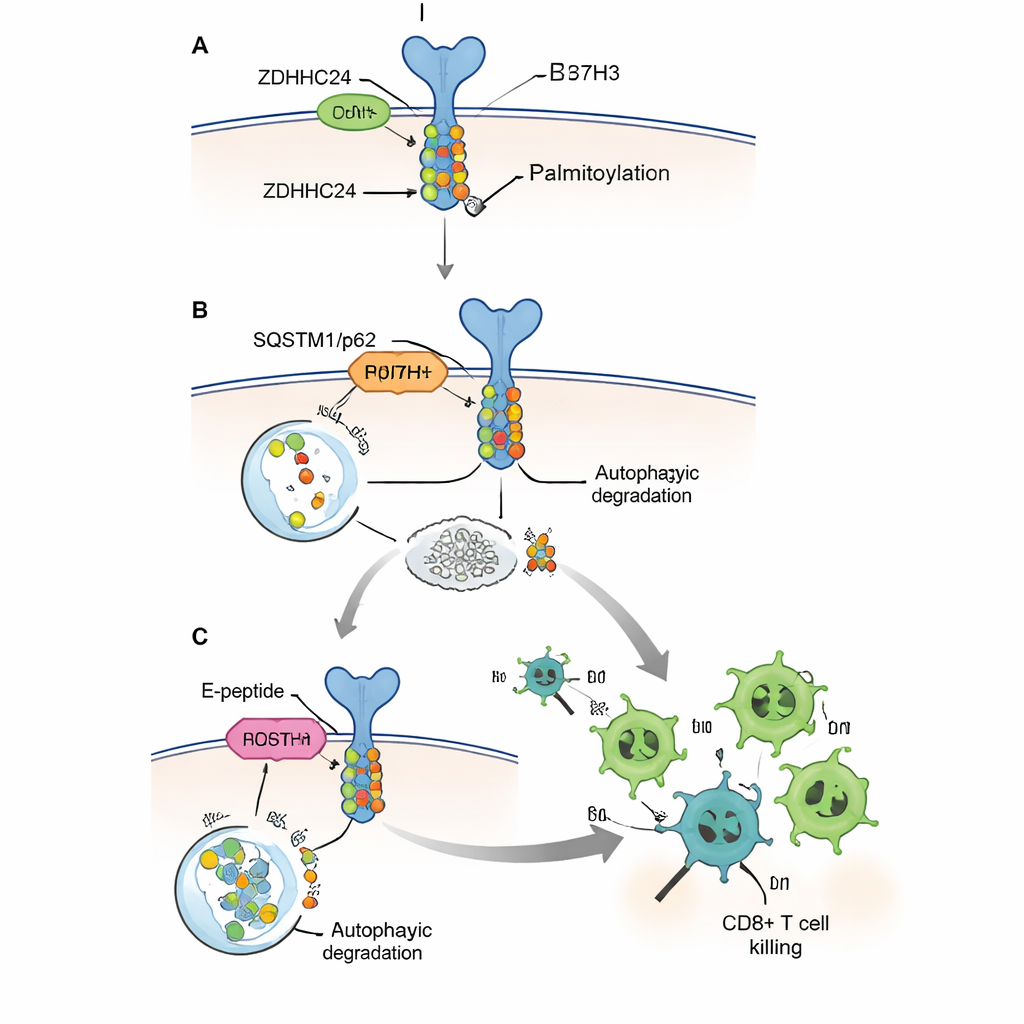
降低防护屏障并增强 T 细胞
由于在患者中完全用基因方法消除 ZDHHC24 或 B7H3 不现实,作者设计了一种短小、能穿透细胞的肽,称为 E-肽。它模拟 B7H3 蛋白中一段通常与 ZDHHC24 结合的小片段,作为诱饵阻止该酶修饰真实的 B7H3 分子。在培养细胞中,E-肽降低了 B7H3 的棕榈酰化和蛋白水平,恢复了其被自噬识别的能力,使人类 CD8+ T 细胞更有效地杀死肿瘤细胞。在包括带有人体免疫细胞与人源结直肠肿瘤的人源化小鼠在内的多个小鼠模型中,注射 E-肽可缩小肿瘤、增加肿瘤内 CD8+ T 细胞数量,并提升颗粒酶 B 与干扰素-γ 等关键杀伤分子的产生。
作为现有免疫疗法的新搭档
最后,研究者探讨了该策略能否与常规 PD-1 阻断并用。在结直肠癌小鼠模型中,单独使用 E-肽或单独使用抗 PD-1 抗体都能在一定程度上控制肿瘤。但当两者联合使用时,治疗产生了更强且更持久的肿瘤抑制,在某些情况下导致肿瘤消失,并使平均生存期较对照组增加超过一倍。这表明通过切断 B7H3 的脂肪“锚”来解除其防护可以补充靶向 PD-1 通路的现有检查点药物。
对未来癌症治疗的意义
简言之,这项研究表明一种常见的膳食脂肪——棕榈酸——可以被结直肠肿瘤劫持,用来化学性地装甲一种免疫阻断蛋白(B7H3),帮助癌症躲避免疫系统。通过阻断这一单一的化学附着,作者能够剥掉这层护甲,使细胞自身的清除系统移除 B7H3,并重新开放 CD8+ T 细胞的攻击通路。虽然 E-肽本身仍是早期实验工具,但这项工作确定了 B7H3 棕榈酰化及其酶 ZDHHC24 为有前景的药物靶点。如果类似药物在人体中被证明安全且有效,未来有可能将更多对免疫疗法“冷漠”的结直肠癌转变为免疫系统可识别并消灭的“热”肿瘤。
引用: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
关键词: 结直肠癌免疫疗法, B7H3 检查点, 棕榈酸代谢, 蛋白质棕榈酰化, CD8 T 细胞肿瘤免疫