Clear Sky Science · zh
斑马鱼巨噬细胞将物理伤口信号转化为快速的血管通透性增加
一条小鱼如何教会我们关于伤口肿胀的知识
当你擦伤膝盖时,受伤区域会迅速变红、肿胀并渗出液体。附近血管的这种快速变化对于抵抗感染和启动修复至关重要,但身体如何在几秒钟内感知损伤并作出反应,实时观察一直很困难。通过使用透明的斑马鱼幼体和先进的活体成像,这项研究揭示了缠绕在血管周围的专门免疫细胞如何将伤口的物理冲击转化为几乎瞬时的血管渗漏,为炎症、愈合乃至人类肺损伤提供了新的见解。
观察损伤如何在体内传播
研究人员使用透明体的幼年斑马鱼,这使得科学家能够在显微镜下观察细胞和血管的活动。他们切下尾鳍尖端,并在循环系统中注入一种能在健康血管内保持的荧光染料。当受伤的鱼被放回普通淡水中时,组织中突然进入的水造成了伤口周围的“渗透冲击”。数分钟内,附近血管扩张并开始将荧光染料渗入周围组织,模拟了人类伤口周围发生的肿胀和渗出。通过在普通和特殊平衡的盐或糖溶液之间切换鱼体,研究团队证明了这种快速的血管通透性增加强烈依赖于渗透性变化,而不仅仅是组织撕裂。
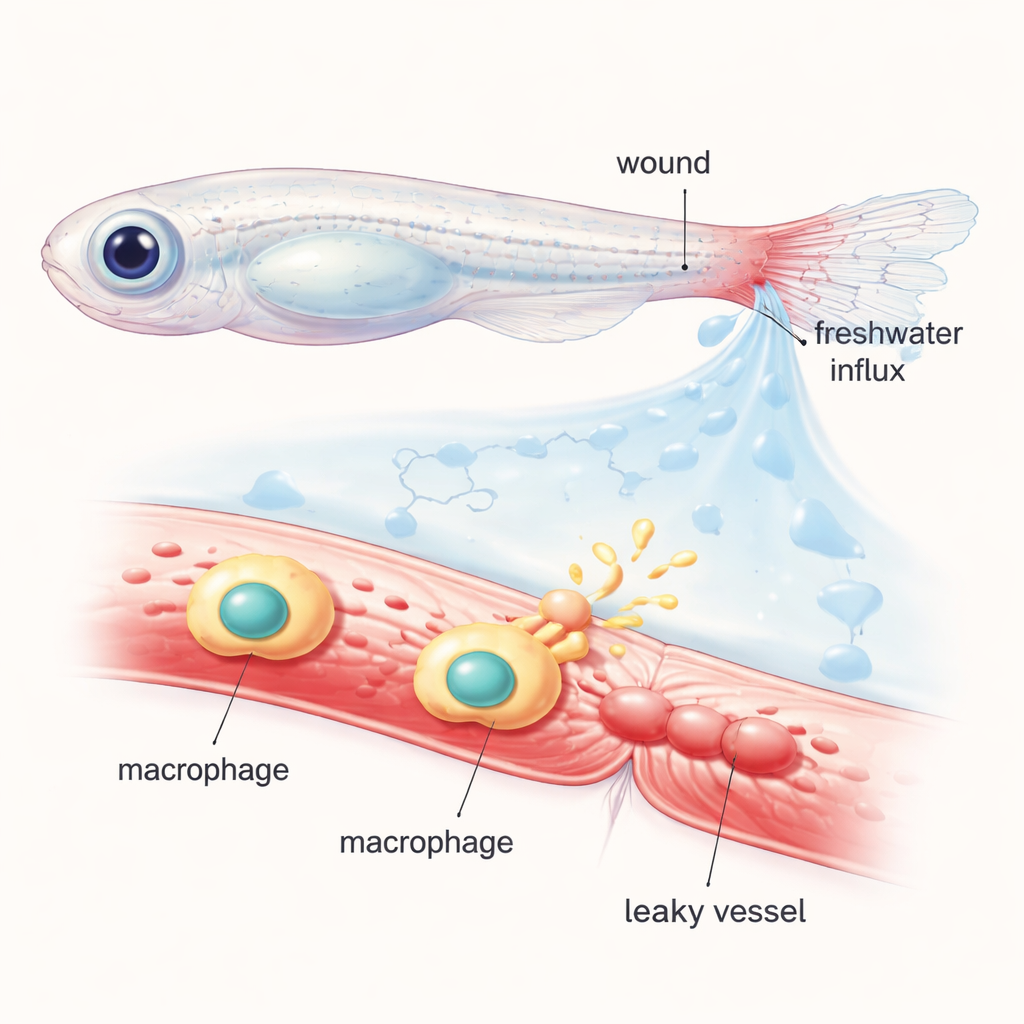
追踪导致渗漏的化学信使
为了找出哪些分子将物理冲击转化为渗漏信号,科学家们考察了一类由花生四烯酸生成的脂类化合物——二十碳烯酸类(eicosanoids)。这些脂质在炎症和血流调节中作用显著。研究中通过遗传突变和药物手段,选择性抑制了该代谢通路中的个别酶。阻断一个关键酶Alox5a(5-脂氧合酶)或其伴侣Lta4h,会明显减少渗透冲击后从血管中逸出的染料量,但不影响伤口本身的闭合。相比之下,干扰其他相关酶影响甚微。这指向了脂类通路的一个特定分支,作为快速渗漏反应的主要驱动者,类似于一个可按需开启或关闭的化学阀门。
紧贴血管的免疫细胞的意外作用
血液中有多种免疫细胞,在斑马鱼幼体中,中性粒细胞和巨噬细胞是主要角色。研究团队用一种巧妙的遗传方法在受伤前选择性地消除中性粒细胞或巨噬细胞。除去中性粒细胞对血管渗漏影响不大。但当巨噬细胞被清除时,渗漏反应下降约一半,这与阻断Alox5a–Lta4h脂质通路的效果相呼应。重要的是,这些操作并未阻止伤口快速闭合,表明白细胞募集与血管渗漏可以在一定程度上独立调控。这揭示了血管周围的巨噬细胞——紧贴血管外表的巨噬细胞——作为物理损伤与血管行为之间的关键“翻译者”。
从细胞核拉伸到化学信号
这些血管周围的巨噬细胞如何探测到可能远处的伤口?答案在于它们细胞核对机械应力的响应方式。当来自伤口的渗透冲击在附近组织中传播时,水分进入导致细胞轻微膨胀和细胞核形变。研究人员将一种机械感受性酶cPla2用荧光标记,并在巨噬细胞中特异性表达。在正常淡水环境下受伤后,cPla2迅速沿着细胞核内膜转位,在组织中以约每秒50微米的速度形成一波,匹配溶解盐类的扩散速度。此转位依赖低渗条件,在等渗溶液中则弱得多。靠近血管的巨噬细胞显示出尤其剧烈且可逆的核内cPla2结合脉冲,进而释放花生四烯酸以转化为引发渗漏的脂质分子。
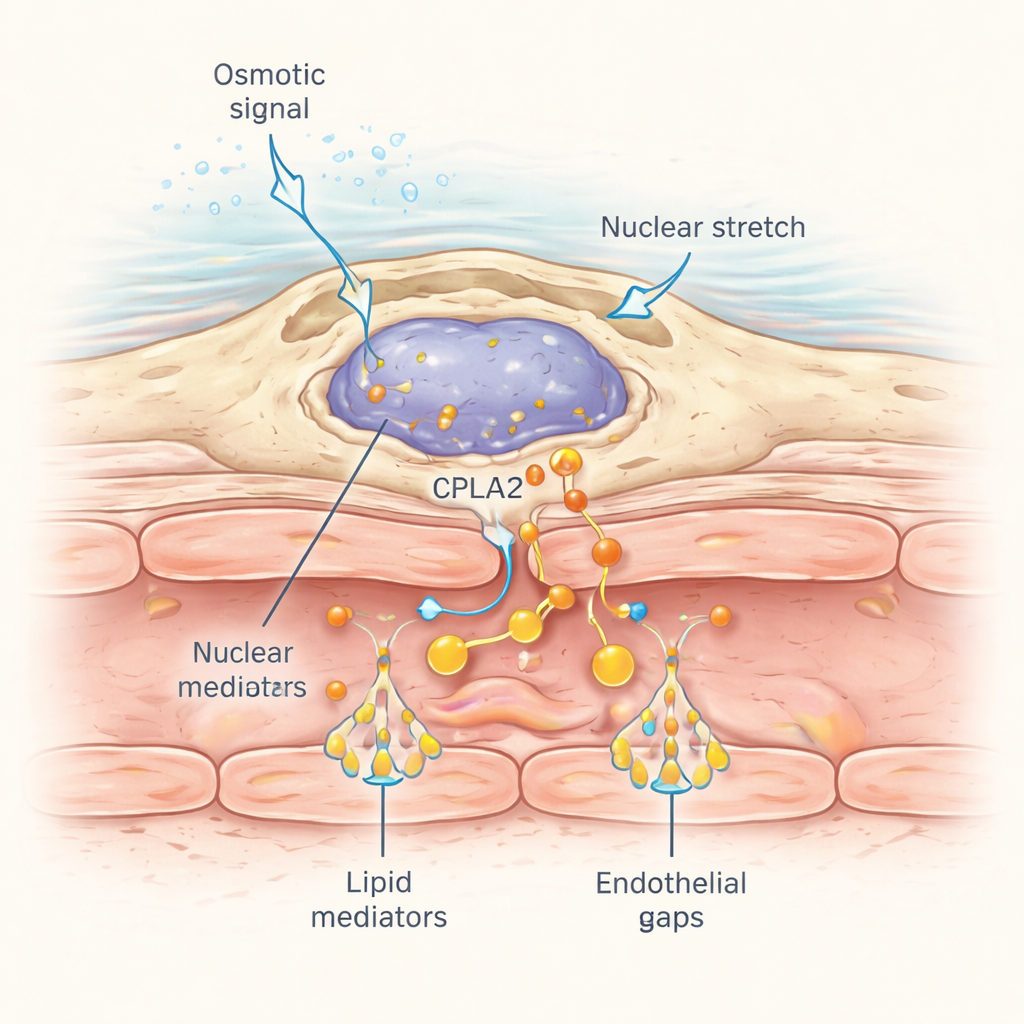
这项工作为何超越鱼类而重要
简而言之,这项研究表明某些巨噬细胞充当物理哨兵:它们感知由伤口引起的组织和细胞核膜的拉伸,在其核表面激活cPla2,并迅速产生脂质信使,指示附近血管“打开闸门”,让液体和免疫因子涌入。尽管斑马鱼生活在淡水中并面临独特的渗透挑战,但类似的机械感受通路很可能在人类组织中也存在,尤其是在像机械通气时肺部遭受变化的压力和流动的情况下。理解细胞核拉伸与脂质信号如何实时控制血管通透性,最终可能为调整炎症的治疗提供依据——既可以抑制急性肺损伤等病症中的有害渗漏,也可以增强有益反应以加速组织修复。
引用: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
关键词: 伤口愈合, 血管, 巨噬细胞, 炎症, 斑马鱼