Clear Sky Science · zh
用于微秒时间分辨冷冻电子显微镜的超薄液体腔
实时观察蛋白质的工作状态
维持细胞生命的许多分子机器由蛋白质构成,我们经常知道这些蛋白质在被“冻住”时的样子。但我们真正想看的是它们在执行功能时如何运动。本研究引入了一种新方法,可在极短的时间尺度——百万分之一秒——内观测这些运动,同时不牺牲现代冷冻电子显微镜(cryo‑EM)所能达到的锐利细节。
显微世界的新窗口
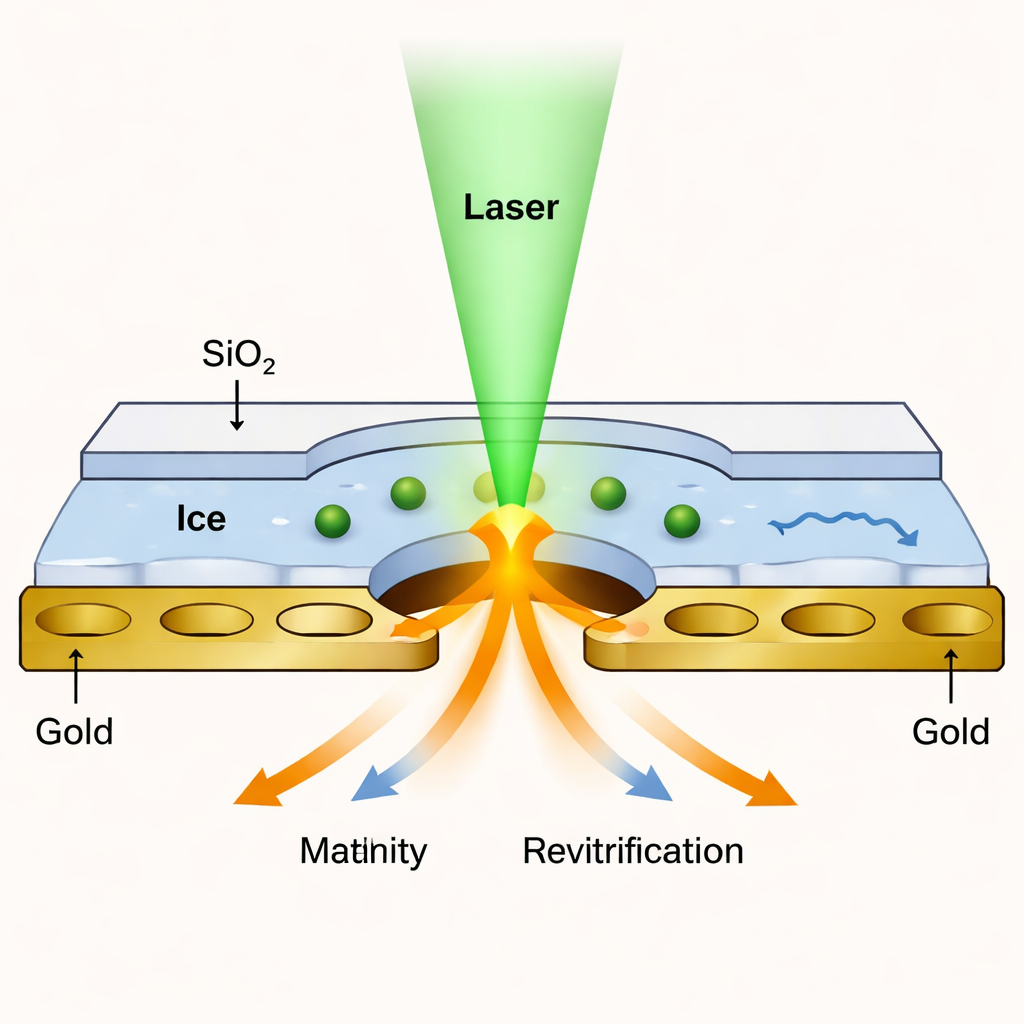
冷冻电子显微镜通过以近原子分辨率成像快速冷冻的蛋白质,已在结构生物学领域带来革命性变化。然而,传统方法只能显示静态画面。为捕捉运动,研究者开发了“微秒时间分辨冷冻电子显微镜”——用激光短暂熔化冰层让蛋白质发生位移,然后迅速再冻结以将新构象捕获。问题在于,激光产生的微薄液膜往往在几十微秒后分裂,限制了可观察的时间长度。新工作通过将样品封装在超薄液体腔中解决了这一瓶颈,使液层在更长时间内保持稳定,从而能够观察更慢、更复杂的运动。
构建超薄液体腔
研究团队制备了一种纳米级的“三明治”结构:蛋白溶液先在标准的穿孔金网格上冷冻,然后两侧覆上一层约 1.4 纳米厚的二氧化硅——仅几层原子。这些类似玻璃的薄层充当透明的盖子,在激光熔冰时防止液体挥发。短脉冲激光将密封样品加热到受控温度,然后在微秒级内重新冻结。由于膜极薄,它们仍允许足够的电子透过,使显微镜能产生与常规 cryo‑EM 几乎相同的分辨率——对测试蛋白 apoferritin 可达约 1.7–1.8 埃。
更清晰的视野与更均匀的取向
冷冻电子显微镜中的一个隐性挑战是,蛋白质倾向于粘附在薄冰层的水-气界面,上下排列出类似方向,这使得重建完整三维结构变得困难。液体腔中的二氧化硅涂层将界面从水-气变为水-固,并使表面更亲水。因此,蛋白质不太可能以单一构象粘附。作者在测试大型细胞机器 50S 核糖体亚基时发现,颗粒的取向分布几乎变得完全均匀,基本消除了长期存在的“优选取向”问题,同时在最终重建中仍然保持高分辨率。
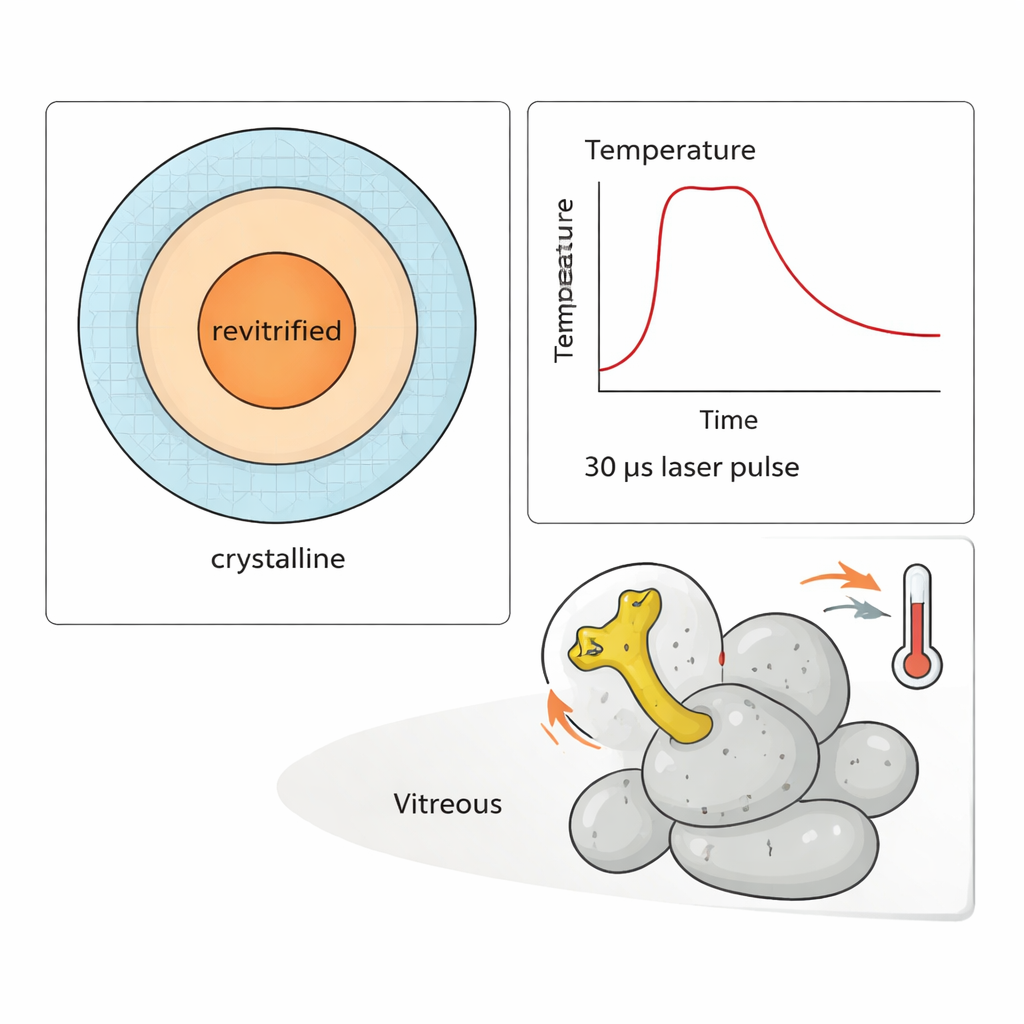
给分子杠杆计时
为展示方法的威力,研究者对 50S 亚基进行了“温度跳变”实验。该颗粒上的一根柔性臂——称为 L1 臂——在蛋白质合成过程中像杠杆一样摆动。通过发射一系列 30 微秒的激光脉冲,他们能将样品加热到不同温度,持续时间最多约 300 微秒,然后再冻结。对哪些区域已重新冻结成玻璃态的模拟和测量使他们能够估算每个观测到颗粒的温度。分析数千张图像显示,L1 臂摆动的振幅随温度明显增大——但这一变化只在数百微秒之后才出现。在早期时间点,构象分布仍反映冻结前的室温状态。
这对未来生物学的重要性
对非专业读者而言,关键结论是,这种超薄液体腔设计显著延长了在不模糊结构细节的前提下观测蛋白质运动的时间。它将微秒时间分辨 cryo‑EM 从仅能捕捉最快事件,扩展到可以探测诸如 L1 臂对热脉冲的延迟响应等较慢、具有生物学意义的重排。通过进一步改进,这一方法可能将时间尺度推进到毫秒甚至更长,并提供新的样品制备方式、减少成像伪影以及在网格上直接触发反应的途径。实际意义上,这意味着科学家离制作将蛋白质形状与其在活细胞中实际功能联系起来的“分子电影”又近了一步。
引用: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
关键词: 时间分辨冷冻电子显微镜, 蛋白质动力学, 液体腔电子显微镜, 核糖体 L1 臂, 超薄二氧化硅薄膜