Clear Sky Science · zh
仿生Janus水凝胶通过机机械-免疫时空调控驱动感染的跟腱再生
这对受伤腱体为何重要
跟腱断裂在运动员和老年人中都很常见,当伤口被细菌感染时,愈合常常不理想:腱体可能变弱、与周围组织粘连,甚至再次断裂。这项研究提出了一种新的“智能”水凝胶敷料,灵感来自腱体自身的天然鞘膜,可在手术中直接涂覆于被感染的跟腱上。它旨在同时完成三项工作:在机械上保护腱体、杀灭耐药细菌,并温和地引导免疫系统从有害的炎症状态转向真正的再生。
受自然启发的双面敷料
健康的腱体位于一层光滑的鞘膜内,这使其能够在保持固定的同时平滑滑动。外科医生在修复后难以复制这一点:容易黏附在腱体上的材料往往也会粘到周围组织,导致疼痛性的粘连。研究者用一种名为HAPP@H-EXO的Janus(两面)水凝胶复制了这种天然的“黏附与润滑”设计。一面通过可逆化学键和氢键与腱表面牢固结合,提供坚实的机械支撑。另一面采用类似莲叶的处理,具有疏水和低摩擦特性,使周围组织不易粘附。这就形成了一个随腱体运动但能抵抗周围瘢痕形成的保护套。 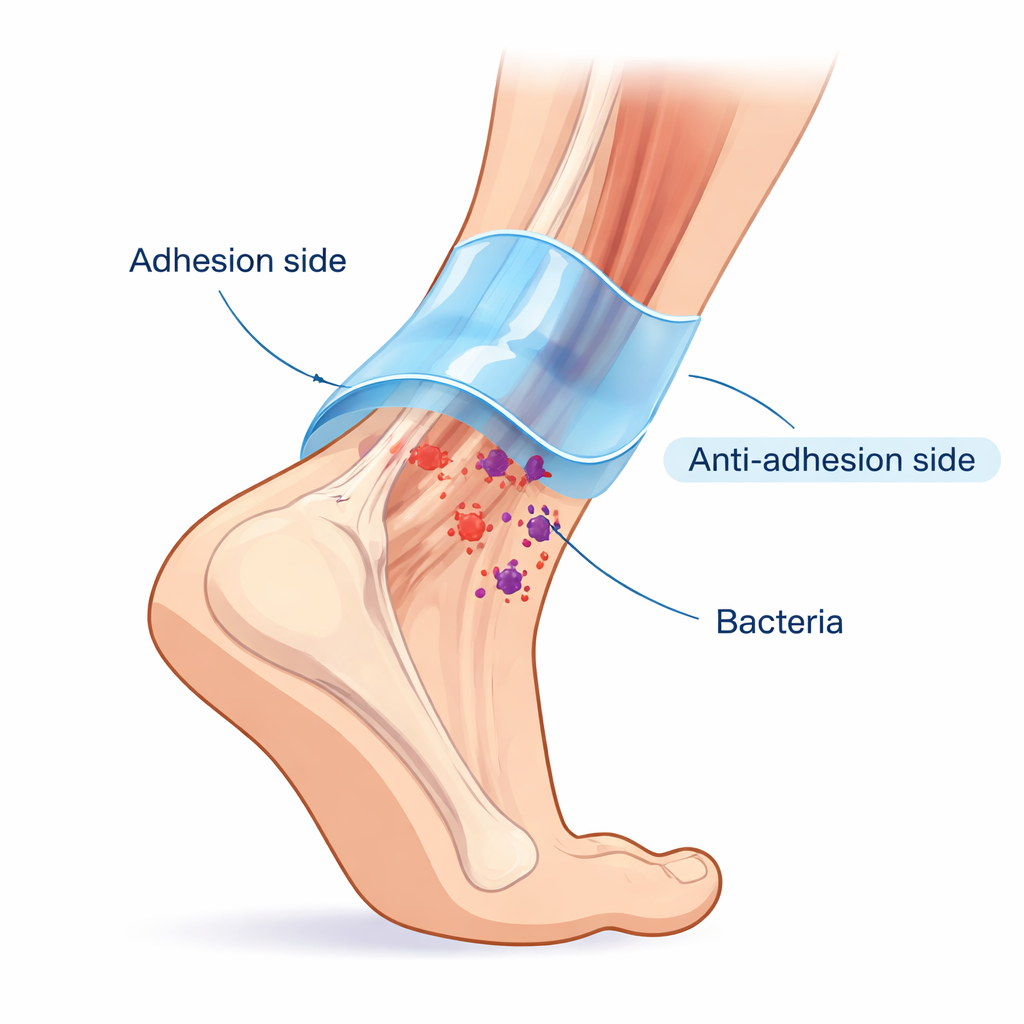
为分担载荷并承受反复拉伸而设计
与许多软凝胶不同,这种材料被设计用于严苛的机械环境:每一步行走都会对跟腱施加载荷并释放。研究团队将一个刚性、永久交联的网络与第二个可在应力下重排的动态网络结合。测试显示该水凝胶能在拉伸和压缩时不易断裂,在至少100次受力循环中保持强度,并且能量耗散较少,这意味着它能够回弹而不是缓慢变形。计算机模拟表明,当该凝胶包裹在缝合的腱体周围时,凝胶会将缝合点处的高应力向腱体边缘扩散,降低修复处再次断裂的风险。在动物实验中,这转化为修复后的腱体在强度和刚度上接近正常组织。
捕捉细菌并抗击耐药性
细菌感染是腱修复失败的主要原因,尤其由耐多药菌株如MRSA引起时。研究者没有依赖传统抗生素,而是让水凝胶通过物理方式捕捉并杀死细菌。其中一种成分——苯硼酸基团——能识别细菌细胞壁上富含糖的结构并与之形成可逆键,将细菌从周围液体中“拉出”。另一种成分为带正电的聚合物,随后破坏细菌膜,使其破裂。在体外测试中,该凝胶能迅速杀死MRSA、常见金黄色葡萄球菌和大肠杆菌,分解顽固的生物膜,并在多日和多次使用循环中保持其抗菌效力,同时未诱导细菌对捕捉或杀灭机制产生耐药性。 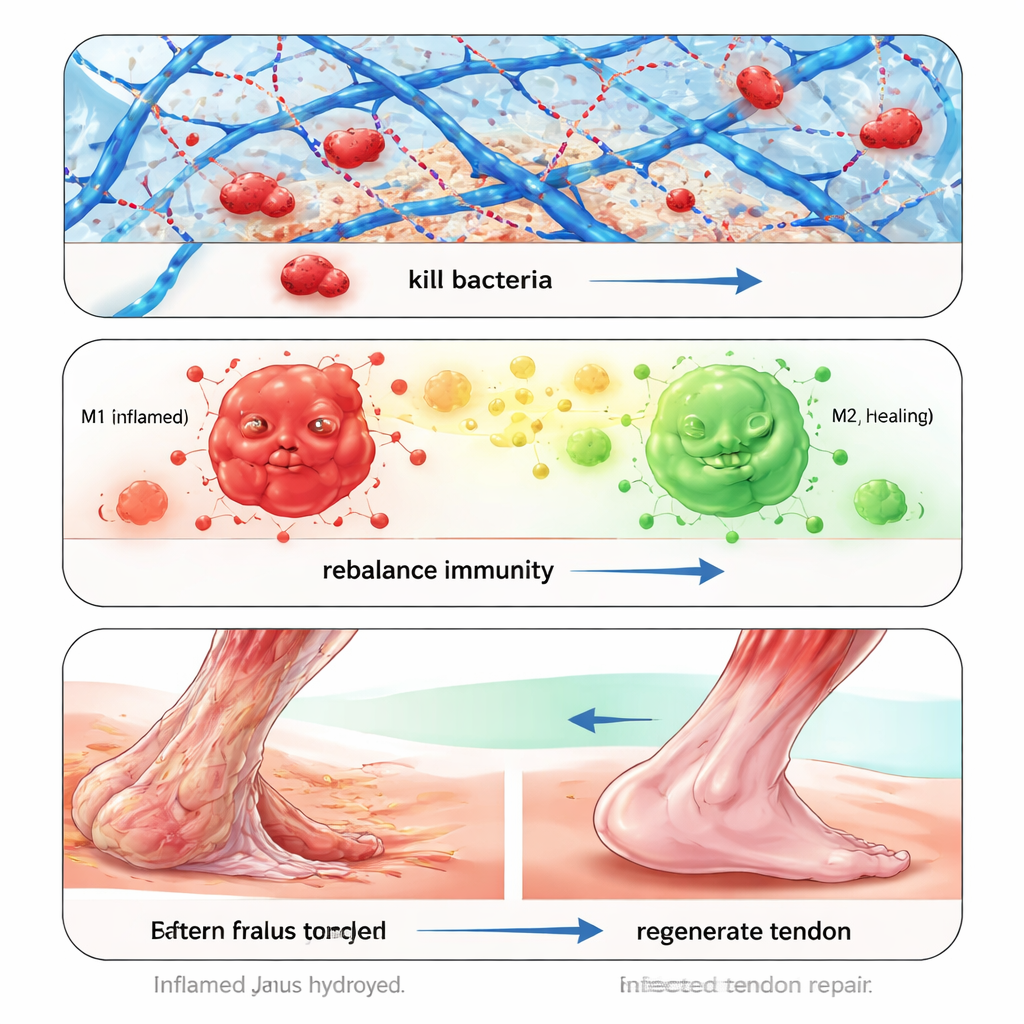
引导免疫系统并重建组织
即使细菌被清除,受感染的腱体常常仍处于氧化应激和慢性炎症状态,这会阻碍正常修复。为此,研究者在水凝胶中装载了来自在低氧条件下培养的腱干细胞分泌的小膜囊—外泌体。这些“缺氧”外泌体富含抗炎和促再生信号。凝胶的化学性质使其在酸性、炎症早期阶段更快释放外泌体,而在条件恢复正常时释放更慢。在细胞实验中,负载外泌体的凝胶减少了有害的活性氧,恢复了线粒体功能,促进血管形成,并将免疫细胞从促炎状态(M1)推向愈合状态(M2)。基因分析显示,NF-κB通路——炎症的核心驱动之一—受到抑制。
从感染断裂到功能性恢复
在故意用MRSA感染的鼠和兔跟腱断裂模型中,手术中应用Janus水凝胶在一周内几乎清除了伤口处的活菌。随后的数周内,处理组腱体表现出更少的氧化损伤、更低的炎症标志物以及更多的促愈合信号。显微镜观察显示胶原纤维排列更好且更粗,血管更多,并且表达了关键的腱成熟相关蛋白。重要的是,凝胶的外层不粘面防止了腱体与周围组织粘连,这一点通过成像和肉眼检查得到证实。接受外泌体负载版本处理的动物恢复了更接近正常的步态模式和更高的腱承载能力,表明不仅结构上得到修复,功能也得到恢复。
这对患者可能意味着什么
这项工作展示了一种将机械支撑、感染控制和免疫平衡整合于一体的仿生材料。通过将双面物理设计与捕菌化学和时序释放的再生外泌体相结合,Janus水凝胶帮助感染的跟腱在动物中更强健地愈合、减少瘢痕并改善运动功能。尽管仍需进行人体试验,但这一方法提示了一个可期的未来:复杂的软组织损伤,尤其是伴随耐药性感染的情况,可能通过这种能够主动协调愈合过程的“智能”外科敷料得到治疗。
引用: Li, J., Wang, Z., Yang, W. et al. Bionic Janus hydrogel drives infected Achilles tendon regeneration via mechano-immune spatiotemporal steering. Nat Commun 17, 1805 (2026). https://doi.org/10.1038/s41467-026-68514-0
关键词: 跟腱修复, 水凝胶敷料, 耐药性感染, 组织再生, 免疫调节