Clear Sky Science · zh
细胞间肽自组装产生的机械力驱动球体形成
在实验室构建微型组织
科学家们正加速制造行为与真实组织相似的人体微型模型。这些活体模型可以使癌症药物的测试更安全,并将糖尿病及其他疾病的新疗法推向现实。本研究提出了一种巧妙的方法,诱导细胞形成逼真的三维簇块,并在其中建成原始的“类似血管”网络,改善营养供应和功能。
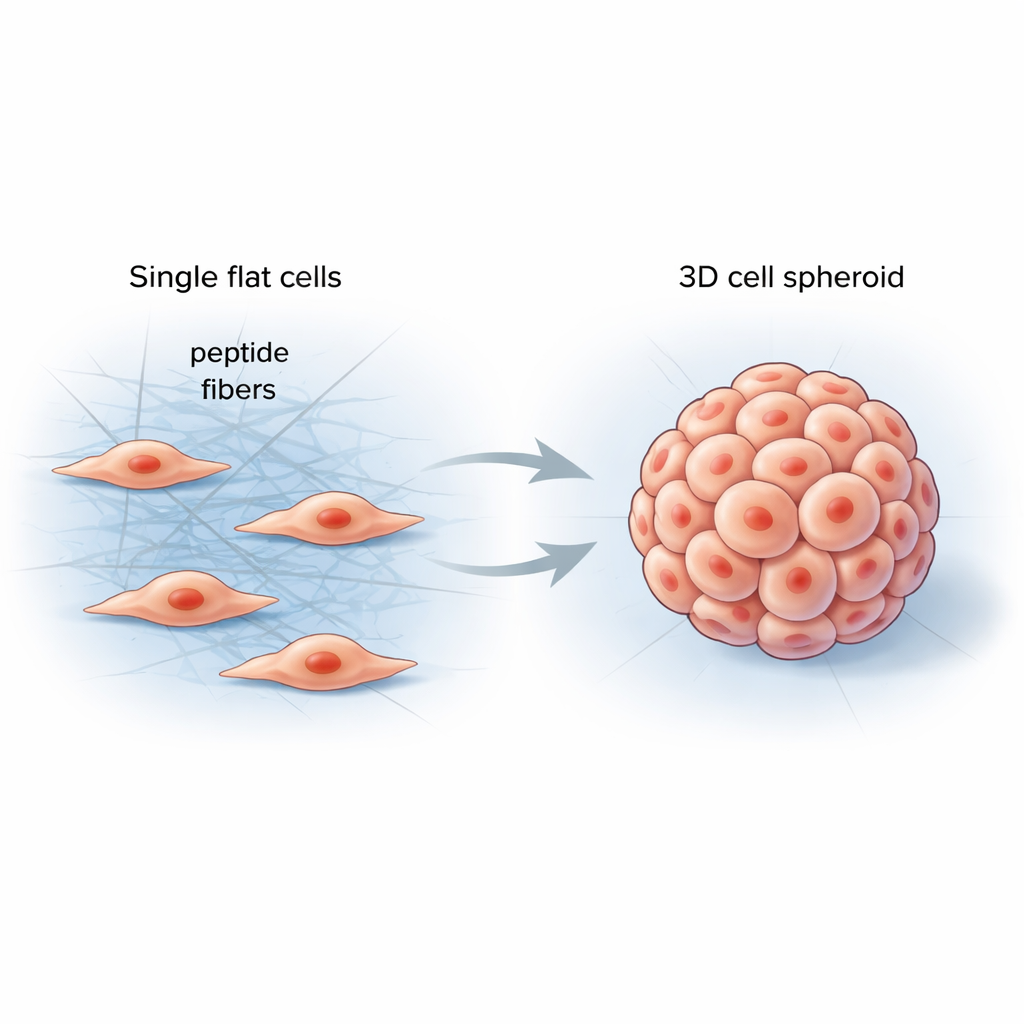
帮助细胞感知周围环境
在我们体内,细胞生活在一种既柔软又有结构的环境中,称为细胞外基质——它是由蛋白质构成的网状结构,支撑组织并持续向细胞传递机械信号。常规模拟材料难以复制这种复杂性,经常产生与真实器官或肿瘤行为差异很大的平面细胞层。研究者旨在设计一种简单且可编程的材料,能在细胞之间直接形成,受控地改变周围刚度,并推动细胞趋向更自然的三维形态。
在细胞之间自组装的智能肽
团队设计了短肽——短的蛋白片段,它们在遇到细胞表面的特定酶时能连接成细长纤维。当这些肽被加入到癌细胞中时,起初保持不活跃,像透明溶液一样。一旦细胞自身的酶切除分子的一部分,肽便迅速自组装成包裹并连接相邻细胞的纤维网络。新的纤维网改变了局部机械力,促使细胞相互牵拉、重塑内部支架,并聚集成圆形的三维球体,而不是铺展成一层薄片。
从细胞簇到类血管网络
为了更接近真实组织,科学家随后引入了人内皮细胞——通常构成血管内层的细胞,同时加入携带小“地址标签”的第二种肽以吸引这些内皮细胞。原有与修饰后的肽共同形成了共享的纳米纤维支架。内皮细胞借此支架发芽形成管状延伸,包裹并穿透球体,构建出毛细血管样结构。当研究团队在这些结构周围流动带荧光的类糖分子时,他们观察到这些分子较未含内管的球体更深入地渗透到球体核心,显示营养物质和信号的运输显著改善。
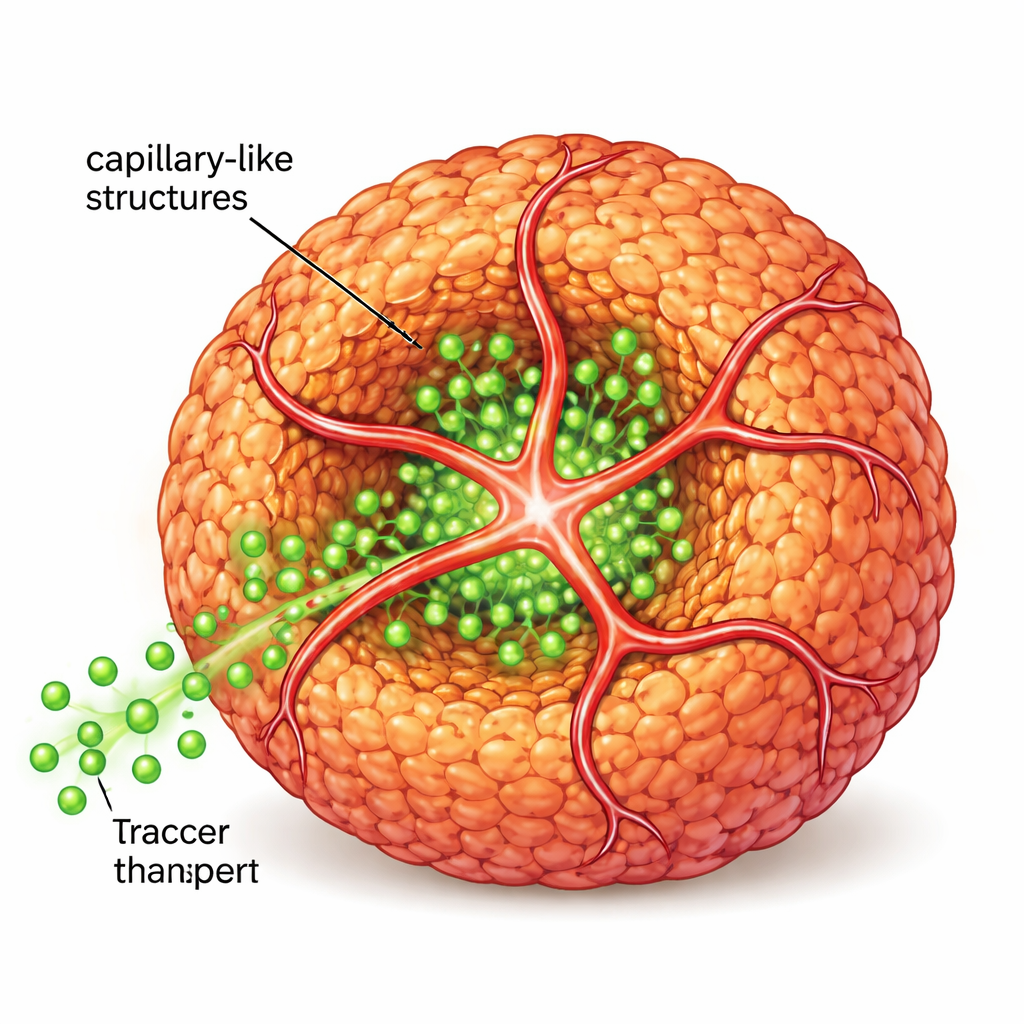
更接近真实肿瘤与功能性胰岛
基因活性分析显示,含有毛细血管样结构的肿瘤球体在分子特征上更接近患者的胶质母细胞瘤样本,而非传统的平面培养或未血管化的球体。在小鼠体内,含有这些原始血管网络的球体生长为更大且血管化程度更高的肿瘤,表明体外模型捕捉到了真实肿瘤行为的关键特征。相同策略也被应用于胰腺β细胞——这些细胞通常位于高度血管化的胰岛中,并对葡萄糖分泌胰岛素。当使用肽系统和内皮细胞为β细胞球体装备毛细血管样结构时,它们表现出更强且更精细调控的胰岛素释放,表明该方法对糖尿病研究与再生医学具有重要价值。
这对未来疗法的重要性
通过让简单的肽在活细胞之间自组装,这项工作提供了一种通用配方,用于构建在触感和功能上更接近体内组织的微型血管化组织。由此得到的球体更能反映患者的肿瘤和功能性胰岛,使其在药物测试、疾病机制研究和新细胞疗法设计中具有重要价值。对于非专业读者,关键结论是:给予体外培养细胞“恰当的触感”和微小的类血管网络,能显著提升它们模拟人体组织的准确性,从而有可能加速基础研究向有效治疗的转化。
引用: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
关键词: 组织工程, 癌症模型, 血管生成, 类器官, 肽自组装