Clear Sky Science · zh
间歇性禁食通过肠道微生物介导的甲硫氨酸–m6A 调控抑制 Tp53 驱动的胶质瘤
为何让肠道休息可能减缓致命性脑瘤
胶质母细胞瘤是最具侵袭性的脑癌之一,现有治疗——手术、放疗和化疗——往往只为患者争取有限的时间。此项研究提出了一个简单但具有深远意义的问题:我们的饮食方式,特别是间歇性禁食,是否能改变肠道细菌和血液化学组成,从而显著放慢某些脑瘤的生长?
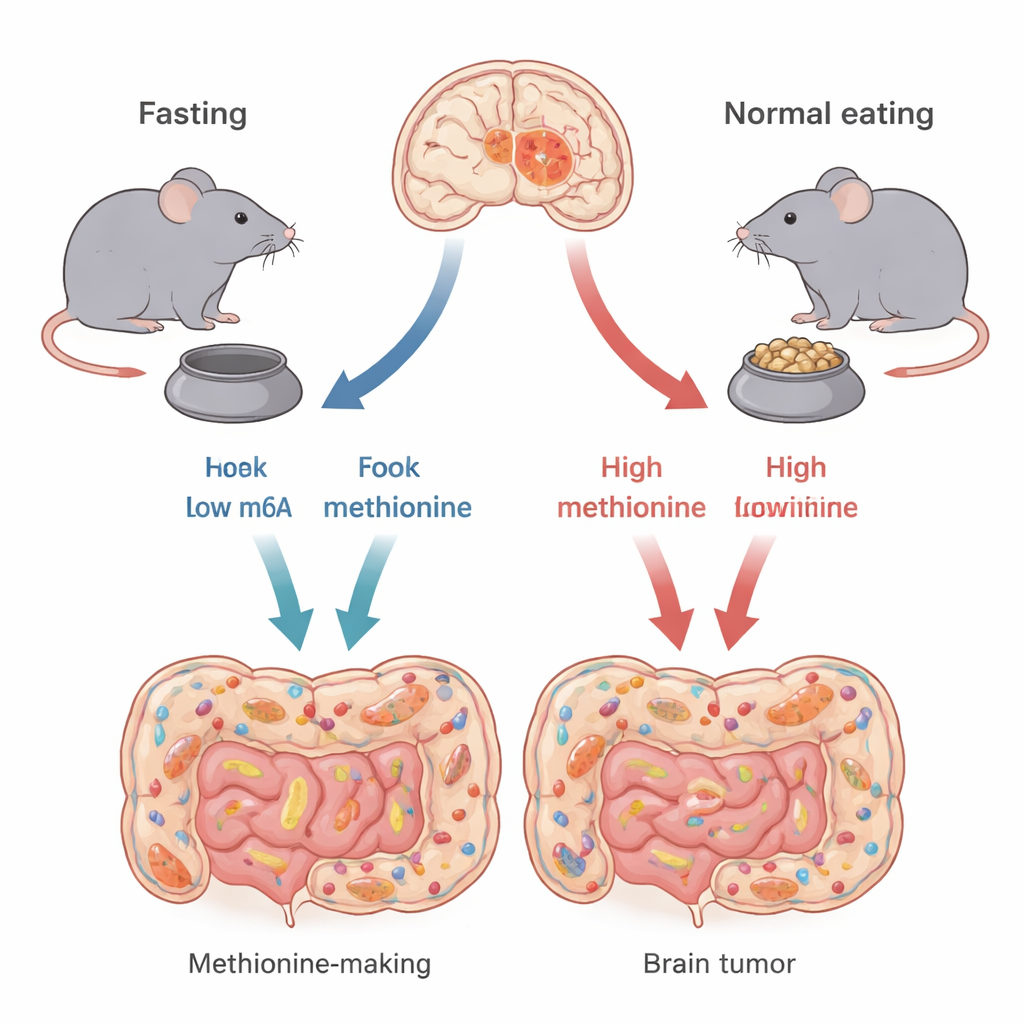
“相同”脑瘤的不同类型
并非所有胶质母细胞瘤都相同。作者关注两类主要的遗传亚型,由 TP53 和 CDKN2A 基因的改变定义。这些基因参与控制细胞的生长与死亡。利用能较好模拟各人类亚型的小鼠模型,研究者表明间歇性禁食——24 小时禁食随后 24 小时进食——并不能同等地帮助所有脑瘤。携带 TP53 型肿瘤的小鼠在禁食时存活更久且肿瘤更小,而携带 CDKN2A 型肿瘤的小鼠几乎没有益处。这提示禁食是否有效可能强烈取决于肿瘤的基因线路。
从进食节律到肠道菌群再到脑内化学变化
研究团队接着探究禁食选择性作用的机制。由于两组摄入的总食物量相同,关键区别在于进食的时间安排。这样的时间改变强烈重塑了肠道微生物群——肠道中庞大的细菌群落。在禁食的 TP53 小鼠中,某些高效合成氨基酸甲硫氨酸的细菌群(例如特定的 Alistipes 和 Prevotella 菌株)丰度下降。因为甲硫氨酸是动物必须从食物或肠道微生物获得的必需氨基酸,这种微生物学上的转变意味着来自肠道进入血液并最终进入大脑的甲硫氨酸减少。
单一营养素如何调整致癌信号
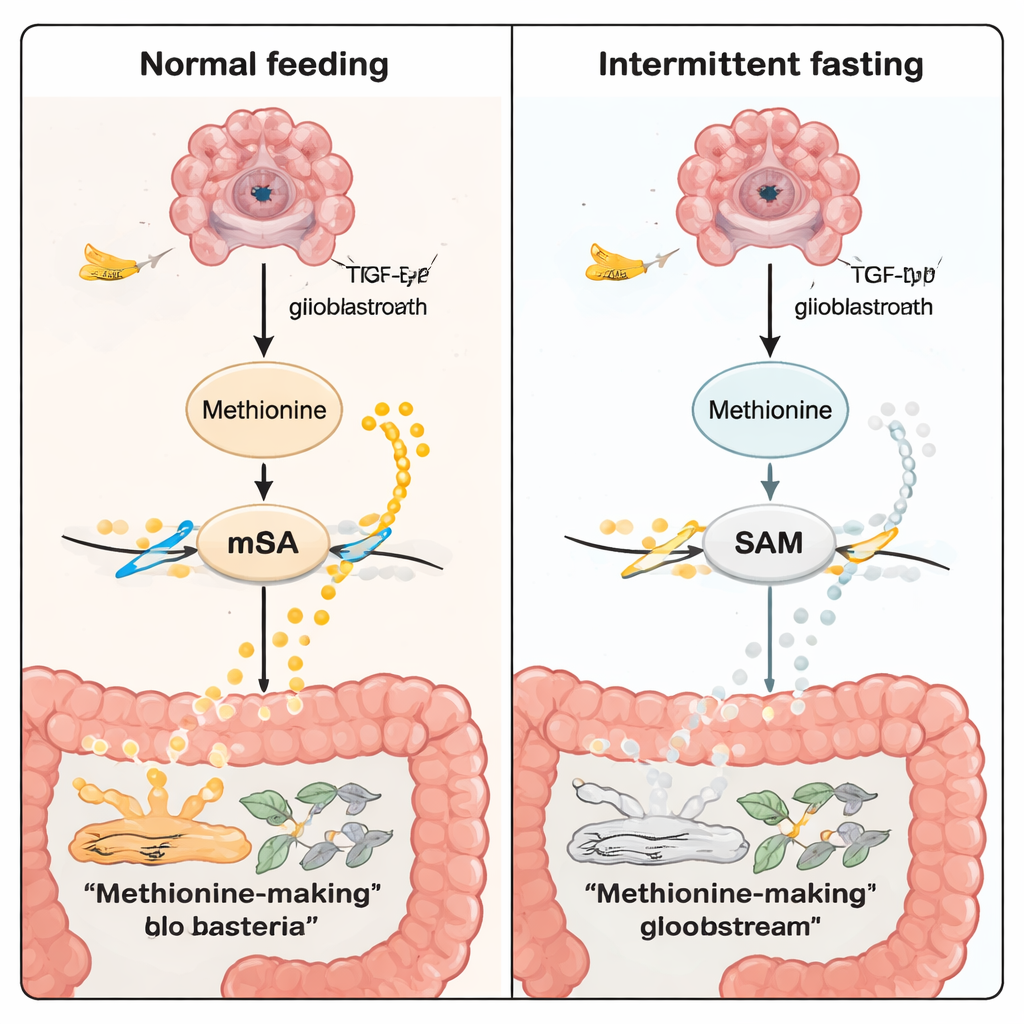
甲硫氨酸不仅是营养物质,它还是合成 S-腺苷甲硫氨酸(SAM)的原料,SAM 是细胞通用的“甲基供体”。SAM 为一种作用于 RNA 的化学标记过程(称为 m6A)提供甲基。这些标记帮助控制某些基因的表达强度。在 TP53 肿瘤模型中,禁食降低了血液和脑肿瘤区域的甲硫氨酸与 SAM 水平。通过多层“组学”技术——常规 RNA 测序、单细胞 RNA 分型以及基因活动与代谢物的空间图谱——研究者发现禁食下关键致癌相关 RNA 的 m6A 标记减少。其中一个重要靶基因是 TGFB2,属于已知能驱动肿瘤生长与侵袭的 TGF‑β 信号通路。禁食时,写入 m6A 标记的酶 METTL3 与 TGFB2 的水平都被下调,TGF‑β 信号减弱。
用靶向干预证明因果关系
为超越相关性,科学家进行了“救援”实验。他们用药物抑制 METTL3,或将禁食小鼠的肠道菌群移植到正常进食的小鼠体内,发现即便不禁食,肿瘤生长也减慢——支持了微生物群与 m6A 机制为关键作用者的观点。相反,当对禁食小鼠补充额外甲硫氨酸或使用可提高 m6A 标记的药物处理时,它们的肿瘤生长更像正常进食小鼠,生存优势消失。重要的是,用广谱抗生素扰乱肠道细菌会抹去许多与禁食相关的变化,突显出肠道群落在这条因果链中处于核心地位。
对人及未来治疗的意义
对普通读者而言,核心信息是:并非所有癌症,甚至并非所有胶质母细胞瘤,对诸如间歇性禁食之类的饮食策略反应相同。在 TP53 型胶质瘤中,禁食似乎通过肠道向大脑“传话”:它重塑肠道细菌,从而降低甲硫氨酸产生,减少 RNA 的化学标记,并抑制肿瘤细胞内强有力的生长信号。尽管这些工作是在小鼠中完成,且需要谨慎地向临床转化,但它指向了一个前景:可以根据肿瘤的基因亚型,将简单的生活方式模式、基于肠道微生物的治疗和针对甲硫氨酸或 m6A 通路的药物相结合进行个体化治疗。
引用: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
关键词: 间歇性禁食, 胶质母细胞瘤, 肠道微生物组, 甲硫氨酸代谢, RNA m6A 修饰