Clear Sky Science · zh
TET1 作为主控因子调节急性髓性白血病中依赖与非依赖 GPX4 的铁死亡监控
这项研究为何对癌症治疗重要
许多新型抗癌药物旨在将恶性细胞推入一种称为铁死亡的自毁状态,这是一种由铁和脂质损伤驱动的细胞死亡形式。然而有些肿瘤顽固地抵抗这种策略。本研究揭示了一种称为 TET1 的 DNA 修饰蛋白如何通过两条不同的生化防御途径帮助白血病细胞规避铁死亡——并表明阻断这些防御能使即便是抗性肿瘤也变得脆弱。
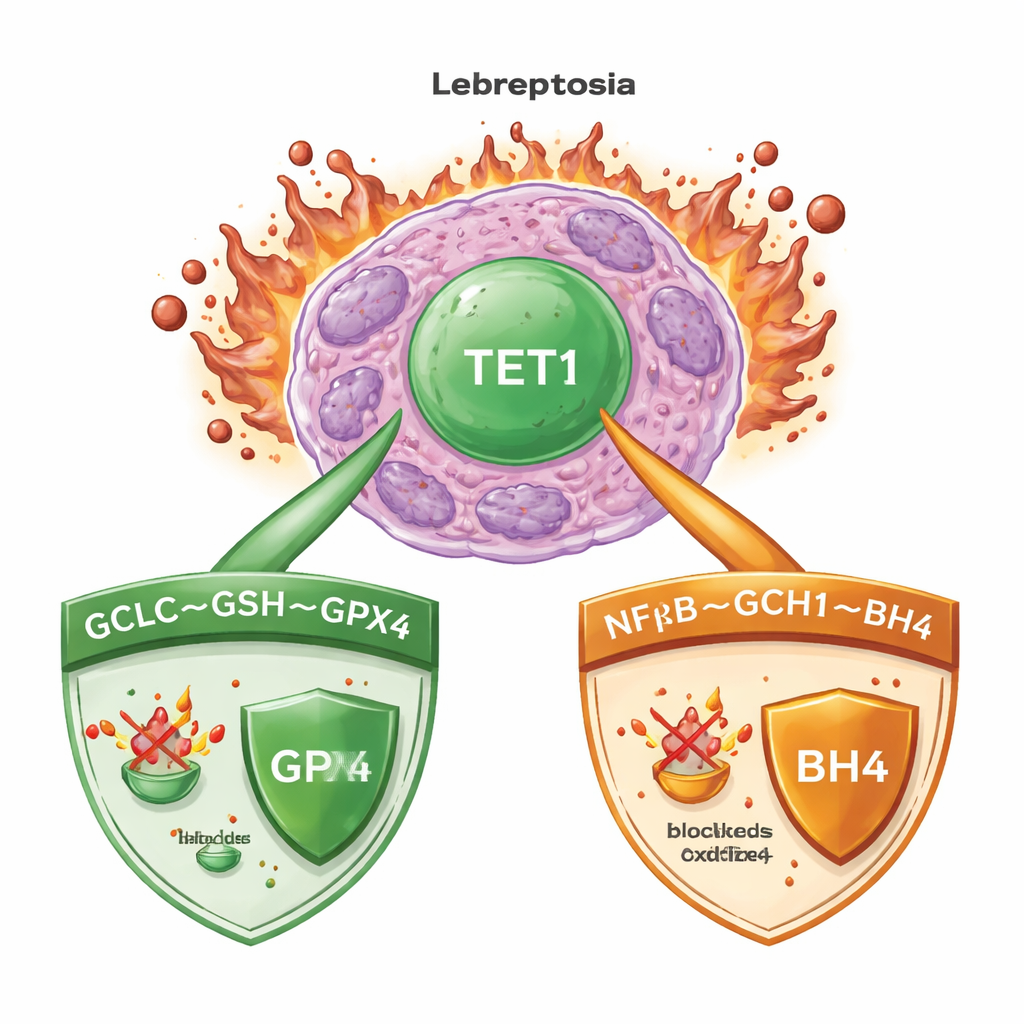
铁与受损脂质的致命混合
铁死亡发生在铁促进细胞膜脂质的失控氧化时,最终导致细胞破裂。在急性髓性白血病(AML)中,和许多癌症一样,细胞部署强大的监控系统来抑制这一过程。一个关键的守护者是酶 GPX4,它利用一种称为谷胱甘肽的小分子中和有害的脂质过氧化物。其他备用系统会生成抗氧化分子,即使在 GPX4 受损时也能捕获危险自由基。了解哪些主控开关协调这些防御,对于设计能可靠触发癌细胞铁死亡同时保护健康组织的疗法至关重要。
TET1 成为中央控制枢纽
研究人员比较了数十个癌细胞样本,包括多种 AML 细胞系和患者来源的细胞,观察到一个清晰的模式:抵抗铁死亡的细胞具有更高水平的 TET1,TET1 是一种能改变 DNA 化学标记并影响基因活性的酶。当他们使用基因学工具降低 TET1 水平或用小分子抑制其活性时,癌细胞对诱导铁死亡药物的敏感性显著增加。这一现象在体外培养和 AML 小鼠模型中均成立。相反,提升 TET1 表达能保护细胞免受铁死亡并限制驱动膜损伤的活性氧(ROS)积累。
增强主要抗氧化屏障
进一步研究中,团队绘制了 TET1 在基因组上的作用位点,发现其直接激活名为 GCLC 的基因。GCLC 编码一台关键酶,启动谷胱甘肽的生成,后者是 GPX4 的燃料。通过在 GCLC 启动子处增加一种特定的 DNA 标记(5-羟甲基胞嘧啶),TET1 提高了谷胱甘肽合成。在正常营养条件下,这会提升细胞的主要抗氧化库;在胱氨酸匮乏时,该酶复合体还会生成不寻常的 γ-谷氨酰肽,有助于清除过量谷氨酸,另一种阻止铁死亡的方式。在培养细胞和小鼠中,丧失 TET1 或药理抑制谷胱甘肽合成都明显降低了谷胱甘肽水平及这些保护性肽,使白血病细胞对铁死亡诱导剂更为敏感。
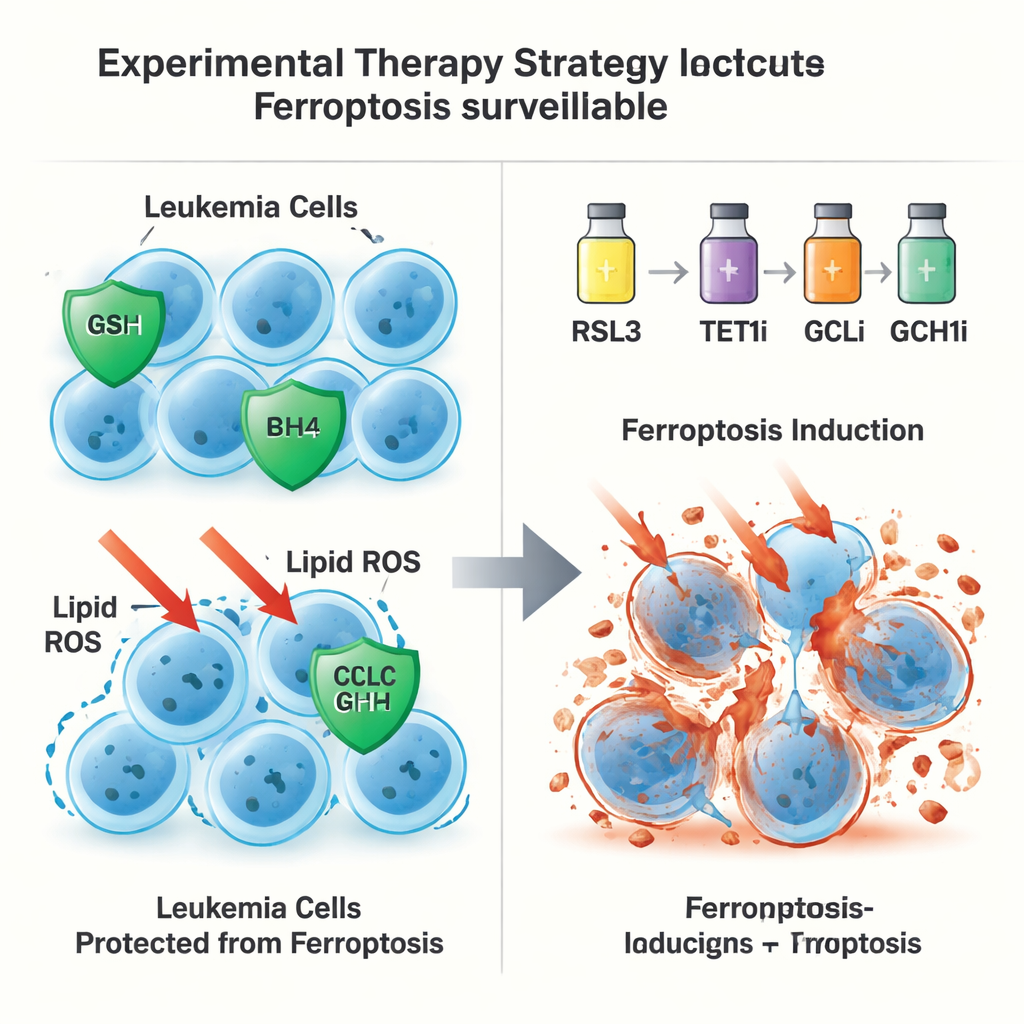
第二条非依赖 GPX4 的逃逸路线
令人惊讶的是,TET1 的保护作用并未止于谷胱甘肽–GPX4 轴。即使在将 GPX4 从白血病细胞中移除的情况下,额外的 TET1 仍能阻止铁死亡,提示存在第二道防线。作者将其追溯到 TET1 对 NFκB 信号通路的激活,特别是一个称为 NFKB2 的成分。这反过来增强了 GCH1 的表达,GCH1 是产生抗氧化分子 BH4 的酶。BH4 可以不依赖 GPX4 就保护膜脂质免受氧化。当 GCH1 被基因沉默或化学阻断时,TET1 对细胞铁死亡的保护能力部分丧失。综上,这些发现定义了一条 TET1–NFKB2–GCH1 路径,构成了一套非依赖 GPX4 的铁死亡监控系统。
将弱点转为治疗机遇
凭借这张双通路图谱,研究人员测试了是否同时促使铁死亡并削弱 TET1 控制的防御可带来治疗优势。在小鼠 AML 模型和患者来源的白血病移植小鼠中,低剂量的铁死亡诱导药与 TET1 抑制剂、GSH 合成抑制剂(通过 GCLC)或 GCH1 抑制剂联合使用,显著降低了白血病负荷、延长了生存期并耗尽了白血病起始细胞群。重要的是,铁死亡诱导剂所用剂量远低于既往研究报道的剂量,降低了对正常造血干细胞毒性的担忧。
这对未来癌症疗法意味着什么
对非专业读者而言,关键信息是白血病细胞通过运行两套重叠的抗氧化“护盾”系统来存活,这两套系统均由 TET1 协调:一套以谷胱甘肽和 GPX4 为中心,另一套基于 GCH1 和 BH4。该研究表明,通过温和诱导铁死亡并同时阻断 TET1 及其下游伙伴,未来或可克服抗性,并选择性地将癌细胞推向死亡边缘,同时不至于压垮健康组织。尽管这些策略尚未进入临床,该研究将 TET1 确立为一个强有力的控制节点和有前景的联合治疗靶点,适用于 AML 及可能其他难治性癌症。
引用: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
关键词: 铁死亡, 急性髓性白血病, TET1, 谷胱甘肽, 癌症表观遗传学