Clear Sky Science · zh
在强酸性条件下为细胞内氧化还原稳态同时进行硫化物氧化和硫酸盐还原
为什么清除有毒气体需要聪明的微生物
许多行业排放硫化氢,这是一种有毒的、闻起来像臭鸡蛋的气体,会腐蚀设备、污染空气并危害工人健康。为去除它,工程师越来越依赖能将硫化物转化为更安全硫形态的微生物。本文揭示了一种意想不到的微生物策略:一种新鉴定的分枝杆菌同时运行通常相互对立的两个化学通路,既能快速解毒硫化物,又能在极强酸性环境下保护自身免受内在损伤。
硫循环中的拉锯战
在自然界中,硫循环由两类相反的反应驱动。一些微生物将硫化物(最还原、最有毒的形式)氧化为元素硫或硫酸盐等较不危险的产物,从中获得能量;另一些则相反,将硫酸盐还原回硫化物,用于合成含硫氨基酸等必需细胞组分。由于这些反应相互抵消,生物学家长期认为单个细胞会避免同时进行两者;这看起来既浪费又像是开窗同时制冷和制热。 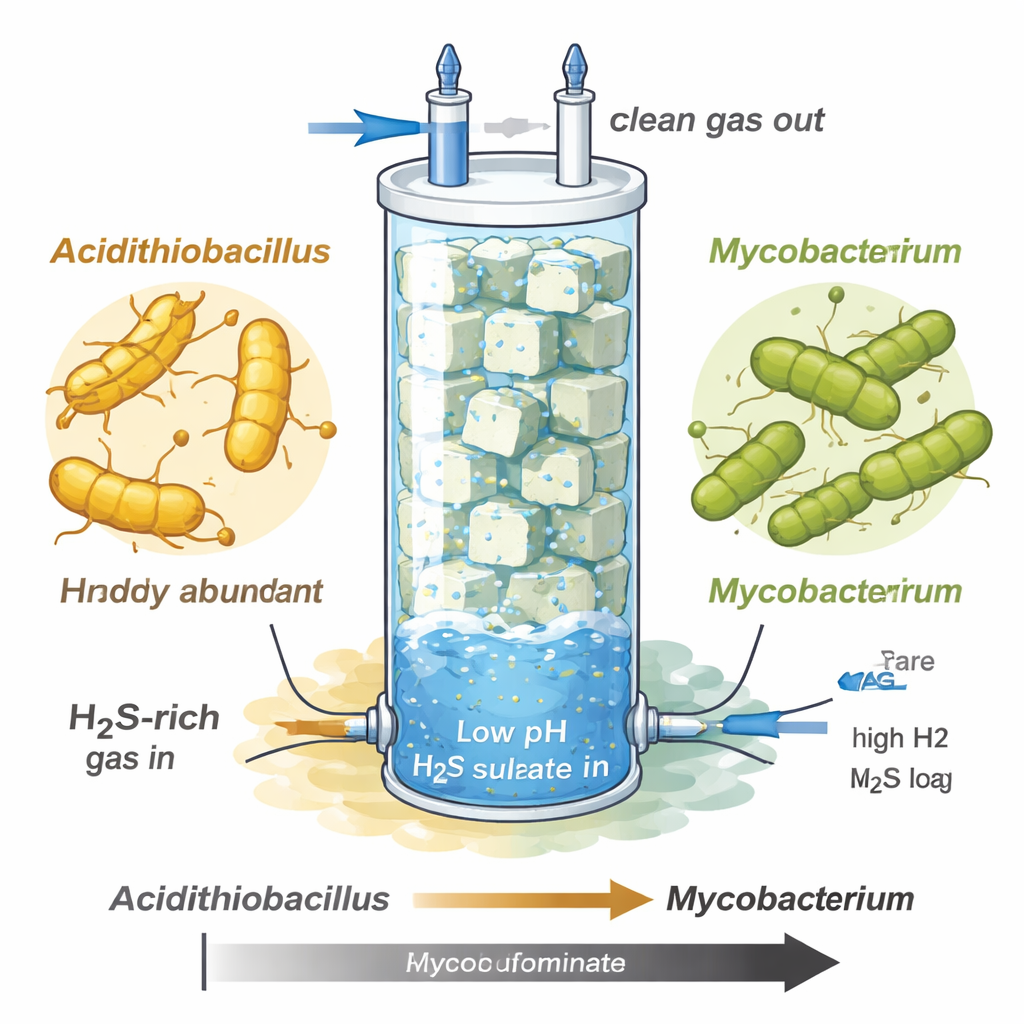
在极端反应器中发现的幸存者
研究者研究了一个生物滴滤塔——一个装有泡沫立方体的高玻璃柱,用于洗涤类似原始沼气或天然气的气流中的硫化氢。当他们提高硫化物负荷并保持系统高度酸性(pH 大约在 1–1.5)时,微生物群落发生了剧烈变化。起初,一种著名的硫化物氧化菌酸化硫杆菌(Acidithiobacillus)繁盛,将大量硫化物转化为硫酸盐,但在极端硫化物压力下随后崩溃。取而代之的是一种先前未表征的分枝杆菌物种,标记为 MAG-M116,几乎占据了整个群落,尽管在起初较温和阶段其生长速度更慢。
打破常规的微生物
基因和蛋白水平分析表明 MAG-M116 具有不同寻常的代谢布局。它携带一种关键酶——硫化物:醌氧化还原酶(sulfide:quinone oxidoreductase),将硫化物仅氧化到固态元素硫,后者以微小颗粒形式积累。与此同时,该微生物拥有一整套同化性硫酸盐还原基因路径,这一路径将硫酸盐摄入细胞并还原,用于合成半胱氨酸和甲硫氨酸等氨基酸。在高硫化物条件下,这两条通路同时被激活。硫化物氧化将电子注入细胞的能量代谢系统,而硫酸盐还原则吸收了部分电子流,将硫循环的两个方向在单个细胞内连接起来。
把“浪费”循环变成安全阀
同时运行这两条通路理论上似乎会徒劳——消耗能量而无净收益。但研究团队表明,对于 MAG-M116 来说,这充当了多余电子的安全阀。大量硫化物氧化会向细胞呼吸链释放电子浪潮,这些电子可能泄漏并产生活性氧(ROS)——攻击 DNA、蛋白质和膜的有害分子。通过主动将硫酸盐还原为氨基酸,细胞将约 10–14% 的电子分流到建设性工作中,从而降低了过度还原、易泄漏状态的累积。比较有无硫酸盐条件的实验显示,活跃的硫酸盐还原将 ROS 产生量最多降低约 60%,并防止了会促成氧化损伤的还原型辅因子累积。 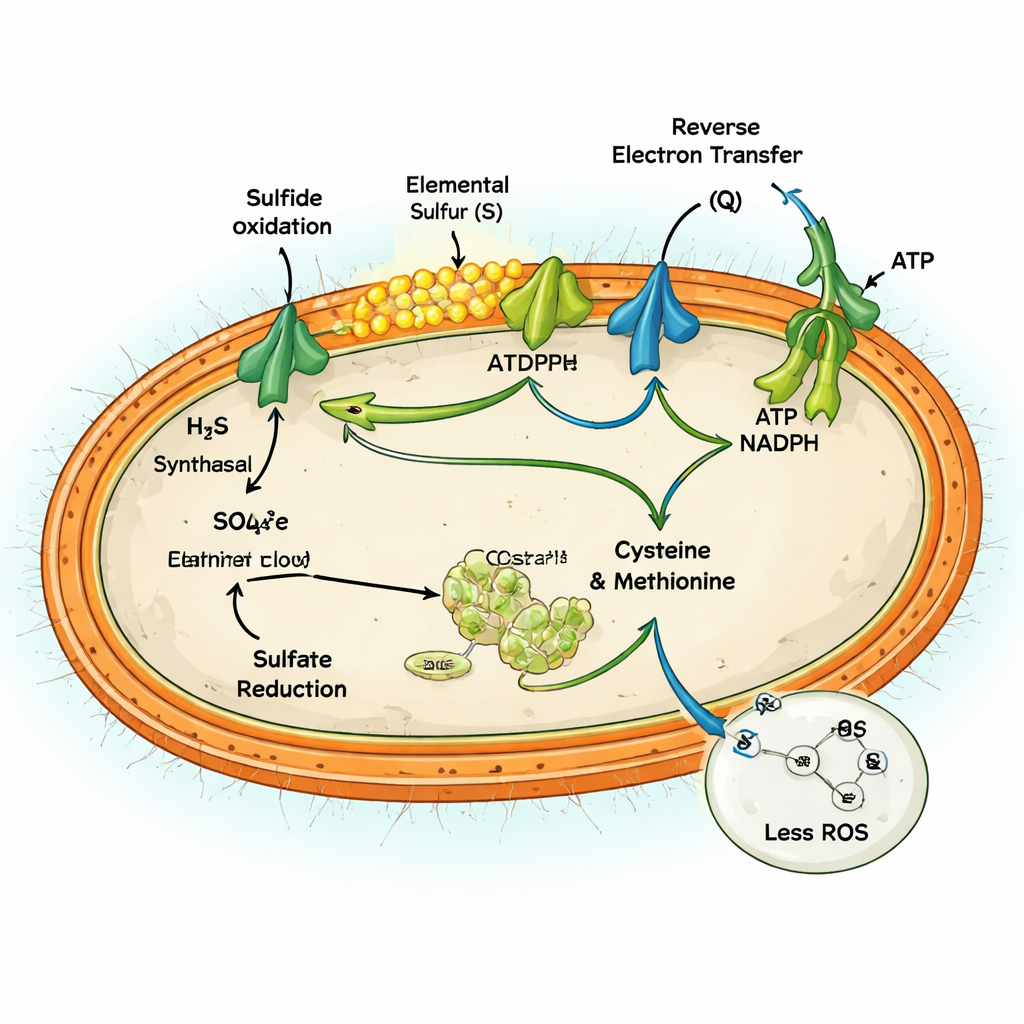
从有毒气体到有用产物
在反应器运行的后期,当 MAG-M116 占主导地位时,几乎所有进入的硫化氢都被转化为固态元素硫,而不是硫酸盐。与此同时,研究者在液相中检测到半胱氨酸和甲硫氨酸水平上升,表明微生物将过剩的含硫氨基酸释放到周围环境中。这种组合——稳定的元素硫加上有价值的有机硫化合物——将曾经的有害污染物转变为可回收、可利用的产物,应用于农业、材料和能源系统。
对健康和技术的意义
对非专业读者来说,核心信息是这种分枝杆菌解决了双重问题:它既能清除高浓度的有毒气体,又能保持自身内部化学平衡。它通过运行通常被分开的“推–拉”硫反应,利用看似浪费的循环作为内建的缓冲器来处理过量电子和有害氧自由基。这一发现不仅为设计耐低 pH 的稳健生物反应器用于硫化物和硫酸盐去除提供了新思路,也暗示相关微生物(包括致病分枝杆菌物种)可能利用类似策略在人体内抵御氧化性攻击。
引用: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
关键词: 硫循环, 硫化氢, 分枝杆菌, 氧化还原稳态, 生物脱硫