Clear Sky Science · zh
一种能够通过ADRB2介导的信号转导来调节糖原分解的人工细胞
教会微小气泡“交流”
想象一个微观的肥皂泡,能够感知外部类似激素的信号,然后“决定”燃烧内部储存的燃料,就像真正的人体细胞一样。该研究正是构建了这种人工细胞,展示了人造细胞模拟体如何接收化学信息并将其转化为受控的能量相关化学反应。这类工作使我们更接近智能药物载体、实验室制造的组织以及能对环境做出反应的简单合成生命形式。
从外向内构建细胞
真实细胞通过其外膜上的受体不断监听周围环境。作者们着手用纯化的成分和简单的脂质小泡(称为巨型囊泡)复制其中一条天然通路。他们聚焦于一种常见的人体受体——β2-肾上腺素受体(ADRB2),在人体中它参与调节心率、肺功能和能量利用。当该受体遇到像异丙肾上腺素(ISO)这样的药物时,通常会触发一系列内部事件,产生一种称为cAMP的信使分子,进而控制细胞如何分解糖原(人体储存的葡萄糖形式)。在人工细胞中重现这整套序列此前尚未实现。
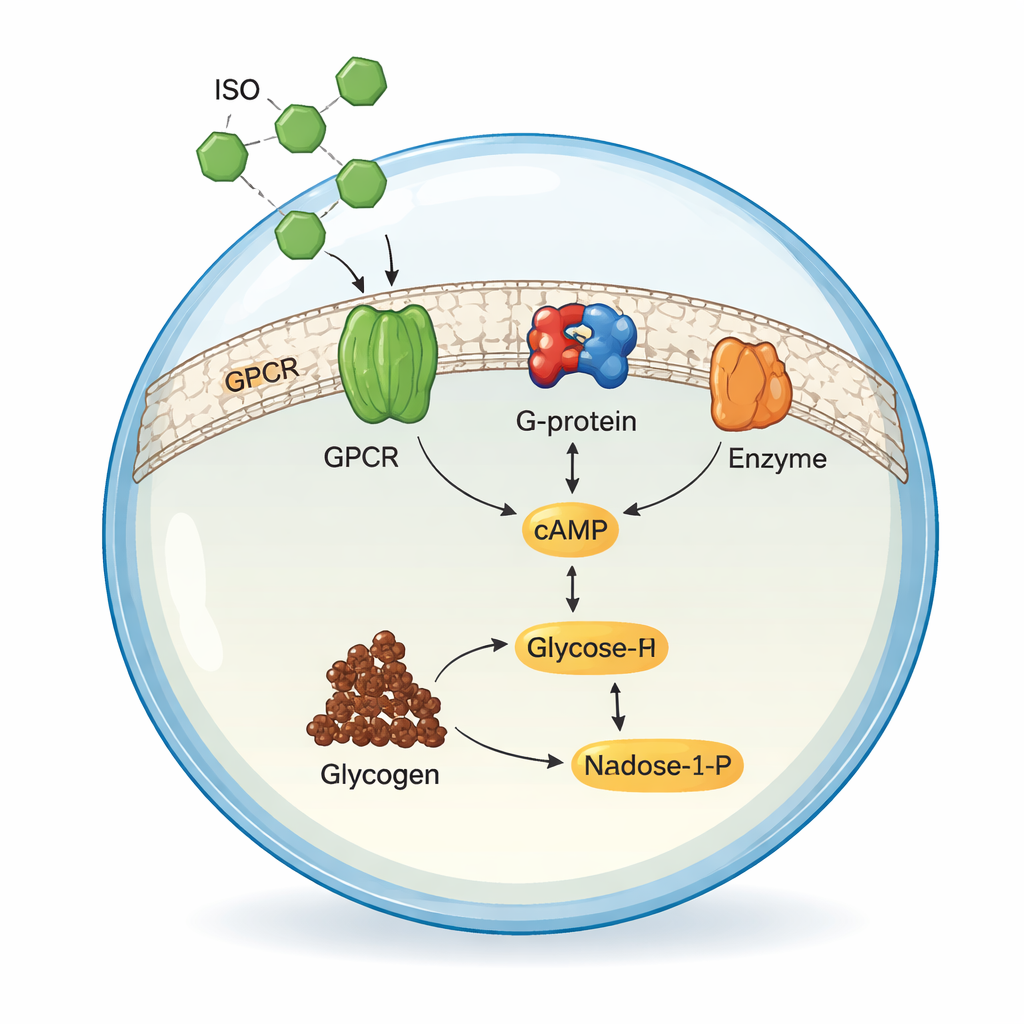
重建首个信号传递环节
团队首先在溶液中(不依赖膜)重建了信号通路的早期阶段。他们在昆虫细胞中表达了三种人源蛋白:ADRB2、其配对的G蛋白亚基(Gsα)和将ATP转化为cAMP的腺苷酸环化酶V(ADCY5)。在精心调节的条件下将这些组分与ISO混合时,肾上腺素受体被激活后促使ADCY5将ATP转化为cAMP。通过高效液相色谱测量cAMP,研究者优化了pH、温度和镁离子水平,发现他们重构的体系效率与许多先前体系相当或更好,证实了核心信号化学已经复现。
在人工膜中安装真实受体
接着,作者将三种蛋白嵌入巨型单层囊泡的膜中——这些细胞大小的脂质气泡作为人工细胞的底盘。他们用荧光标记ADRB2和ADCY5以验证蛋白位于膜中、能够自由移动且数量众多,约每个囊泡有1.8百万个受体。酶学处理显示超过94%的受体朝向正确,结合位点暴露在外部。荧光GTP探针证实膜上ISO结合确实激活了囊泡内的G蛋白。这意味着人工细胞原则上能够像天然细胞一样将外部ISO信号穿膜传递。
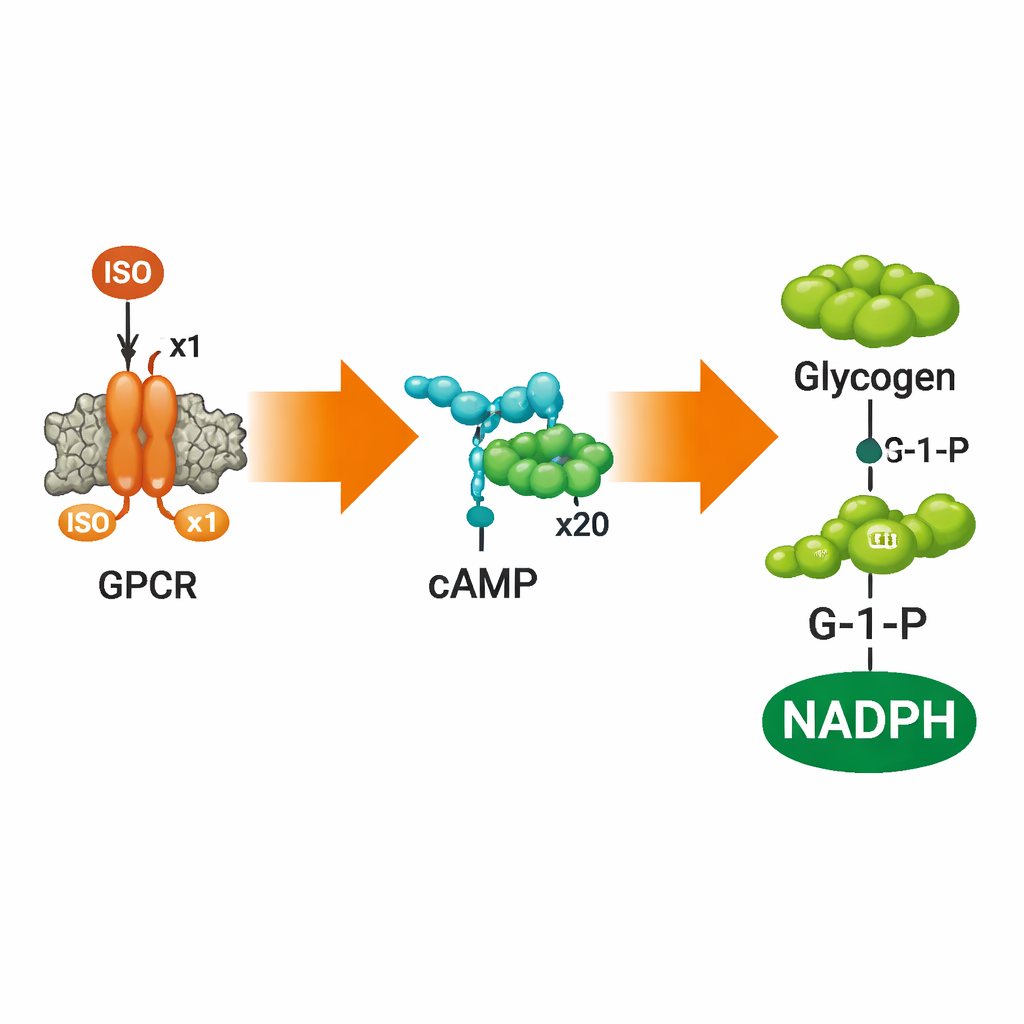
将信号转化为燃料分解
为了检验这些合成细胞是否能将信号用于有用的事情,团队在囊泡内加入了cAMP传感器以及完整的糖原分解通路。使用基于FRET的cAMP探针,他们表明在囊泡外加入ISO会在囊泡内引起cAMP水平以剂量依赖的方式上升,然后随着受体饱和而趋于平稳,这与天然G蛋白偶联受体的典型行为一致。抑制或静默ADRB2的药物——阿普洛洛尔(alprenolol)和卡哌洛尔(carazolol)——准确地关闭了该反应。当作者还将五种通常将糖原转化为葡萄糖-1-磷酸(G-1-P)并进一步转化为NADPH的酶封装入囊泡时,ISO刺激导致人工细胞内部可测量的G-1-P和NADPH产生,研究者通过质谱、色谱和荧光检测进行了跟踪。
把低语放大成呼喊
一个关键发现是内部响应被强烈放大的程度。囊泡外的适量ISO产生的大约是其分子数22倍的cAMP分子,而且这种放大在通路下游进一步增长。当信号推动糖原分解并伴随NADPH生成、转化为6-磷酸葡萄糖内酯时,总体放大超过百倍。这种逐级放大的特征是天然激素信号传递的标志,表明人工体系不仅检测ISO——它还处理并将信息放大为强大的代谢输出。
这对未来合成生命意味着什么
对非专业读者来说,技术细节归结为一个简单想法:研究者教会了一个最小的人造细胞像活细胞一样倾听并响应。外部的药物分子停靠在一个逼真的人类受体上,信号穿过合成膜传递到内部,内部的酶网络通过动员储存的化学能做出反应。在精简的人工体系中展示从受体激活到受控代谢的完整链条,是迈向自主合成细胞的重要一步——这些细胞能够感知、决策并采取有用行动,例如在检测到正确化学线索时调整自身的能量供应或仅在需要时释放治疗物质。
引用: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
关键词: 人工细胞, 信号转导, GPCR, 糖原分解, 合成生物学