Clear Sky Science · zh
从古代肠道微生物组中鉴定抗菌肽
从古老线索中挖掘对抗现代病菌的办法
随着全球抗生素耐药性的上升,医生在治疗危险感染时可用的手段日益减少。这项研究采取了一种不同寻常的方法:研究者并不局限于高端化学实验室,而是转向人类粪便的化石化遗留物——古代肠道“时间胶囊”——以发现可能仍然对当今细菌有效的天然抗菌分子。
古代微生物:隐藏的药橱
在现代医学出现之前,人类肠道早已是有益微生物与入侵病原体争夺空间和营养的战场。许多有益肠道细菌能产生抗菌肽——短小的蛋白片段,能够在细菌细胞上形成孔洞或以其他方式使其失活。现代研究大多在当今的微生物组中寻找这些杀菌肽。但我们当前的肠道群落已与抗生素使用和现代生活方式共同进化,给有害细菌提供了多次发展耐药性的机会。相比之下,保存于干化粪便(称为粪石)中的古代肠道群落形成于没有处方抗生素的时代,这使它们成为“被遗忘”防御机制的有前景来源,现代病原体或许尚未学会躲避这些防御。
用于读取化石化DNA的轻量级AI工具
为了探索这个古代药房,研究团队构建了一种名为AMPLiT(AMP Lightweight Identification Tool)的新计算工具。AMPLiT无需大型超级计算机,就能在普通笔记本上高效运行,同时保持较高的准确性。它扫描来自微生物组样本的大规模DNA数据集,标记出可能编码抗菌肽的短序列。团队对AMPLiT的设计进行了微调,使其能在数小时内处理来自受损、历经数百年乃至千年DNA的数百万片段,与早期方法相比将训练时间缩短约80%,同时在识别可能的杀菌候选分子方面仍接近最先进的性能。
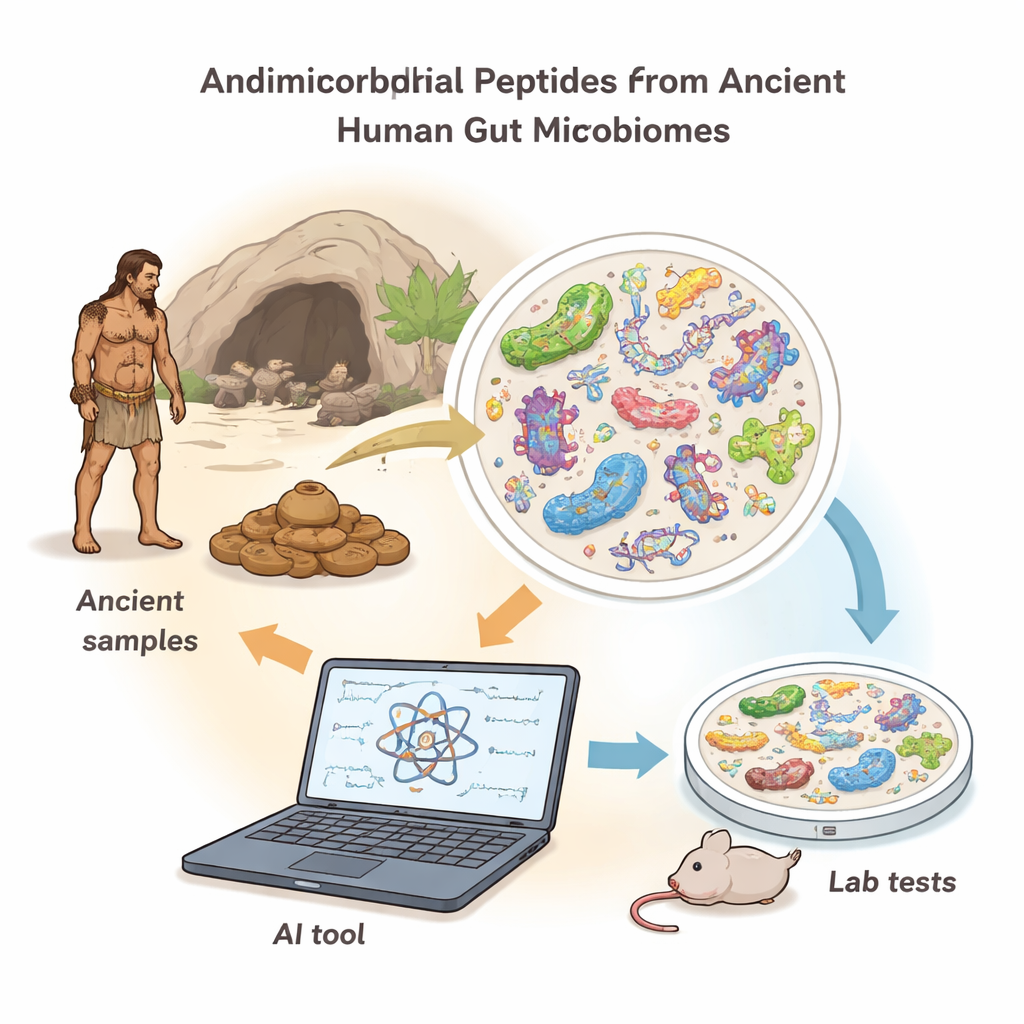
从古代肠道居民中复活杀菌分子
研究者使用AMPLiT分析了来自7名生活在北美、年代为公元1000–2000年间的古代人的肠道DNA。排除了环境污染并聚焦于简短、实际可行的肽长后,工具预测了数十万条可能的抗菌序列。一系列更严格的筛选——在多名个体中的存在、化学性质及低预测毒性——将候选数量缩减到41条高置信度序列,其中40条可在实验室中化学合成。对“革兰氏阳性”和“革兰氏阴性”细菌(包括许多常见病原体的两大类)进行测试时,40条肽中有36条在相对较低剂量下抑制或阻止了细菌生长,这在此类发现工作中是一个异常高的成功率。
出人意料的明星:正在消失的肠道盟友
大约三分之二的高活性肽来自单一肠道细菌:Segatella copri,它与曾被归类为Prevotella copri的一类微生物关系密切。该物种在古代肠道中十分丰富,并且在饮食更传统、工业化程度较低的人群中仍然常见,但在许多城市化、西式生活的人群中已变得稀少。通过追踪这些肽基因在Segatella基因组中的位置,团队发现大多数实际上是更大、日常“家务”基因的片段,微生物似乎将这些片段重新利用为武器——一种高效的进化策略。许多这些古代肽与现代数据库中的肽差异较大,表明它们代表真正新的化学设计,而不仅仅是已知抗生素的微小变体。
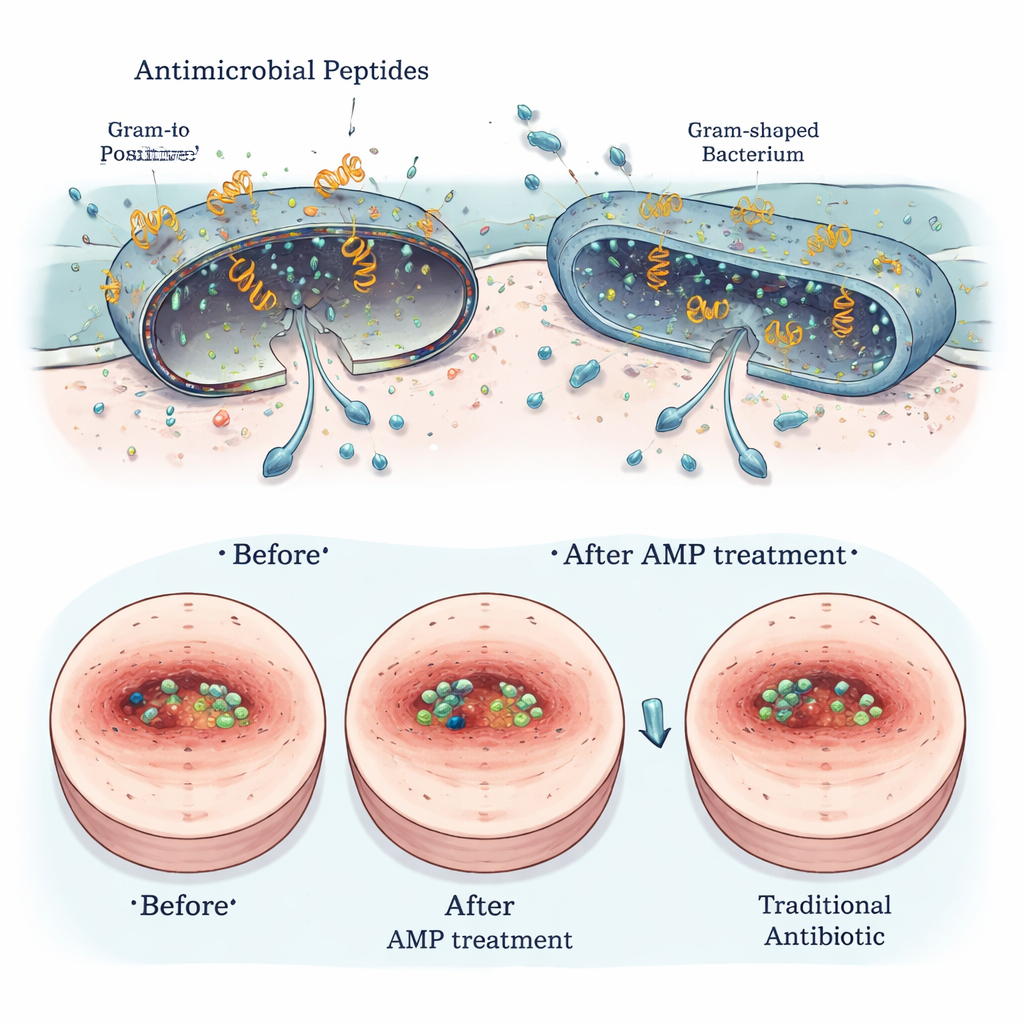
对宿主安全、对病菌致命——并在伤口模型中展现出希望
几种最有前景的Segatella肽进行了安全性和实际效用测试。在体外培养皿中,它们对红细胞的破坏很小或没有,对类肠道的人类细胞也仅有轻微影响(如果有的话)。高分辨率显微镜显示这些肽物理性地破坏了有害细菌的外膜,而对哺乳动物细胞则相对不伤害。在啮齿类动物的感染伤口模型中,外用筛选出的肽能减少细菌负荷、加速伤口愈合并减轻炎症迹象,其效能与已有抗生素(如万古霉素和多粘菌素B)相当,尤其是在对抗如金黄色葡萄球菌等革兰氏阳性细菌方面表现突出。
这对未来药物意味着什么
对非专业读者而言,结论很直接:我们祖先的肠道微生物可能蕴含尚对当今难治性感染有效的新型抗生素蓝图。这项研究表明,借助像AMPLiT这样聪明且高效的AI工具,科学家能够从古代DNA中开采出既强效又对人类细胞相对温和的抗菌肽。尽管要将任一这些分子开发成药物仍有许多步骤要走,但这项工作提示,复兴像Segatella copri这样的“失落”微生物伙伴——或至少借用它们的分子武器——可能有助于补充我们日益减少的对抗耐药细菌的武库。
引用: Chen, S., Yuan, Y., Wang, Y. et al. Identification of antimicrobial peptides from ancient gut microbiomes. Nat Commun 17, 1788 (2026). https://doi.org/10.1038/s41467-026-68495-0
关键词: 抗菌肽, 古代微生物组, Segatella copri, 抗生素耐药性, 宏基因组挖掘