Clear Sky Science · zh
针对UFL1–AKT级联抑制三阴性乳腺癌进展
这项研究为何重要
三阴性乳腺癌(TNBC)是乳腺癌中致死率较高的一类,因为它缺乏许多现代药物所针对的激素受体和生长因子受体。患者通常只能接受传统化疗,但随着肿瘤产生耐药,这类疗法常常失效。本研究揭示了一个此前未被注意的分子“发动机”,它助长TNBC细胞生长并抵抗化疗,并提出了一种直接干扰该发动机的新型药物策略。
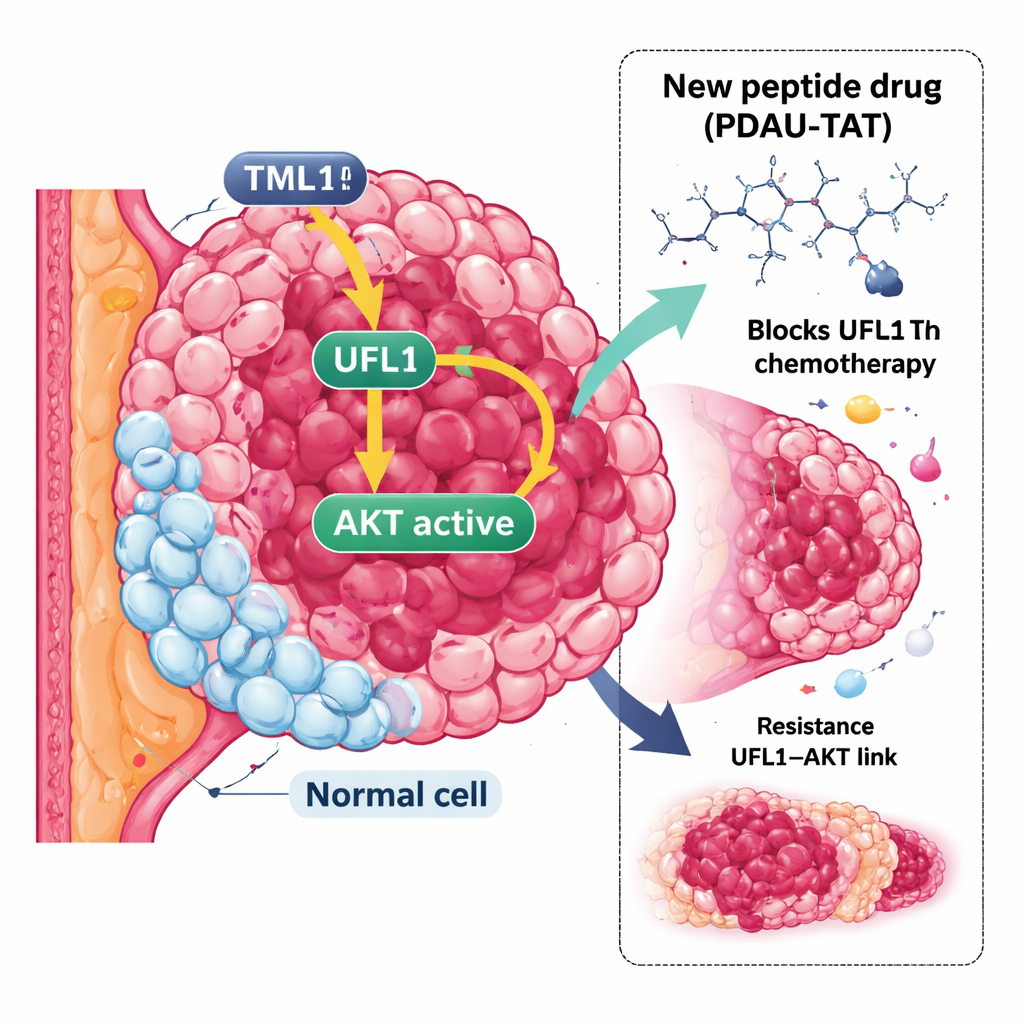
一种顽固的乳腺癌类型
TNBC以缺失三种常见标志物为特征:雌激素受体、孕激素受体和HER2生长受体。没有这些标志物,许多行之有效的靶向疗法就无法适用。相应地临床上更多使用顺铂和阿霉素等传统药物,但TNBC肿瘤常常对这些治疗产生抗性或迅速适应,并且更易发生转移。这就迫切需要新的策略,超越常见靶点,寻找肿瘤控制系统中的其他脆弱点。
一个鲜为人知但影响重大的蛋白
研究者将注意力集中在UFL1上,这是一种将小型标记物UFM1连接到其他蛋白上的蛋白,称为UFM化修饰。这个标记系统近年才被发现,其在癌症中的作用尚不明确,甚至存在矛盾结论。通过分析患者数据和肿瘤样本,团队发现与正常乳腺组织相比,TNBC中UFL1明显升高。在TNBC细胞系和小鼠肿瘤模型中减少UFL1水平后,癌细胞增殖显著减慢,并对化疗更为敏感,表明在此情境下UFL1具有促进肿瘤的作用。
将UFL1与一个主控生长开关连接起来
进一步研究显示,UFL1可直接与AKT结合,AKT是驱动细胞生长、生存与代谢的核心信号蛋白,且在多种癌症中常呈过度活化状态。在TNBC中,即便缺乏常见的上游突变,AKT也常处于高活性。团队发现UFL1在AKT的三个特定位点上进行化学标记,这使得AKT更易被其激活伙伴打开,同时也保护AKT免受通常使其关闭的酶的作用。缺失UFL1的细胞或表达无法被标记的工程化AKT的细胞,AKT活性明显降低,增殖减慢,并在细胞培养和动物模型中对化疗更易感。
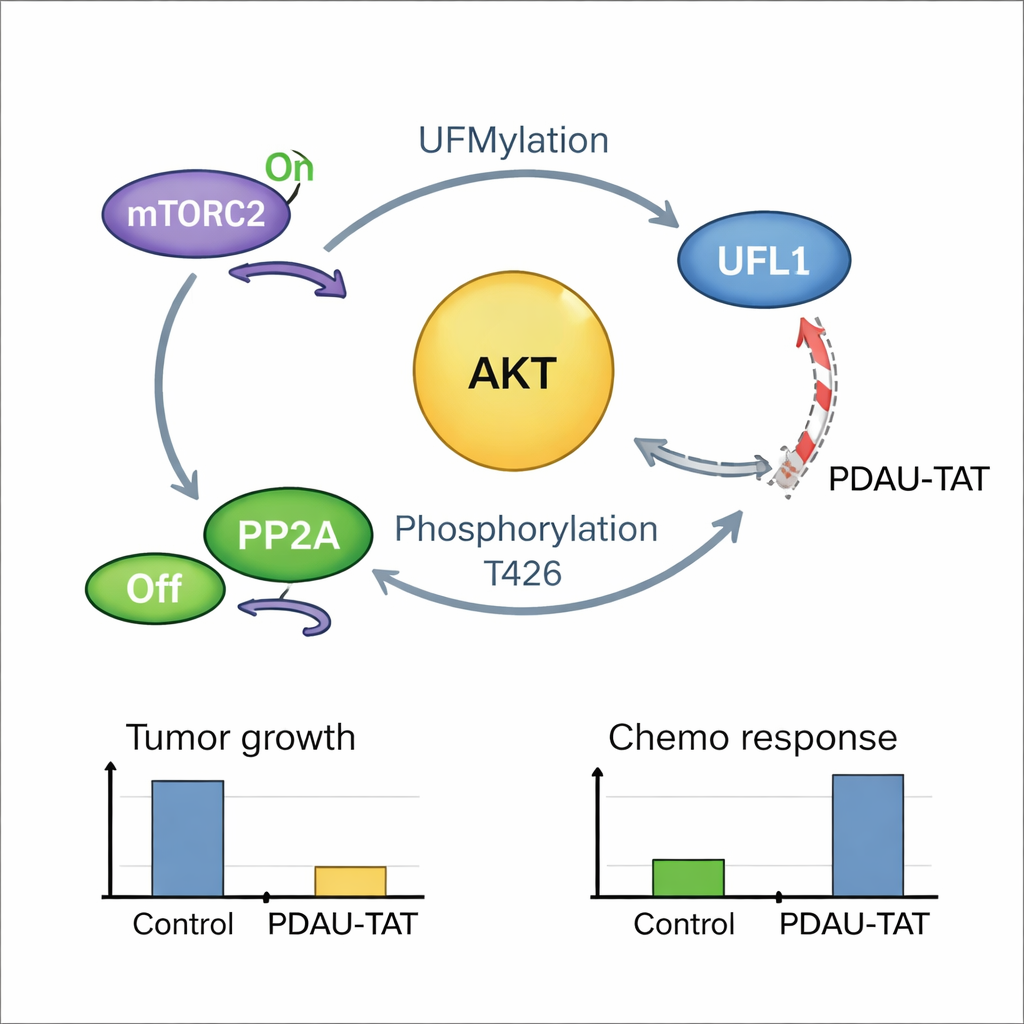
一个自我强化的癌症回路及其破解方式
事实更为紧密:一旦AKT被激活,它会反馈并在UFL1的一个关键位点上进行修饰,增强UFL1对AKT及其他底物的标记活性。由此形成一个正反馈回路——UFL1激活AKT,活化的AKT又反过来强化UFL1。患者肿瘤样本显示,高水平被修饰的UFL1与高水平的活化AKT强相关,支持该回路在人类疾病中的存在。为利用这一脆弱点,团队设计了一种短小、可穿透细胞膜的肽PDAU-TAT,它模拟UFL1的一小段区域并插入UFL1与AKT之间,破坏它们的相互作用,降低AKT的激活,抑制肿瘤生长,使TNBC细胞和来源于患者的肿瘤对化疗更敏感,并且在小鼠中未见对主要器官的明显损伤。
这对患者可能意味着什么
简而言之,研究者发现了TNBC细胞内的一张隐秘线路图:UFL1与AKT缠绕成一个自我放大的回路,使生长信号长期处于“开”状态并助长肿瘤耐药。通过构建一个能插入该回路并切断UFL1与AKT连接的小肽,他们展示了一种可行的新方法,有望在不严重损伤正常细胞的情况下削弱TNBC肿瘤,因正常细胞通常具有较低的UFL1水平。尽管该工作仍处于临床前阶段,但它指向了一类新的靶向疗法——不是针对常见受体,而是针对驱动某些侵袭性乳腺癌的蛋白—蛋白相互作用。
引用: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
关键词: 三阴性乳腺癌, AKT信号通路, UFM化修饰, UFL1, 肽类抗癌疗法