Clear Sky Science · zh
UFL1–AKT 正反馈回路通过增强脂质合成促进乳腺癌进展
为什么癌细胞如此重视脂肪
乳腺癌细胞和所有快速生长的细胞一样,需要持续供应的构件来合成新的膜和信号分子。脂肪或脂质是这些构件的重要组成部分。本研究揭示了一种鲜为人知的蛋白质系统如何将癌细胞推入“脂肪生成超速”状态,帮助肿瘤生长并逃避免疫和治疗。理解这一隐藏的燃料来源,可能为阻止或“饿死”乳腺癌开辟新途径。
一种隐蔽的蛋白质标记却有重大后果
我们的细胞通过微小的化学标记不断调整蛋白质的功能。其中一种称为 UFM1 的标记由酶 UFL1 附加。UFM1 标记(UFMylation)已与 DNA 修复和应激反应相关,但其在癌症中的作用尚不清楚。作者证明,在人类乳腺肿瘤中,UFL1 的活性明显高于正常乳腺组织,且在主要亚型中普遍存在。肿瘤中 UFL1 水平较高的患者通常生存率较差。当研究者在乳腺癌细胞或小鼠肿瘤中降低 UFL1 时,癌细胞生长减慢,细胞分裂减少,细胞死亡增加,提示 UFL1 表现出促癌特性。
如何将一个信号枢纽转换为产脂模式
为弄清 UFL1 如何助力肿瘤,团队寻找其分子伙伴,发现了关键的信号调控蛋白 AKT1。AKT1 是一个中央开关,指示细胞生长并合成新脂质。研究显示 UFL1 与 AKT1 发生物理结合,并在若干特定位点将 UFM1 附着到 AKT1 上。这种标记改变了 AKT1 的构象,放松了通常使其保持抑制的“内在刹车”。它还促使 AKT1 转移到细胞内的膜区室——内质网,在那里其他酶通过磷酸化可以完全激活它。如果这些位点没有 UFM1 标记,AKT1 就更难被激活。
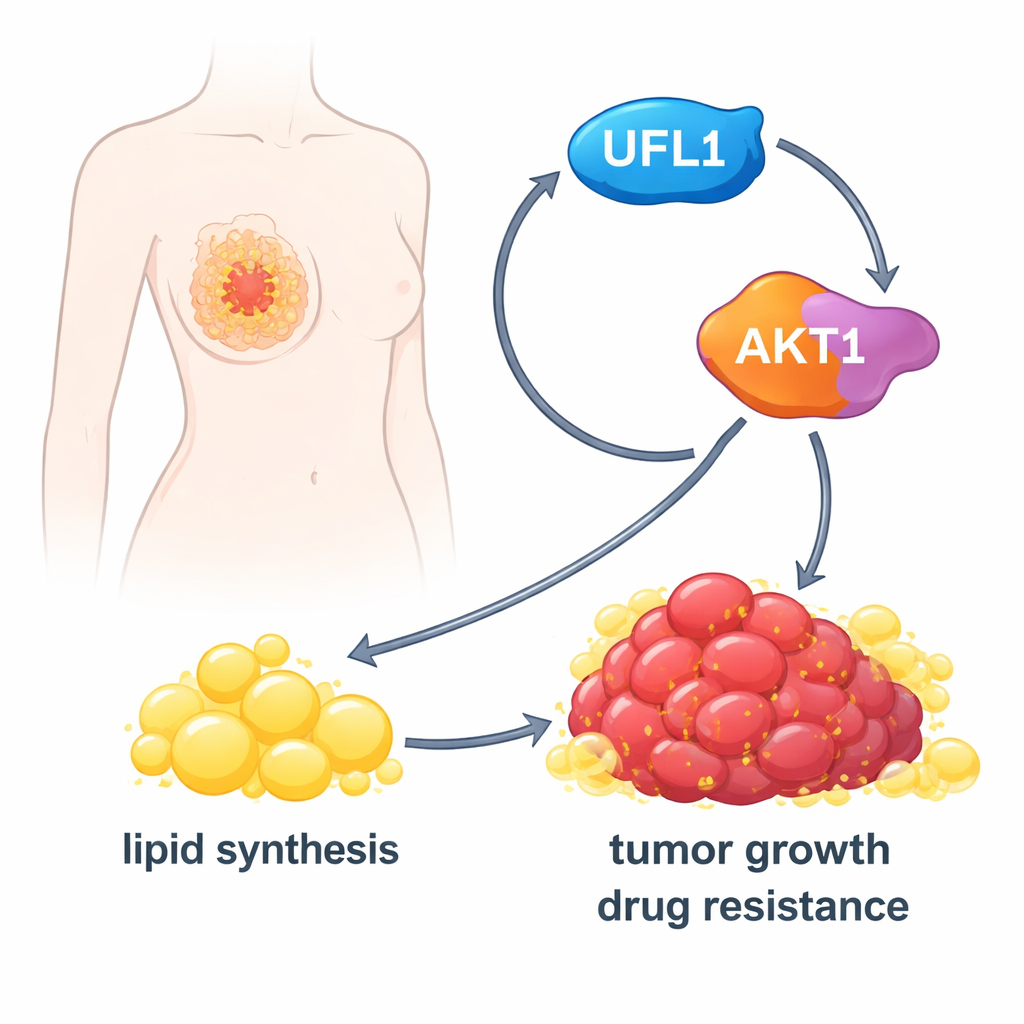
开启癌细胞的脂肪工厂
一旦被激活,AKT1 推动细胞提高脂质合成。它增强关键代谢酶 ACLY 的活性,并提高像 SREBP1 这样的主调控因子的水平,后者可开启许多产脂基因。在体外培养的乳腺癌细胞中,UFL1 使细胞积累更多脂滴、游离脂肪酸和胆固醇。去除 UFL1 明显减少了这些脂质储备,无论是在培养皿中还是在小鼠生长的肿瘤中。向细胞外补充额外脂肪酸可以在很大程度上挽救缺失 UFL1 的癌细胞生长,说明 UFL1 的主要作用是确保足够的脂质以维持肿瘤扩张。
驱动肿瘤生长的自我放大回路
令人惊讶的是,UFL1 与 AKT1 之间的关系是双向的。研究者发现,一旦 AKT1 被激活,它反过来在 UFL1 的特定位点添加磷酸基。这种修饰进一步增强了 UFL1 给 AKT1 添加 UFM1 标记的能力,从而形成正反馈回路:UFL1 激活 AKT1,而 AKT1 反过来激活 UFL1。突变 AKT1 上的 UFM1 标记位点或 UFL1 上的磷酸化位点会破坏该回路。在小鼠中,携带这些突变版本的肿瘤生长不良,脂质含量减少并显示更多细胞死亡。在三阴性乳腺癌患者样本中,活化的 UFL1 和活化的 AKT1 往往同时升高,强调该回路在真实肿瘤中确实存在。
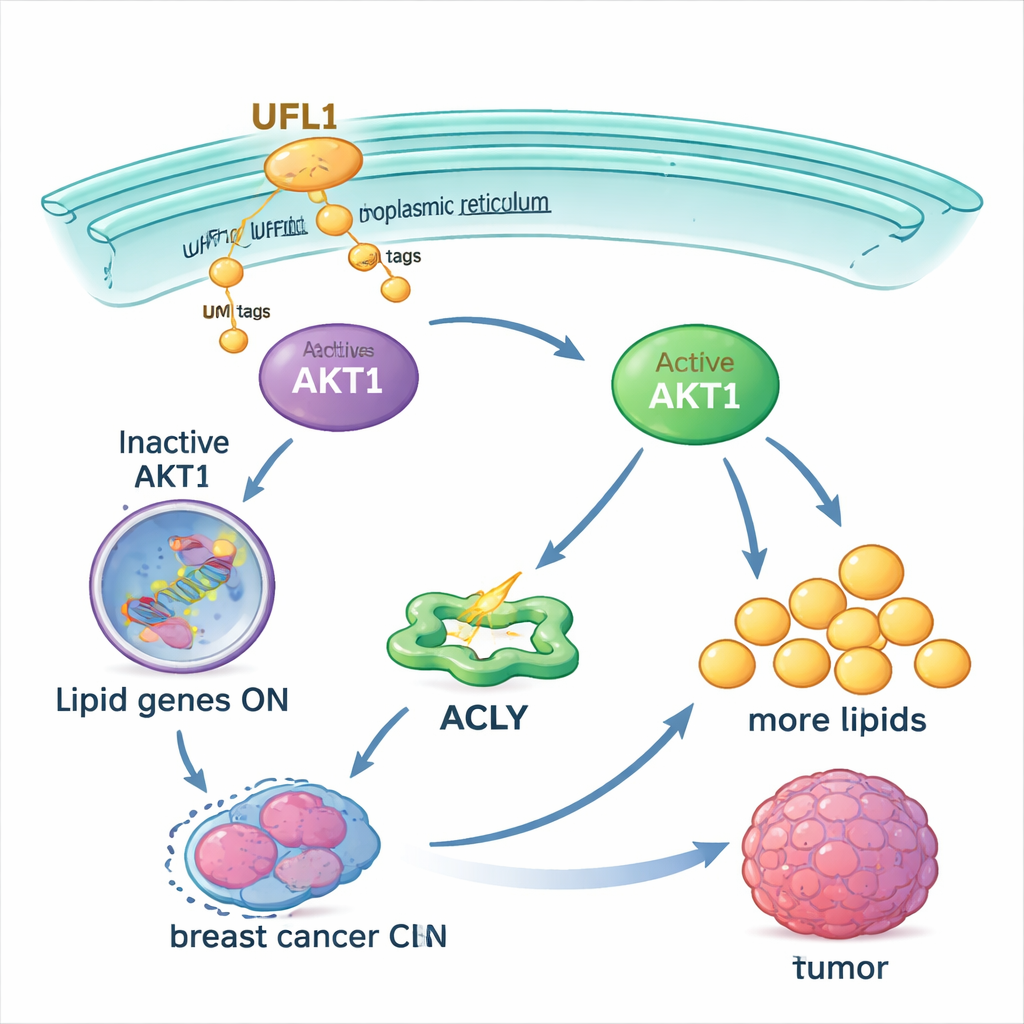
削弱回路以提升治疗效果
由于许多药物试验已经针对 AKT,作者测试了阻断 UFMylation 是否能增强这些疗法的效果。在乳腺癌细胞中,一种小分子 UFMylation 抑制剂和一种 AKT 抑制剂各自都能降低 AKT1 活性和脂质积累,但两者联合使用的效果远胜于单用。该组合在小鼠肿瘤中也减缓了肿瘤生长并降低了脂质含量,同时动物体重无明显下降。阻断 UFMylation 还使癌细胞对顺铂和依托泊苷等标准化疗药物更为敏感,而这些药物在 AKT 高活性的情况下常常疗效受限。
这对患者意味着什么
对非专业读者而言,这项研究表明某些乳腺癌通过自我增强的回路来同时供养其生长和脂质供应。UFL1 与 AKT1 协同工作,像两个同时踩下的踏板:一个负责标记,一个负责信号,两者共同驱动脂质生成和肿瘤扩张。通过找到干扰该回路的药物——无论是阻断 UFMylation、抑制 AKT1,还是阻断它们的相互作用——未来的治疗或许能够放慢肿瘤生长并提升现有疗法的疗效,尤其是在侵袭性乳腺癌类型中。
引用: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
关键词: 乳腺癌, 脂质代谢, AKT 信号, UFMylation, 靶向治疗