Clear Sky Science · zh
原位自组装细胞库水凝胶用于调控多阶段放射免疫疗法
将放射线变成更聪明的抗癌武器
放射治疗是最广泛使用的癌症疗法之一,但肿瘤常通过躲避免疫监视和在低氧(缺氧)环境中生长来抵抗放射线的杀伤。本研究描述了一种可注射的“智能”水凝胶,它可在肿瘤内部直接形成,充当微型药物工厂和氧气发生器。通过同时向肿瘤提供放射线能量和按时序释放的免疫刺激信号,该系统旨在把难治性肿瘤转变为机体自身防御能够识别并消灭的目标。
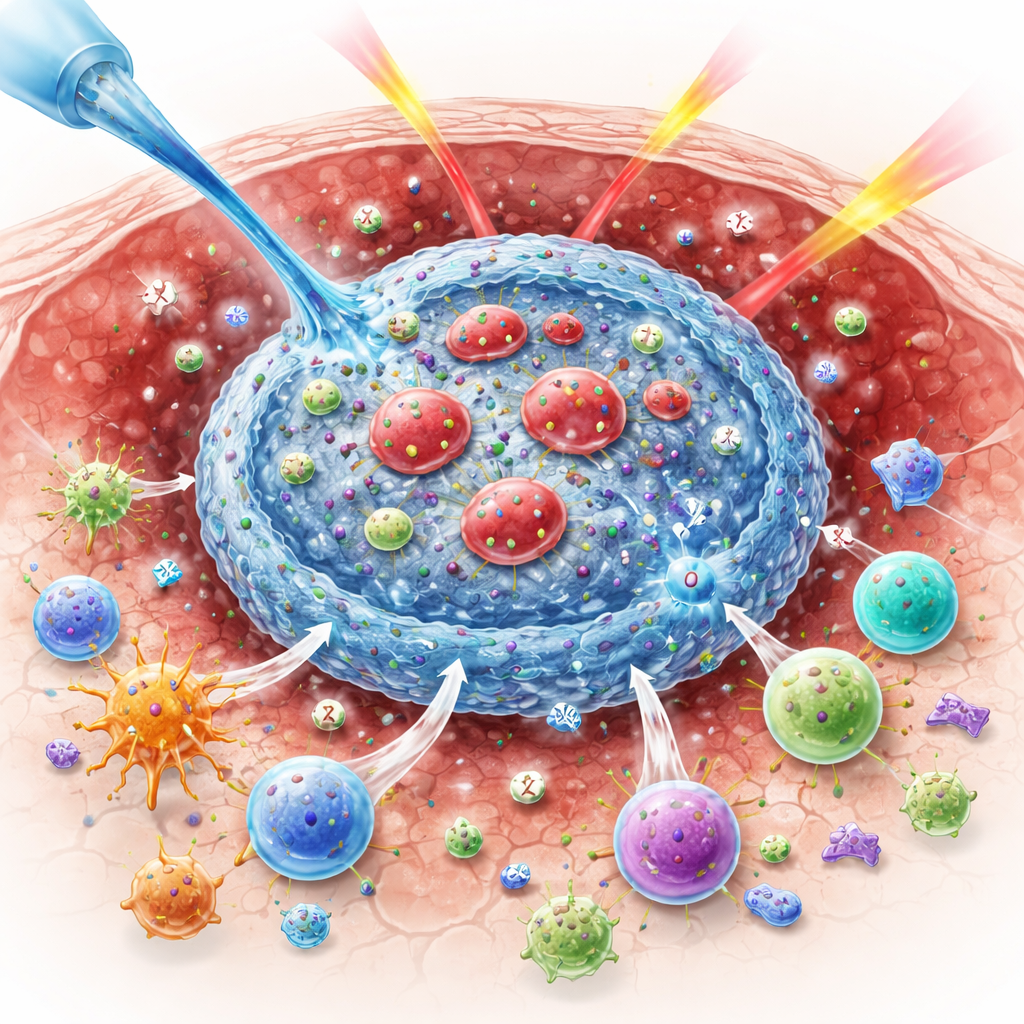
为什么氧气对战胜肿瘤很重要
放射线部分通过产生高度反应性的氧分子来断裂癌细胞的DNA,从而杀死癌细胞。当肿瘤缺氧时,这类化学反应效率降低,因而更多的癌细胞得以存活。与此同时,放射线对免疫系统发出的是混合信号:它可以揭示肿瘤蛋白,使肿瘤被识别为危险,但也可能增强免疫细胞的“刹车”——例如检查点蛋白CTLA-4,并有利于抑制性调节性T细胞的存在,从而抑制攻击。这些相互对立的效应有助解释为何在患者身上,将放疗与免疫药物联用的效果常常不如在小鼠模型中理想。
在肿瘤内构建的活性凝胶
研究人员设计了一种只在肿瘤酸性环境中自组装的材料。它由三种关键成分组成:一种天然糖类聚合物——海藻酸盐,一种无机粉末——过氧化钡,以及经温和工程化、携带两种免疫药物的红细胞。将混合物注入肿瘤后,酸性条件触发过氧化钡分解,释放钡离子和过氧化氢。钡离子立刻使海藻酸盐发生交联,形成柔软的水凝胶,将工程化红细胞固定其中,防止药物被冲走。与此同时,红细胞内天然存在的酶将过氧化氢转化为氧气,有助于缓解肿瘤缺氧,使肿瘤更易受到放疗的作用。
双重免疫信号的时序释放
该系统的真正威力在于它如何错开两种免疫制剂的释放时序:一种阻断CTLA-4的抗体和一种名为白细胞介素-12(IL-12)的细胞因子。抗体装载在红细胞内部,而IL-12则锚定在其表面。随着氧气的产生,红细胞膜产生孔隙,使阻断CTLA-4的抗体迅速逸出。早期的这一爆发解除免疫抑制,促使树突状细胞将肿瘤抗原携带到邻近的淋巴结,并帮助激活特异性肿瘤T细胞。相比之下,IL-12随着水凝胶结构逐步松弛而缓慢渗出。后期信号促使T细胞和自然杀伤细胞产生干扰素-γ,推动更多效应性杀伤细胞进入肿瘤,并强化免疫哨兵与效应细胞之间的正反馈循环。
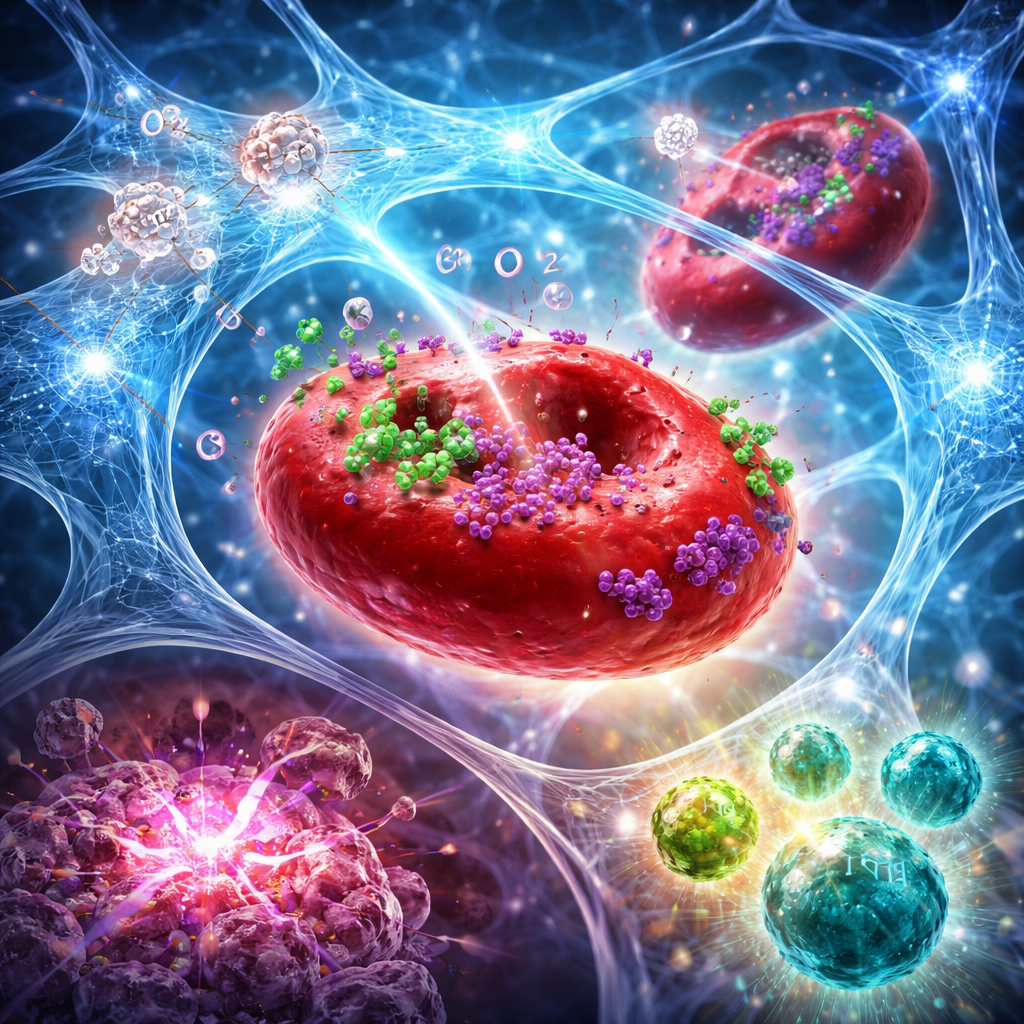
从局部注射到全身性免疫攻击
在侵袭性乳腺癌和胰腺癌的小鼠模型中,将该水凝胶与聚焦放射联合使用的效果不仅仅是缩小被治疗的肿瘤。联合方法使肿瘤内的氧气水平维持数日,增强了放射引起的DNA损伤,并触发了一种更明显的细胞死亡形式,这种死亡天然地将肿瘤标记为免疫识别的目标。流式细胞术和组织染色显示肿瘤微环境发生显著变化:细胞毒性CD8 T细胞和自然杀伤细胞增多,调节性T细胞减少,“效应”与“抑制”细胞的比例升高。淋巴结中专门的树突状细胞也增加,表明抗原呈递更为有效。许多小鼠出现肿瘤完全消退,有些在数周后再次接种癌细胞时仍受保护,提示形成了持久的免疫记忆。
安全性、可行性与未来方向
由于凝胶在局部形成并固定载荷,只有少量IL-12和抗CTLA-4泄入血液,降低了像细胞因子风暴或器官损伤等严重副作用的风险,这些副作用在过去限制了这些制剂的应用。构成材料——海藻酸盐、红细胞和过氧化钡——相对廉价且易于扩展生产,这提高了将该策略适配于不同癌种的希望。尽管在制造、质量控制以及将凝胶递送到深部或广泛转移肿瘤方面仍存在挑战,这项工作展示了一种有前景的方式,能够将放疗与精确时序的免疫激活同步化,把一种物理性治疗转变为激发全身抗肿瘤免疫的强力触发器。
这对患者可能意味着什么
通俗地说,这项研究表明,与其分别给与放疗和免疫药物并寄希望于它们自然协同,不如把它们打包进一种智能材料,置于肿瘤内,自行产生氧气,并按精心编排的顺序释放免疫信号。在动物实验中,这种方法不仅使放疗对癌细胞更具杀伤力,还训练免疫系统识别并记住肿瘤,有助于防止复发。如果在人类中也能获得类似结果,这类水凝胶有朝一日可能将难治肿瘤变为机体自身防御能够可靠发现并清除的目标。
引用: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
关键词: 放射免疫治疗, 水凝胶, 癌症免疫疗法, 肿瘤微环境, 放疗